کدام اسید خطرناک ترین است؟ قوی ترین اسید دنیا قوی ترین ابر سیال. شگفت انگیزترین مواد قوی ترین اسید بدون اکسیژن
انسان همیشه به دنبال یافتن موادی بوده که هیچ شانسی برای رقبای خود باقی نمی گذارد. از زمان های قدیم، دانشمندان به دنبال سخت ترین مواد در جهان، سبک ترین و سنگین ترین بوده اند. عطش کشف منجر به کشف شد گاز ایده آلو بدنی کاملا مشکی ما بیشترین را به شما ارائه می دهیم مواد شگفت انگیزدر جهان.
1. سیاه ترین ماده
سیاه ترین ماده در جهان Vantablack نام دارد و از مجموعه ای از نانولوله های کربنی تشکیل شده است (کربن و آلوتروپ های آن را ببینید). به بیان ساده، این ماده از «موهای» بیشماری تشکیل شده است که پس از گیرکردن در آنها، نور از یک لوله به لوله دیگر میپرد. به این ترتیب، حدود 99.965٪ از شار نور جذب می شود و تنها بخش کوچکی به عقب منعکس می شود.
کشف Vantablack چشم انداز گسترده ای را برای استفاده از این ماده در نجوم، الکترونیک و اپتیک باز می کند.
2. قابل اشتعال ترین ماده
تری فلوراید کلر قابل اشتعال ترین ماده ای است که تاکنون وجود داشته است برای بشر شناخته شده است. این یک عامل اکسید کننده قوی است و تقریباً با همه آنها واکنش نشان می دهد عناصر شیمیایی. تری فلوراید کلر می تواند بتن را بسوزاند و به راحتی شیشه را مشتعل کند! استفاده از تری فلوراید کلر به دلیل اشتعال پذیری فوق العاده و عدم امکان اطمینان از استفاده ایمن عملا غیرممکن است.
3. سمی ترین ماده
قوی ترین سم سم بوتولینوم است. ما آن را با نام بوتاکس می شناسیم که در زیبایی به آن می گویند، جایی که کاربرد اصلی خود را پیدا کرده است. سم بوتولینوم یک ماده شیمیایی است که توسط باکتری کلستریدیوم بوتولینوم تولید می شود. سم بوتولینوم علاوه بر اینکه سمی ترین ماده است، بیشترین وزن مولکولی را نیز در بین پروتئین ها دارد. سمیت خارقالعاده این ماده با این واقعیت مشهود است که تنها 0.00002 میلیگرم در دقیقه سم بوتولینوم برای نیم روز برای انسان کشنده کردن ناحیه آسیبدیده کافی است.
4. داغ ترین ماده
این به اصطلاح پلاسمای کوارک گلوئون است. این ماده از برخورد اتم های طلا با سرعت نزدیک به نور ایجاد شده است. پلاسمای کوارک گلوئون دارای دمای 4 تریلیون درجه سانتیگراد است. برای مقایسه، این رقم 250000 برابر بیشتر از دمای خورشید است! متأسفانه عمر ماده به یک تریلیونم یک تریلیونم ثانیه محدود شده است.
5. بیشترین اسید کاستیک
در این نامزدی، قهرمان اسید فلوراید-آنتیمونی H است. اسید فلوراید-آنتیمونی 2×1016 (دویست کوینتیلیون) برابر بیشتر از اسید سولفوریک است. این ماده بسیار فعال است و اگر مقدار کمی آب به آن اضافه شود می تواند منفجر شود. دودهای این اسید سمی کشنده است.
6. مواد منفجره ترین
انفجاری ترین ماده هپتانیتروکوبان است. بسیار گران است و فقط برای آن استفاده می شود تحقیق علمی. اما اکتوژن کمی کمتر انفجاری با موفقیت در امور نظامی و زمین شناسی هنگام حفاری چاه استفاده می شود.
7. پرتوزاترین ماده
پولونیوم 210 ایزوتوپ پلونیوم است که در طبیعت وجود ندارد، اما توسط انسان ساخته شده است. برای ایجاد منابع انرژی مینیاتوری، اما در عین حال بسیار قدرتمند استفاده می شود. نیمه عمر بسیار کوتاهی دارد و بنابراین می تواند باعث بیماری شدید تشعشع شود.
8. سنگین ترین ماده
این البته فولریت است. سختی آن تقریبا 2 برابر بیشتر از الماس طبیعی است. می توانید در مقاله سخت ترین مواد در جهان درباره فولریت بیشتر بخوانید.
9. قوی ترین آهنربا
قوی ترین آهنربا در جهان از آهن و نیتروژن ساخته شده است. در حال حاضر، جزئیات در مورد این ماده در دسترس عموم نیست، اما از قبل مشخص شده است که ابر آهنربای جدید 18٪ قوی تر از قوی ترین آهنرباهایی است که در حال حاضر استفاده می شود - نئودیمیم. آهنرباهای نئودیمیم از نئودیمیم، آهن و بور ساخته می شوند.
10. سیال ترین ماده
هلیوم 2 ابر سیال تقریباً در دماهای نزدیک به صفر مطلق ویسکوزیته ندارد. این خاصیت به دلیل آن است دارایی منحصر به فردنشت کرده و از ظرف ساخته شده از هر ماده جامد بیرون بریزید. هلیوم II چشم اندازی برای استفاده به عنوان یک رسانای حرارتی ایده آل دارد که در آن گرما از بین نمی رود.
بیش از یک نسل از شیمیدانان در مورد اینکه کدام اسید قوی ترین است بحث کردند. که در زمان های مختلفاین عنوان به اسید نیتریک، سولفوریک و کلریدریک داده شد. برخی معتقد بودند که هیچ ترکیبی قوی تر از اسید هیدروفلوئوریک وجود ندارد. اخیراً ترکیبات جدیدی با خواص اسیدی قوی به دست آمده است. شاید در میان آنها قوی ترین اسید دنیا پیدا شود؟ این مقاله به بررسی ویژگیهای قویترین اسیدهای ماندگار زمان ما میپردازد و ویژگیهای شیمیایی مختصری را ارائه میدهد.
مفهوم اسید
شیمی یک علم کمی است. و عنوان "قوی ترین اسید" را باید به طور منطقی به یک ماده خاص نسبت داد. شاخص اصلی که قدرت هر اتصال را مشخص می کند چه می تواند باشد؟
ابتدا بیایید تعریف کلاسیک اسید را به یاد بیاوریم. این کلمه عمدتاً برای ترکیبات شیمیایی پیچیده که از هیدروژن و یک باقی مانده اسید تشکیل شده است استفاده می شود. تعداد اتم های هیدروژن در یک ترکیب به ظرفیت باقیمانده اسید بستگی دارد. به عنوان مثال، در یک مولکول اسید هیدروکلریک تنها یک اتم هیدروژن وجود دارد. و اسید سولفوریک در حال حاضر دارای دو اتم H + است.

خواص اسیدها
همه اسیدها مقداری دارند خواص شیمیایی، که می توان آن را برای یک کلاس معین از ترکیبات شیمیایی مشترک نامید.

در تمام ویژگی های فوق ، "مهارت" دیگری از هر اسید شناخته شده آشکار می شود - این توانایی رها کردن اتم هیدروژن و جایگزینی آن با اتم ماده شیمیایی دیگر یا مولکول هر ترکیب است. این توانایی است که "قدرت" اسید و میزان تعامل آن با سایر عناصر شیمیایی را مشخص می کند.
آب و اسید
وجود آب توانایی اسید برای اهدای اتم های هیدروژن را به میزان قابل توجهی کاهش می دهد. این با این واقعیت توضیح داده می شود که هیدروژن قادر به تشکیل خود است پیوندهای شیمیاییبین مولکول های اسید و آب، در نتیجه توانایی آن برای جدا شدن از پایه کمتر از اسیدهای رقیق نشده است.
سوپر اسید
کلمه "سوپراسید" در سال 1927 با کمک شیمیدان مشهور جیمز کانانت وارد فرهنگ لغت شیمیایی شد.
استاندارد قدرت این ترکیب شیمیایی اسید سولفوریک غلیظ است. ماده شیمیایی یا هر مخلوطی که اسیدی تر از اسید سولفوریک غلیظ باشد، سوپراسید نامیده می شود. ارزش یک سوپراسید با توانایی آن در ایجاد بار الکتریکی مثبت به هر پایه تعیین می شود. شاخص مربوطه H 2 SO 4 به عنوان پارامتر اساسی برای تعیین اسیدیته در نظر گرفته می شود. در میان اسیدهای قوی، موادی با نام ها و خواص نسبتاً غیر معمول وجود دارد.
اسیدهای قوی شناخته شده
معروف ترین اسیدها از دوره شیمی معدنی عبارتند از: اسیدهای هیدرویدیک (HI)، هیدروبرومیک (HBr)، هیدروکلریک (HCl)، سولفوریک (H2SO4) و نیتریک (HNO3). همه آنها شاخص اسیدیته بالایی دارند و قادر به واکنش با اکثر فلزات و بازها هستند. در این سری، قوی ترین اسید مخلوطی از اسید نیتریک و هیدروکلریک اسید است که به آن "آکوا رژیا" می گویند. فرمول قوی ترین اسید در این سری HNO 3+3 HCl است. این ترکیب قادر است حتی فلزات گرانبها مانند طلا و پلاتین را نیز در خود حل کند.

به اندازه کافی عجیب، اسید هیدروفلوئوریک، که ترکیبی از هیدروژن با قوی ترین هالوژن - فلوئور است، در رقبای عنوان "قوی ترین اسید در شیمی" قرار نگرفت. تنها ویژگی این ماده توانایی آن در حل کردن شیشه است. بنابراین، چنین اسیدی در ظروف پلی اتیلن ذخیره می شود.
اسیدهای آلی قوی
مدعیان عنوان "قوی ترین اسید در شیمی ارگانیک» - اسیدهای فرمیک و استیک. اسید فرمیک قوی ترین در سری همولوگ اسیدهای اشباع است. این نام به دلیل وجود مقداری از آن در ترشحات مورچه ها است.

اسید استیک کمی ضعیف تر از اسید فرمیک است، اما طیف توزیع آن بسیار گسترده تر است. اغلب در آب گیاهان یافت می شود و در طی اکسیداسیون مواد آلی مختلف تشکیل می شود.
پیشرفت های اخیر در زمینه شیمی امکان سنتز ماده جدیدی را فراهم کرده است که می تواند با مواد آلی سنتی رقابت کند. اسید تری فلورومتان سولفونیک دارای شاخص اسیدیته بالاتر از اسید سولفوریک است. علاوه بر این، CF3SO3H یک مایع رطوبت سنجی پایدار با خواص فیزیکوشیمیایی ثابت در شرایط عادی است. امروزه می توان عنوان «قوی ترین اسید آلی» را به این ترکیب نسبت داد.
بسیاری ممکن است فکر کنند که درجه اسیدیته نمی تواند به طور قابل توجهی بالاتر از اسید سولفوریک باشد. اما اخیراً دانشمندان تعدادی از مواد را سنتز کرده اند که پارامترهای اسیدیته آنها چندین هزار برابر بیشتر از اسید سولفوریک است. ترکیباتی که از واکنش اسیدهای پروتیک با اسیدهای لوئیس به دست میآیند دارای مقادیر اسیدی غیرعادی بالایی هستند. که در دنیای علمیبه آنها می گویند: اسیدهای پروتیک پیچیده.
اسید جادویی
آره. همه چیز درست است. اسید جادویی اسمش همینه ماژیک اسید مخلوطی از هیدروژن فلوراید یا فلوروسولفورونیک اسید با پنتا فلوراید آنتیموان است. فرمول شیمیاییاین اتصال در شکل نشان داده شده است:

این نام عجیباسید جادویی در جشن کریسمس شیمیدانان که در اوایل دهه 1960 برگزار شد، به دست آمد. یکی از اعضای گروه تحقیقاتی J. Olah با حل کردن یک شمع مومی در این مایع شگفتانگیز، ترفند خندهداری را به نمایش گذاشت. این یکی از قوی ترین اسیدهای نسل جدید است، اما ماده ای که از نظر قدرت و اسیدیته از آن پیشی می گیرد قبلاً سنتز شده است.
قوی ترین اسید دنیا
اسید کربوران اسید کربوران است که با اختلاف قوی ترین ترکیب در جهان است. فرمول قوی ترین اسید به این صورت است: H(CHB11Cl11).
این هیولا در سال 2005 در دانشگاه کالیفرنیا با همکاری نزدیک موسسه کاتالیزوری نووسیبیرسک SB RAS ساخته شد.
ایده سنتز همراه با رویای مولکولها و اتمهای جدید که تاکنون دیده نشده بود، در ذهن دانشمندان پدید آمد. اسید جدید یک میلیون بار قوی تر از اسید سولفوریک است، با این حال اصلاً تهاجمی نیست و قوی ترین اسید را می توان به راحتی در یک بطری شیشه ای ذخیره کرد. درست است، با گذشت زمان شیشه حل می شود و با افزایش دما، سرعت این واکنش به طور قابل توجهی افزایش می یابد.

این نرمی شگفت انگیز به دلیل پایداری بالای ترکیب جدید است. مانند تمام مواد شیمیایی اسیدی، اسید کربوران به راحتی واکنش نشان می دهد و تنها پروتون خود را اهدا می کند. در این حالت، باز اسیدی آنقدر پایدار است که واکنش شیمیایی بیشتر ادامه نمی یابد.
خواص شیمیایی کربوران اسید
اسید جدید یک دهنده عالی پروتون H+ است. این همان چیزی است که قدرت این ماده را تعیین می کند. محلول اسید کربوران بیش از هر اسید دیگری در جهان یون هیدروژن دارد. که در واکنش شیمیایی SbF 5 - پنتا فلوراید آنتیموان، یلون فلوئور را متصل می کند. در این حالت اتم های هیدروژن بیشتر و بیشتر آزاد می شوند. بنابراین، اسید کربن قوی ترین در جهان است - تعلیق پروتون ها در محلول آن 2 × 10 19 برابر بیشتر از اسید سولفوریک است.
با این حال باز اسیداین ارتباط به طرز شگفت انگیزی پایدار است. مولکول این ماده از یازده اتم برم و به همان تعداد اتم کلر تشکیل شده است. در فضا، این ذرات یک شکل پیچیده و از نظر هندسی منظم را تشکیل می دهند که به آن ایکوساهدر می گویند. این آرایش اتم ها پایدارترین است و این پایداری اسید کربوران را توضیح می دهد.

معنی اسید کربوران
قوی ترین اسید در جهان جوایز و شناخت شایسته ای را برای سازندگان خود در دنیای علمی به ارمغان آورد. اگرچه تمام خواص ماده جدید به طور کامل شناخته نشده است، اما اکنون مشخص شده است که اهمیت این کشف فراتر از آزمایشگاه ها و موسسات تحقیقاتی است. کربوران اسید می تواند به عنوان یک کاتالیزور قوی در واکنش های صنعتی مختلف استفاده شود. علاوه بر این، اسید جدید می تواند با سرسخت ترین مواد شیمیایی - گازهای بی اثر - تعامل داشته باشد. در حال حاضر، کار در حال انجام است تا زنون بتواند واکنش نشان دهد.
بدون شک خواص شگفت انگیز اسیدهای جدید کاربرد خود را در زمینه های مختلف علم و فناوری پیدا خواهد کرد.
اسیدهای زیادی وجود دارند که حتی در مقادیر کم، برای انسان خطرناک هستند. بسیاری از مردم معتقدند که اسید سولفوریک خطرناک ترین است، اما این کاملاً درست نیست. اسید کربوران قوی ترین در نظر گرفته می شود که فقط در ظروف مخصوص قابل نگهداری است. این ماده چندین برابر قوی تر از اسید سولفوریک است و به شما امکان می دهد تا به سرعت فلزات، شیشه و سایر مواد مقاوم در برابر سایر مواد شیمیایی را حل کنید. اما اگر اسید کربوران بسیار نادر و فقط در شرایط آزمایشگاهی باشد، می توانید با ماده قوی دیگری در زندگی روزمره. به گفته بسیاری از کارشناسان، سمی ترین اسید هیدروسیانیک اسید است و نه تنها در آزمایشگاه، بلکه در مواد غذایی نیز یافت می شود.
چگونه می توانید مسموم شوید؟
اسید هیدروسیانیک بسیار سمی است. هنگامی که وارد بدن انسان می شود، علائم مسمومیت نسبتاً سریع ظاهر می شود. این ماده می تواند با محصولات حاوی آن و همچنین با محصولاتی که با سیانید درمان شده اند وارد بدن شود.
بیشتر این ماده سمی در بادام یافت می شود. مقدار کل می تواند تا 3٪ برسد. انسان فقط باید یک مشت کوچک بادام بخورد تا مسموم شود.علاوه بر این، این ماده خطرناک در دانه های توت ها و برخی میوه ها نیز وجود دارد. اکثر اسیدها حاوی:
- هلو - تا 2.8٪؛
- زردآلو - تا 1.6٪؛
- آلو - تا 0.95٪؛
- گیلاس - حدود 0.8٪؛
- سیب - تقریباً 0.6٪.
در دانههای بادام و هستههای میوه، اسید هیدروسیانیک به صورت خالص وجود ندارد، بلکه به شکل آمیگدالین گلیکوزید است. این ماده است که طعم و عطر خاصی به آجیل می دهد. آمیگدالین زمانی که وارد بدن انسان می شود به سه جزء تجزیه می شود که یکی از آنها هیدروسیانیک اسید است. بادام تلخ به ویژه سرشار از این ماده است، بنابراین بزرگسالان می توانند این محصول را به مقدار کم مصرف کنند، اما کودکان به هیچ وجه نباید آن را بخورند.
شراب های ساخته شده از انواع توت ها و میوه ها با دانه ها خطر بزرگی هستند. شراب دم کرده با گیلاس با هسته، آلو و زردآلو می تواند منجر به مسمومیت شود.
کمپوت و مربای تهیه شده از انواع توت ها به همراه دانه ها خطری برای سلامتی ندارند. هنگامی که تا 80 درجه گرم می شود، اسید هیدروسیانیک به اجزای ایمن تجزیه می شود.
چه مقدار اسید باعث مسمومیت می شود
 مقدار غذایی که برای مسموم شدن باید بخورید می تواند به میزان قابل توجهی متفاوت باشد. بستگی به سن، وزن بدن فرد دارد، شرایط عمومیسلامتی و وجود آسیب شناسی های مزمن. اما میانگین هایی وجود دارد که باید رعایت شود.
مقدار غذایی که برای مسموم شدن باید بخورید می تواند به میزان قابل توجهی متفاوت باشد. بستگی به سن، وزن بدن فرد دارد، شرایط عمومیسلامتی و وجود آسیب شناسی های مزمن. اما میانگین هایی وجود دارد که باید رعایت شود.
اگر 30 مغز بادام، بیش از 50 هسته زردآلو، بیش از 70 هسته آلو یا گیلاس بخورید، مسمومیت شدید ممکن است رخ دهد. اگر بیش از 100 دانه سیب بخورید ممکن است مسموم شوید.
تحت تأثیر خود اسید سمی، مسمومیت کشنده ممکن است رخ دهد. دوز بحرانی آمیگدالین 1 میلی گرم به ازای هر کیلوگرم وزن بدن انسان است. خوردن 40 دانه بادام تلخ یا 100 هسته زردآلو برای مسمومیت کشنده کافی است.
لذیذهایی که واقعاً آجیل بادام را به شکل بدون تغییر دوست دارند، باید این خوراکی لذیذ را فقط از فروشگاه های تخصصی خریداری کنند. بسته بندی باید حاوی تمام اطلاعات مربوط به سازنده و ترکیب محصول باشد. حتی بادام شیرین در صورت مصرف زیاد می تواند منجر به مسمومیت شود.
بادام تلخ در حال حاضر تنها در تولید برخی داروها و محصولات آرایشی و بهداشتی استفاده می شود. چنین آجیل عملا خورده نمی شود.
علائم مسمومیت
اسید هیدروسیانیک، هنگامی که وارد جریان خون می شود، با گلبول های قرمز در تماس است، در حالی که مانع از جدا شدن اکسیژن و انتقال بیشتر آن به بافت ها می شود. به همین دلیل میزان اکسیژن خون به شدت افزایش می یابد، اما به هیچ وجه به اندام ها نمی رسد که منجر به هیپوکسی می شود. مغز در درجه اول تحت تأثیر قرار می گیرد. تمام عملکردهای این اندام به شدت مهار می شود و عملکرد تمام سیستم ها و سایر اندام های مهم بدن مختل می شود.
هنگام مسمومیت با این اسید، علائم مشخصه زیر ظاهر می شود:
- پوست و تمام غشاهای مخاطی صورتی روشن می شوند.
- سردرد شدید و همچنین سرگیجه، لب ها بی حس می شوند و مردمک ها گشاد می شوند.
- عدم تعادل وجود دارد، فرد نمی تواند به طور معمول روی پای خود بایستد، هماهنگی حرکات مختل است.
- نبض تند می شود، مانند تنفس.
- قربانی درد قفسه سینه و تنگی نفس را احساس می کند.
- حالت تهوع و استفراغ رخ می دهد؛
- طعم فلزی و تلخی در دهان وجود دارد.
- ممکن است حرکات روده کنترل نشده وجود داشته باشد.
قربانی بوی مشخصی از بادام تلخ متصاعد می کند که با آن می توان تشخیص داد که فرد مسموم شده است. اگر وضعیت بسیار شدید باشد، تنفس سریع به سرعت با نبض آهسته جایگزین می شود. فلج مرکز تنفسی رخ می دهد و تشنج شروع می شود.
اگر در صورت مسمومیت با اسید هیدروسیانیک، در عرض 3 دقیقه به قربانی کمک نشود، مرگ رخ می دهد.
مراقبت فوری
در صورت مسمومیت با اسید قوی - اسید هیدروسیانیک، باید بلافاصله با آمبولانس تماس بگیرید. قبل از رسیدن پزشکان، به قربانی کمک های اولیه داده می شود که شامل اقدامات زیر است:

پادزهر اسید هیدروسیانیک محلول ضعیف متیلن بلو است. این درمان معمولاً توسط پزشکان اورژانس داده می شود.
پس از ارائه کمک های اولیه، قربانی باید از لباس های تنگ بیرون آورده شود و سرش را با بالش بلند کرده و در رختخواب قرار دهد. اگر فردی هوشیاری آشفته دارد، توصیه می شود که یک سواب پنبه ای مرطوب شده با آمونیاک را بو کند. آمونیاک، یک بار در خون، اسید را خنثی می کند.
اگر فردی تنفس یا نبض ندارد، باید در اسرع وقت فشرده سازی قفسه سینه و انجام تنفس مصنوعی انجام شود. چنین اقداماتی باید در چند دقیقه اول پس از توقف فرآیندهای حیاتی انجام شود.
در یک محیط بیمارستان، به بیمار داروهای ضد تشنج، پادزهر و داروها برای بازگرداندن گردش خون طبیعی داده می شود. در طول روند بهبودی، مجموعه ای از ویتامین ها برای بیمار تجویز می شود.
پس از مسمومیت با اسید هیدروسیانیک، فرد باید تا مدتی از استرس جسمی و روحی خودداری کند. در این زمان به بیمار توصیه می شود مایعات فراوان از جمله شیر بنوشد. همچنین باید در هوای تازه زیاد راه بروید، یک رژیم غذایی متعادل را رعایت کنید و تمام عادات بد را کنار بگذارید.
توسعه سریع علم به دانشمندان اجازه می دهد تا اکتشافات هیجان انگیز جدیدی در زمینه فیزیک، شیمی و سایر زمینه ها داشته باشند. دنیای علمی به طور سیستماتیک از اخبار مربوط به ایجاد مواد جدید با خواص منحصر به فرد و قبلاً دیده نشده شوکه می شود. البته مردم عادی همیشه دنبال چنین اکتشافاتی نیستند. همه نمی دانند که قوی ترین اسید جهان در سال 2005 در آمریکا ساخته شد. برای بسیاری، قوی ترین چنین ماده شیمیایی اسید سولفوریک است که در مدرسه به خوبی مطالعه شده است.
اسید کربن قوی ترین در جهان است
در سال 2005، دانشمندانی که در دانشگاه کالیفرنیا در ایالات متحده آمریکا کار می کردند، موفق به ایجاد اسید جدید با قدرت بی سابقه ای شدند. ترکیب اختراع شده یک میلیون بار قوی تر از اسید سولفوریک غلیظ است. دانشمندان در آن لحظه به دنبال یافتن یک مولکول جدید بودند که به یک کشف واقعی در دنیای علمی تبدیل می شد و موفق شدند به نتیجه مثبتی دست یابند.
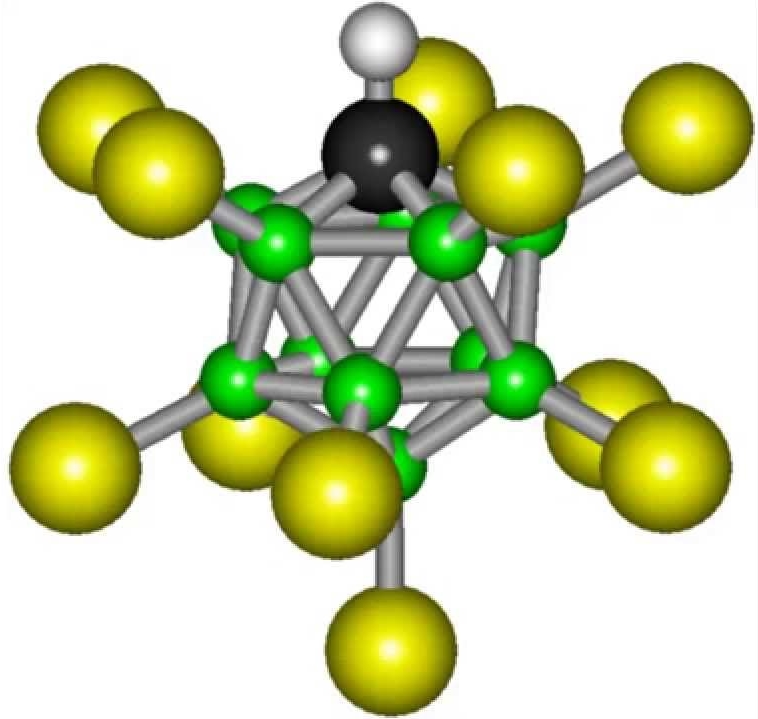
فرمول اسید کربوران خیلی پیچیده نیست: H(CHB11Cl11). اما هنوز هم سنتز چنین ماده ای در یک آزمایشگاه معمولی امکان پذیر نخواهد بود. اسید کربوران بیش از یک تریلیون برابر اسیدی تر از آب معمولی است.
خاصیت منحصر به فرد قوی ترین اسید
اگر در جایی به قوی ترین اسید دنیا اشاره شود، تخیل انسان ماده ای را تصور می کند که هر چیزی را در مسیر خود حل می کند. در واقع، خواص مخرب اصلاً نشانه اصلی قدرت یک ماده شیمیایی نیست. به عنوان مثال، بسیاری معتقد بودند که قوی ترین اسید، اسید هیدروفلوئوریک است، زیرا شیشه را حل می کند. اما این دور از واقعیت است. اسید هیدروفلوریک ظروف شیشه ای را خورده می کند، اما می توان آن را در ظروف پلی اتیلن نگهداری کرد.

به عنوان قوی ترین اسید کربوران در جهان شناخته می شود و به راحتی می توان آن را در ظروف شیشه ای نگهداری کرد. واقعیت این است که این ماده شیمیایی با ثبات شیمیایی قابل توجهی مشخص می شود. مانند سایر ترکیبات مشابه، اسید کربوران هنگام واکنش با معرف ها، اتم های هیدروژن باردار آزاد می کند. پس از چنین واکنشی، ترکیب دارای بار منفی خفیفی است و اثر مخربی روی مواد اطراف ندارد.
کار بیشتر با اسید کربوران
البته سازندگان اسید کربوران در جامعه علمی جهان به خوبی شناخته شده اند. علاوه بر این، به دانشمندان برجسته جوایز شایسته زیادی به دلیل مشارکت قابل توجه آنها در توسعه علم اعطا شد. استفاده از ماده جدید دیگر به آزمایشگاه های علمی محدود نمی شود: اسید کربوران در صنعت به عنوان یک کاتالیزور قوی استفاده می شود.

یکی از ویژگی های منحصر به فرد قوی ترین اسید جهان، توانایی آن در تعامل با گازهای بی اثر است. امروزه مطالعات زیادی برای تعیین امکان واکنش بین زنون و اسید کربوران در حال انجام است. دانشمندان همچنین به طور خستگی ناپذیری برای مطالعه سایر خواص قوی ترین اسید کار می کنند.
معروف ترین اسید قوی
دانشمندان به خوبی از اسید کربوران آگاه هستند. مردم عادی اغلب بر این باورند که اسید سولفوریک قوی ترین است. این به دلیل استفاده مکرر از این ماده در صنعت است. اغلب توسط سازندگان کودهای معدنی برای تولید سوپر فسفات ها و سولفات های آمونیوم استفاده می شود.
اسید سولفوریک به طور گسترده در صنعت متالورژی استفاده می شود. همچنین برای تمیز کردن فلزات از اکسیداسیون استفاده می شود. تولید سوخت مایع بدون استفاده از اسید سولفوریک امکان پذیر نیست. می توان از آن برای تمیز کردن محصولات زیر استفاده کرد:
- روغن های روان کننده؛
- نفت سفید؛
- پارافین؛
- چربی های معدنی

اما این فقط استفاده صنعتی نیست که باعث می شود بسیاری از مردم باور کنند که اسید سولفوریک قوی ترین در جهان است. این عقیده به این دلیل شکل گرفت که این ماده وقتی به گوشت می رسد، آن را ذغال می کند. این خاصیت اسید سولفوریک اغلب در فیلمبرداری فیلم های جنایی استفاده می شود.
قوی ترین اسید آلی
اگر در مورد قوی ترین اسید در شیمی آلی صحبت کنیم، رهبری در اینجا متعلق به اسید فرمیک است. این ماده به این دلیل نامگذاری شد که در ترشحات مورچه ها یافت می شد. اسید فرمیک کاربردهای گسترده ای دارد. اغلب در پزشکی استفاده می شود زیرا دارای خواص ضد درد و تحریک کننده است. اسید فرمیک در بسیاری از پمادها وجود دارد که برای درمان کبودی، واریس و تورم استفاده می شود. داروهای حاوی این ماده می توانند به خلاص شدن از شر آکنه کمک کنند.

اسید فرمیک نیز به طور گسترده در صنایع شیمیایی استفاده می شود. در کشاورزی و زنبورداری نیز کاربرد دارد. این ماده همچنین در مواد غذایی به عنوان افزودنی E236 استفاده می شود.
علیرغم شیوع آن، اسید فرمیک می تواند یک تهدید جدی باشد. تماس ماده غلیظ با پوست باعث سوختگی یا درد شدید می شود. حتی استنشاق بخار اسید فرمیک می تواند به دستگاه تنفسی آسیب برساند. اما خاصیت مثبت ماده این است که به سرعت از بدن خارج می شود بدون اینکه در آن انباشته شود.
بسیاری از مردم سعی می کنند خودشان پاسخ این سوال را پیدا کنند که قوی ترین اسید کدام است. درک این موضوع خیلی سخت نیست، اما باید ادبیات خاصی را بخوانید. برای کسانی که فقط می خواهند جواب آن را بدانند این سوال، این مقاله نوشته شده است.
بسیاری از مردم معتقدند که قوی ترین اسید، اسید هیدروفلوئوریک است، زیرا می تواند شیشه را حل کند. این قضاوت عملاً بی اساس است. در درک دیگران قوی ترین اسید اسید سولفوریک است. جمله آخر یک توضیح کاملاً منطقی دارد. واقعیت این است که اسید سولفوریک در بین موارد مورد استفاده در صنعت بسیار قوی است. در تماس با بافت زنده، می تواند گوشت را زغال کند و سوختگی های شدیدی بر جای بگذارد که بهبودی طولانی مدت طول می کشد و مشکل ساز است. تولید آن نیازی به هزینه مواد خاصی ندارد. و به جرات می توان گفت که او قوی ترین نیست. علم به اصطلاح سوپراسیدها را می شناسد. در ادامه در مورد آنها صحبت خواهیم کرد. اما در سطح خانواده، رایج ترین اسیدهای قوی هنوز هم اسید سولفوریک است. به همین دلیل است که او خطرناک است.
پس چگونه یک اسید می تواند قوی و ملایم باشد؟ پاسخ در این است که چگونه شیمیدانان قدرت یک اسید را تعیین می کنند. قدرت اسیدی توانایی اسید برای افزودن یون هیدروژن به مولکول های اساسی است. وی خاطرنشان کرد: نمونه دیگر انتخاب اسید برای تمیز کردن رسوبات آهکی داخل کتری مسی است. یک صاحب خانه عاقل، اسید کلریدریک را به اسید نیتریک انتخاب می کند، زیرا قسمت کلر اسید هیدروکلریک به مس حمله نمی کند، در حالی که قسمت نیترات اسید نیتریک، کتری را در یک آشغال از بخارهای قهوه ای سمی حل می کند.
بسیاری از شیمیدانان مدرن معتقدند که قوی ترین اسید در جهان کربوران است. این را نتایج تحقیقات کامل تأیید می کند. این اسید بیش از یک میلیون برابر قوی تر از اسید سولفوریک غلیظ است. خاصیت خارق العاده آن قابلیت نگهداری در لوله آزمایش است که بسیاری از مواد دیگر سری مذکور فاقد آن هستند. ترکیب شیمیایی، که سوز آورترین در نظر گرفته می شد، در ظروف شیشه ای قابل نگهداری نبود. واقعیت این است که اسید کربوران پایداری شیمیایی قابل توجهی دارد. مانند سایر مواد مشابه خود، هنگام واکنش با دیگر معرف ها، اتم های هیدروژن را با بار به آنها اهدا می کند. با این حال، ترکیب باقی مانده پس از واکنش، اگرچه دارای بار منفی است، بسیار پایدار است و نمی تواند بیشتر عمل کند. اسید کربوران فرمول ساده ای دارد: H(CHB 11 Cl 11). اما به دست آوردن ماده نهایی در یک آزمایشگاه معمولی آسان نیست. شایان ذکر است که بیش از یک تریلیون بار اسیدی تر از آب معمولی است. به گفته مخترع، این مادهدر نتیجه توسعه مواد شیمیایی جدید ظاهر شد.
اسیدهای جدید "قوی اما ملایم" اسیدهای کربناته نامیده می شوند. راز قدرت آنها دو چیز است. مهمتر از همه، بخش کربنات اسید یک باز بسیار ضعیف است، ضعیف تر از بخش فلوئوروسولفات اسید فلورسولفوریک، که رکورددار قبلی قوی ترین اسید بود. ثانیاً، کربوران ها پایداری شیمیایی استثنایی دارند.
به گفته رید، آنها آرایش ایکو وجهی از یازده اتم بور به اضافه یک اتم کربن دارند که احتمالاً از نظر شیمیایی پایدارترین خوشه اتم ها در کل شیمی است. این بدان معنی است که بخش کربن اسید نمی تواند در شیمی خوردگی و تجزیه که توسط فلوراید و نیترات موجود در اسید هیدروفلوئوریک نشان داده می شود شرکت کند. اسید نیتریک. در نتیجه، اسیدهای کربوران میتوانند یونهای هیدروژن را به مولکولهای ضعیف بازی اضافه کنند، بدون اینکه مولکولهای اغلب ظریف و با بار مثبت تشکیل شده را از بین ببرند.
لیستی از مواد سوزاننده حاوی اسیدهای هیدروفلوئوریک، هیدروفلوریک و سایر اسیدهای قوی است. معرف های صنعتی شامل نمی شوند. با این حال، هنوز باید مراقب اسیدهای رایج مانند سولفوریک، کلریدریک، نیتریک و غیره باشید. من نمی خواهم کسی را بترسانم، اما مواد این لیست معمولاً برای حمله به سلامتی و تغییر شکل عمدی ظاهر استفاده می شود.
رید افزود که این کیفیت قوی و در عین حال ملایم آنهاست. هیچ یک از این مولکول های دارای بار مثبت قبلاً در دمای اتاق "بطری" نشده بودند زیرا اسیدهای استفاده شده قبلی آنها را تجزیه می کردند. رید گفت که اسیدهای کربنانوئیک قوی اما ملایم بر این مشکل غلبه میکنند و به شیمیدانان اجازه میدهند تا نگاه دقیقتری به مولکولهای مهمی داشته باشند که وجود آنها معمولاً زودگذر است. مولکول های اسیدی شده واسطه های کوتاه مدت مهمی در انواع عظیمی از دگرگونی های شیمیایی کاتالیز شده با اسید، از جمله هضم غذا، بهبود بنزین، تشکیل پلیمر، و سنتز دارویی هستند.
 این است که در میان اسیدهای چرب موجود در غذاها، اسید فرمیک قوی ترین است. اغلب برای حفظ سبزیجات و برای اهداف دارویی استفاده می شود، اما فقط به صورت محلول.
این است که در میان اسیدهای چرب موجود در غذاها، اسید فرمیک قوی ترین است. اغلب برای حفظ سبزیجات و برای اهداف دارویی استفاده می شود، اما فقط به صورت محلول.
باز هم باید گفت که قوی ترین اسید کربوران است. اما امروزه باید بیشتر مراقب موادی باشیم که در صنعت و زندگی روزمره استفاده می شود. شیمی یک علم نسبتا مفید و پیچیده است، اما تولید گسترده ترکیبات ساده نیاز به دانش خاصی ندارد و بنابراین به راحتی می توان اسید را در مقادیر کافی بدست آورد. این باعث افزایش خطر در صورت عدم رسیدگی یا اجرای نیت بد می شود.
اسیدهای کربوران چقدر قوی هستند؟ قویترین آنها حداقل یک میلیون بار قویتر از اسید سولفوریک غلیظ و صدها برابر قویتر از رکورددار قبلی، اسید فلوروسولفوریک است. اسید سولفوریک غلیظ در حال حاضر بیش از یک میلیارد بار قوی تر از اسید رقیق استخر یا اسید معده است. محیط های اسیدی برابر یا بیشتر از اسیدیته اسیدهای کربناته قبلاً با افزودن پنتا فلوراید آنتیموان به اسید فلوروسولفوریک به دست آمده است، اما این مخلوط ها بسیار خورنده هستند و محدودیت های دیگری نیز دارند.
به زبان شیمی، اسیدها آن دسته از موادی هستند که توانایی آزاد کردن کاتیون های هیدروژن را نشان می دهند، یا موادی که توانایی پذیرش یک جفت الکترون را در نتیجه تشکیل دارند. پیوند کووالانسی. با این حال، در مکالمه معمولی، اسید اغلب تنها به عنوان آن دسته از ترکیباتی شناخته می شود که وقتی در محلول های آبی تشکیل می شوند، H30+ اضافی تولید می کنند. وجود این کاتیون ها در محلول به ماده طعم ترش و توانایی واکنش به شاخص ها می دهد. در این مطلب در مورد اینکه کدام ماده قوی ترین اسید است و همچنین در مورد سایر مواد اسیدی صحبت خواهیم کرد.
اسیدهایی که اینقدر قوی هستند سوپراسید نامیده می شوند و با هیدروکربن های نفت در فرآیندی به نام ترک هیدروکربنی واکنش می دهند. این یک فرآیند مهم در افزایش سطح اکتان بنزین است. رید گفت که اسیدهای جدید می توانند در درک و بهبود این فرآیند بسیار مهم باشند. اسیدهای کربنی این میدان را حتی فراتر می برد.
معروف ترین اسید قوی
بسیاری از مولکول های دیگر وجود دارند که به طور نامنظم با اسیدهای سنتی واکنش نشان می دهند و بنابراین چندان مفید نیستند. اسیدهای کربوران اسیدیته بسیار تمیزی را بدون هیچ گونه وحشی ارائه می دهند. بنابراین، کاتالیز اسید پاک واکنش های مهم برای تولید داروها و فرآورده های نفتی باید امکان پذیر باشد.
آنتیموان پنتافلوراید هیدروفلوریک اسید (HFSbF5)
برای توصیف اسیدیته یک ماده، یک نشانگر PH وجود دارد که لگاریتم اعشاری منفی غلظت یون های هیدروژن است. برای مواد معمولی، این شاخص از 0 تا 14 متغیر است. با این حال، این شاخص برای توصیف HFSbF5، که به آن "سوپر اسید" نیز میگویند، مناسب نیست.
رید می گوید: تحقیقات ما شامل ساخت مولکول هایی است که قبلا هرگز ساخته نشده اند. اسیدهای کربنی این امکان را به ما می دهند. این ارزش واقعی این مطالعه است. علم پیشرفت می کند و در عین حال دانش آموزان با تبدیل شدن به دانش، هیجان کشف را تجربه می کنند.
دانشگاه کالیفرنیا، ریورساید، کاندیدای دکترا است دانشگاه تحقیقاتی، یک آزمایشگاه زنده برای تحقیقات نوآورانه در مورد مسائل مهم برای کالیفرنیای جنوبی، ایالت و جوامع در سراسر جهان. اسید قوی به عنوان مقدار pH تعریف می شود که قدرت هیدروژن است که اسید را قوی می کند. با این حال، مقدار pH به ترتیب صعودی کار نمی کند. هر چه مقدار pH کمتر باشد، اسید قوی تر خواهد بود. محدوده pH از 1 تا محلول هایی با مقدار pH کمتر از 7 اسید در نظر گرفته می شوند، در حالی که محلول های با pH بیشتر از 7 باز در نظر گرفته می شوند.
اطلاعات دقیقی در مورد فعالیت این ماده وجود ندارد، اما مشخص است که حتی محلول 55 درصدی HFSbF5 تقریباً 1000000 برابر قوی تر از H2SO4 غلیظ است که در اذهان عادی یکی از قوی ترین اسیدها محسوب می شود. با این حال، پنتا فلوراید آنتیموان یک معرف نسبتا نادر است و خود این ماده فقط در شرایط آزمایشگاهی ایجاد شده است. در مقیاس صنعتی تولید نمی شود.
لیست قوی ترین اسیدها و کاربرد آنها
اسیدهای با مقدار pH کمتر از 1 قوی ترین و محلول هایی با مقدار pH بالای 13 به عنوان پایه قوی در نظر گرفته می شوند. مقدار pH 2 است و یکی از اسیدهای مفید محسوب می شود. نمک یا کرم تارتار موجود در آن به طور طبیعی در طول شراب سازی ایجاد می شود. با بی کربنات سدیم مخلوط می شود و به صورت تجاری به عنوان محصولات پخته به فروش می رسد. در آشپزی استفاده می شود و طعم ترش بی نظیری دارد.
این یک واقعیت است که منبع الماس های موجود در درب یا ته بطری است. این به عنوان استفاده می شود ترکیب آلی، و با کمک همه موجودات زنده تولید می شود. این شیرینی ها حاوی هشدارهایی در مورد آنها هستند و به مشتریان اطلاع می دهند که ممکن است باعث تحریک دهان شوند. لیمو به طور معمول در لیمو یافت می شود و دارای مقدار pH است. معمولاً در غذاهای مرکبات یافت می شود و همچنین به عنوان یک واسطه در چرخه اسید سیتریک که در متابولیسم موجودات هوازی رخ می دهد عمل می کند. این اسید قوی و خوراکی است که در طعم غذاها و نوشیدنی ها مانند نوشابه ها استفاده می شود. و لیموناد
کربورانوئیک اسید (H(CHB11Cl11))
یک اسید فوق العاده دیگر. H(CHB11Cl11)) قوی ترین اسید موجود در جهان است که می توان آن را در ظروف مخصوص نگهداری کرد. مولکول ماده به شکل ایکوسادرون است. اسید کربوران بسیار قوی تر از اسید سولفوریک است. می تواند فلزات و حتی شیشه را حل کند.
این ماده در دانشگاه کالیفرنیا در ایالات متحده آمریکا با مشارکت دانشمندان موسسه فرآیندهای کاتالیزوری نووسیبیرسک ساخته شده است. همانطور که یکی از کارمندان دانشگاه آمریکایی گفت، ایده پشت این خلقت، تمایل به ایجاد مولکول هایی بود که قبلا برای کسی ناشناخته بود.
آن را به بستنی اضافه می کنند، جایی که به عنوان یک امولسیفایر عمل می کند که از آزاد شدن چربی ها جلوگیری می کند. همچنین به عنوان یک عامل تمیز کننده عمل می کند و می تواند برای حذف آهک از اواپراتورها و بویلرها استفاده شود. آب را نرم می کند و در ساخت مواد شوینده و صابون های لباسشویی مفید است. بی بو است و می توان از آن در مکمل های آرایشی و غذایی استفاده کرد.
از این رو، در طیف گسترده ای از محصولات صنعتی و همچنین داخلی استفاده می شود. گوگرد همچنین به عنوان گوگرد شناخته می شود. مقدار pH 5 است و این ترکیب شیمیایی. شواهد کمی مبنی بر وجود آن در محلول وجود دارد، اما در فاز گاز وجود دارد. پایه های این امر آنیون های معمولی، بی سولفات و سولفیت هستند. به عنوان یک عامل کاهش دهنده و ضد عفونی کننده عمل می کند. آنها همچنین به عنوان سفید کننده های ملایم عمل می کنند و می توانند به موادی که توسط سفید کننده های کلر از بین می روند کمک کنند.
قدرت H(CHB11Cl11)) به این دلیل است که یون هیدروژن را کاملاً اهدا می کند. در محلول های این ماده، غلظت این یون ها بسیار بیشتر از سایرین است. بخش دیگر مولکول، پس از آزاد شدن هیدروژن، شامل یازده اتم کربن است که یک ایکوساهدر را تشکیل میدهند که ساختار نسبتاً پایداری است و بی اثر بودن خوردگی را افزایش میدهد.
مقدار pH آن 5 است و یک اسید معدنی است. ماده افزودنی غذایی بازدارنده زنگ مورد استفاده در محصولات دندانپزشکی. همچنین یک جامد کریستالی است، به عنوان یک عامل کاهنده عمل می کند و دارای یک پایه مزدوج است.
یکی دیگر از قوی ترین اسیدها، هیدروژن فلوراید آشناتر است. صنعت آن را به صورت محلول هایی تولید می کند، اغلب چهل، پنجاه یا هفتاد درصد. این ماده نام خود را مدیون فلورسپار است که به عنوان ماده اولیه هیدروژن فلوراید عمل می کند.
این ماده رنگ ندارد. هنگامی که در H20 حل می شود، آزاد شدن قابل توجهی از گرما رخ می دهد. در دماهای پایین، HF قادر به تشکیل ترکیبات ضعیف با آب است.
رطوبت هوا را جذب می کند و یک جامد کریستالی بی رنگ است. به شکل شربت در می آید و وقتی با دمای بالا آزاد می شود در آب حل می شود. این مقدار pH 0 است و مایعی بی رنگ است. برای استفاده می شود. تولید نیترات های معدنی و آلی تولید ترکیبات نیترو برای کودها رنگ - مواد واسطه مواد شیمیایی آلی مواد منفجره. اگر فرد دائماً در معرض بخارات باشد، می تواند باعث پنومونیت شیمیایی و برونشیت مزمن شود.
این ماده شیشه و بسیاری از مواد دیگر را خورده می کند. برای حمل و نقل آن از پلی اتیلن استفاده می شود. با اکثر فلزات بسیار خوب واکنش می دهد. با پارافین واکنش نمی دهد.
کاملا سمی و دارای اثر مخدر است. اگر بلعیده شود، می تواند باعث مسمومیت حاد، اختلال در خون سازی، نارسایی اندام ها و اختلال در سیستم تنفسی شود.
این مایع بی رنگ است که با رها شدن در آب، بخارهای سفیدی از خود خارج می کند. دو نام دیگر برای این اسید، اکسید سولفوریک و انیدرید سولفوریک است. به طور گسترده ای در تولید مواد شیمیایی و مواد منفجره استفاده می شود. به عنوان مثال در ساخت شوینده های مصنوعی، داروها، رنگ ها و رنگدانه های صنعتی، کودها و غیره استفاده می شود. قرار گرفتن در معرض طولانی مدت ممکن است اثرات منفی بر سلامتی داشته باشد و ممکن است به شدت به بدن انسان آسیب برساند.
اسید کلریدریک دارای مقدار pH است. این یک اسید تهاجمی و قوی است که عمدتاً در شرایط آزمایشگاهی استفاده می شود. تشکیل این اسید با حل کردن کلرید هیدروژن در آب انجام می شود. برای بسیاری از موارد مانند تولید کلریدها، کودها و مرگ استفاده می شود. از دیگر کاربردهای اسید می توان به منسوجات، گالوانیزه کردن و ساخت لاستیک اشاره کرد. اگر فردی در معرض این اسید کلریدریک قوی قرار گیرد، قرار گرفتن در معرض آن به موارد زیر منجر می شود.


این ماده یک اسید قوی با دو باز است. گوگرد موجود در ترکیب دارای بالاترین حالت اکسیداسیون (به علاوه شش) است. بی بو و بی رنگ است. اغلب در محلول با آب یا انیدرید سولفوریک استفاده می شود.
چندین راه برای به دست آوردن H2S04 وجود دارد:
- روش صنعتی (اکسیداسیون دی اکسید).
- روش برج (تولید با استفاده از اکسید نیتریک).
- برخی دیگر (بر اساس به دست آوردن ماده ای از برهمکنش دی اکسید گوگرد با مواد مختلف، خیلی رایج نیست).
H2SO4 غلیظ بسیار قوی است، اما محلول های آن نیز یک خطر جدی است. هنگامی که گرم می شود، یک عامل اکسید کننده نسبتاً قوی است. هنگام تعامل با فلزات، آنها اکسید می شوند. در این حالت H2S04 به دی اکسید گوگرد احیا می شود.
H2SO4 بسیار سوزاننده است. این می تواند پوست، دستگاه تنفسی، غشاهای مخاطی و اندام های داخلی انسان را تحت تاثیر قرار دهد. نه تنها وارد شدن آن به بدن، بلکه استنشاق بخارات آن نیز بسیار خطرناک است.
اسید فرمیک (HCOOH)
این ماده یک اسید اشباع با یک باز است. جالب اینجاست که علیرغم قدرت آن به عنوان یک مکمل غذایی استفاده می شود. در شرایط عادی بی رنگ، محلول در استون و به راحتی با آب مخلوط می شود.
HCOOH در غلظت های بالا خطرناک است. با غلظت کمتر از ده درصد فقط اثر تحریک کننده دارد. در سطوح بالاتر، می تواند بافت ها و بسیاری از مواد را خورده کند.
HCOOH غلیظ در تماس با پوست باعث سوختگی بسیار شدید می شود که باعث درد شدید می شود. بخارات این ماده می تواند به چشم ها، اندام های تنفسی و غشاهای مخاطی آسیب برساند. ورود آن به داخل باعث مسمومیت جدی می شود. اما اسید در غلظت های بسیار ضعیف به راحتی در بدن پردازش شده و از آن خارج می شود.

در صورت مسمومیت با متانول، اسید فرمیک نیز در بدن تشکیل می شود. کار او در این فرآیندمنجر به اختلال بینایی به دلیل آسیب به عصب بینایی می شود.
این ماده به مقدار کم در میوه ها، گزنه و ترشحات برخی حشرات یافت می شود.
اسید نیتریک (HNO3)
اسید نیتریک یک اسید قوی با یک باز است. به خوبی با H20 در نسبت های مختلف مخلوط می شود.
این ماده یکی از محبوب ترین محصولات صنایع شیمیایی است. روش های مختلفی برای تهیه آن وجود دارد، اما متداول ترین روش اکسیداسیون آمونیاک در حضور کاتالیزور پلاتین است. HNO3 اغلب در تولید کودهای کشاورزی استفاده می شود. علاوه بر این، از آن در حوزه نظامیدر ایجاد مواد منفجره، در صنعت جواهرسازی، برای تعیین کیفیت طلا و همچنین در ایجاد برخی داروها (مثلا نیتروگلیسیرین).

این ماده برای انسان بسیار خطرناک است. بخارات HNO3 به دستگاه تنفسی و غشاهای مخاطی آسیب می رساند. اسیدی که روی پوست وارد میشود، زخمهایی را از خود به جای میگذارد که بهبودی آنها زمان زیادی طول میکشد. پوست نیز رنگ زردی به خود می گیرد.
هنگامی که در معرض گرما یا نور قرار می گیرد، HNO3 به دی اکسید نیتروژن تجزیه می شود که یک گاز نسبتاً سمی است.
HNO3 با شیشه واکنش نمی دهد، به همین دلیل است که از این ماده برای ذخیره این ماده استفاده می شود. این اسید را ابتدا جابر کیمیاگر به دست آورد.