ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದ ಸಿದ್ಧಾಂತದ ಪರಿಕಲ್ಪನೆ. ರಾಸಾಯನಿಕ ಬಂಧದ ಮಾದರಿಗಳು. ಕ್ರಿಸ್ಟಲ್ ಫೀಲ್ಡ್ ಸಿದ್ಧಾಂತ. ಕಡಿಮೆ ಮತ್ತು ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳು
ದುರ್ಬಲ ಕ್ಷೇತ್ರ ಪ್ರಬಲ ಕ್ಷೇತ್ರ
ಮಧ್ಯಮ ಕ್ಷೇತ್ರ
Frac34;¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾® Δo
3d ಸರಣಿಯ ಅಂಶಗಳೊಂದಿಗೆ ದುರ್ಬಲ ಫೀಲ್ಡ್ ಲಿಗಂಡ್ಗಳು ಹೈ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳನ್ನು ರೂಪಿಸುತ್ತವೆ ಮತ್ತು ಬಲವಾದ-ಫೀಲ್ಡ್ ಲಿಗಂಡ್ಗಳು ಕಡಿಮೆ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳನ್ನು ರೂಪಿಸುತ್ತವೆ. ಅವುಗಳ ನಡುವಿನ ವ್ಯತ್ಯಾಸವು ಡಿ 4 - ಡಿ 7 ಸಂರಚನೆಗಳಿಗೆ ಮಾತ್ರ ಸಂಕೀರ್ಣಗಳ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆಯ ಮೇಲೆ ಪರಿಣಾಮ ಬೀರುತ್ತದೆ:
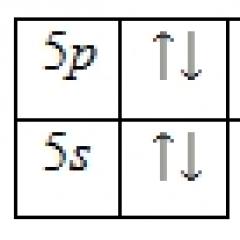
3+ ಡಿ 5 3– ಡಿ 5
ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣ ಕಡಿಮೆ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣ
H 2 O - ದುರ್ಬಲ ಕ್ಷೇತ್ರ ಲಿಗಂಡ್ CN - - ಬಲವಾದ ಕ್ಷೇತ್ರ ಲಿಗಂಡ್
ಕಡಿಮೆ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳು ಯಾವಾಗಲೂ ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳಿಗಿಂತ ಹೆಚ್ಚು ಸ್ಥಿರವಾಗಿರುತ್ತವೆ. ಮಧ್ಯಮ-ಕ್ಷೇತ್ರದ ಲಿಗಂಡ್ಗಳು, ಪರಿಸ್ಥಿತಿಗಳನ್ನು ಅವಲಂಬಿಸಿ (ಕೇಂದ್ರ ಪರಮಾಣುವಿನ ಚಾರ್ಜ್ ಮತ್ತು ಸ್ವಭಾವ), ಹೆಚ್ಚಿನ-ಸ್ಪಿನ್ ಮತ್ತು ಕಡಿಮೆ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳನ್ನು ರಚಿಸಬಹುದು.
ಉದಾಹರಣೆ. TCP ಆಧರಿಸಿ, ಹೆಕ್ಸಾಮೈನ್ ಕೋಬಾಲ್ಟ್ (II) (Δo = 21600 cm–1, P = 21000 cm–1) ಮತ್ತು ಹೆಕ್ಸಾಮೈನ್ ಕೋಬಾಲ್ಟ್ (III) ಅಯಾನುಗಳ (Δo = 9500 cm–1, P = 22500) ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆಯ ಬಗ್ಗೆ ಒಂದು ಊಹೆಯನ್ನು ಮಾಡಿ. cm-1).
ಅಮೋನಿಯವು ಮಧ್ಯಮ-ಕ್ಷೇತ್ರದ ಲಿಗಂಡ್ ಆಗಿದೆ ಮತ್ತು ಲೋಹದ ಆಕ್ಸಿಡೀಕರಣದ ಮಟ್ಟವನ್ನು ಅವಲಂಬಿಸಿ, ಹೆಚ್ಚಿನ-ಸ್ಪಿನ್ ಮತ್ತು ಕಡಿಮೆ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳನ್ನು ರಚಿಸಬಹುದು. ಕೋಬಾಲ್ಟ್ (II) ಮತ್ತು ಕೋಬಾಲ್ಟ್ (III) ಗಾಗಿ ಯಾವ ಸಂಕೀರ್ಣಗಳು ಶಕ್ತಿಯುತವಾಗಿ ಹೆಚ್ಚು ಸ್ಥಿರವಾಗಿರುತ್ತವೆ ಎಂಬುದನ್ನು ನಾವು ಕಂಡುಹಿಡಿಯೋಣ. ಇದನ್ನು ಮಾಡಲು, ಪ್ರತಿ ಅಯಾನಿನ ESC ಅನ್ನು ಬಲವಾದ ಮತ್ತು ದುರ್ಬಲ ಕ್ಷೇತ್ರದಲ್ಲಿ ಹೋಲಿಕೆ ಮಾಡಿ:
(ಎ) 3+, ಡಿ 6

ಬಲವಾದ ಕ್ಷೇತ್ರ ದುರ್ಬಲ ಕ್ಷೇತ್ರ
ESKP (ಬಲವಾದ ಕ್ಷೇತ್ರ) = –6´(2/5)Δo + 2P = –6´(2/5) ´21600 + 2´21000 = –9840 cm –1
ESKP (ದುರ್ಬಲ ಕ್ಷೇತ್ರ) = –4´(2/5)Δo + 2´(3/5)Δo = –4´(2/5) ´21600 + 2´(3/5) ´21600 = –8640 cm – 1
ಕಡಿಮೆ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣದ ಸಂದರ್ಭದಲ್ಲಿ ಶಕ್ತಿಯ ಲಾಭವು ಹೆಚ್ಚಾಗಿರುತ್ತದೆ.
(b) 2+ , d 7

ಬಲವಾದ ಕ್ಷೇತ್ರ ದುರ್ಬಲ ಕ್ಷೇತ್ರ
ESKP (ಬಲವಾದ ಕ್ಷೇತ್ರ) = –6´(2/5)Δo + 1´(3/5)Δo + P = –6´(2/5)´9500 + 1´(3/5) ´9500 + 22500 = 7900 ಸೆಂ-1
ESKP (ದುರ್ಬಲ ಕ್ಷೇತ್ರ) = –5´(2/5)Δo + 2´(3/5)Δo = –5´(2/5) ´9500 + 2´(3/5) ´9500 = –7600 cm – 1
ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣದ ಸಂದರ್ಭದಲ್ಲಿ ಶಕ್ತಿಯ ಲಾಭವು ಹೆಚ್ಚಾಗಿರುತ್ತದೆ.
ಹೀಗಾಗಿ, 3+ ಅಯಾನು ಕಡಿಮೆ-ಸ್ಪಿನ್ ಮತ್ತು 2+ ಅಯಾನು ಹೈ-ಸ್ಪಿನ್ ಆಗಿದೆ.
Δo ಅನ್ನು ಹೆಚ್ಚಿಸುವುದರೊಂದಿಗೆ ESC ಹೆಚ್ಚಾಗುತ್ತದೆ, ಆದಾಗ್ಯೂ, ಇದು ಹೆಚ್ಚಿನ-ಸ್ಪಿನ್ ಮತ್ತು ಕಡಿಮೆ-ಸ್ಪಿನ್ ಸ್ಥಿತಿಗಳಿಗೆ ವಿಭಿನ್ನವಾಗಿರುತ್ತದೆ (Fig. 1.28. Δo = 10Dq ಮೌಲ್ಯದಲ್ಲಿ ಕಾನ್ಫಿಗರೇಶನ್ d 6 ನೊಂದಿಗೆ ಹೆಚ್ಚಿನ-ಸ್ಪಿನ್ ಮತ್ತು ಕಡಿಮೆ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳಿಗೆ ESC ಯ ಅವಲಂಬನೆ . ಎರಡೂ ರಾಜ್ಯಗಳ ಅಸ್ತಿತ್ವವು ಸಾಧ್ಯವಿರುವ ಪ್ರದೇಶವು ಮಬ್ಬಾಗಿದೆ). ಈ ಎರಡು ರೇಖೆಗಳ ಛೇದನದ ಸಮೀಪವಿರುವ ಪ್ರದೇಶವು ಹೆಚ್ಚಿನ-ಸ್ಪಿನ್ ಮತ್ತು ಕಡಿಮೆ-ಸ್ಪಿನ್ ರಾಜ್ಯಗಳಲ್ಲಿ ಅಸ್ತಿತ್ವದಲ್ಲಿರಬಹುದಾದ ಸಂಕೀರ್ಣಗಳಿಗೆ ಅನುರೂಪವಾಗಿದೆ.
ಒಂದು ಉದಾಹರಣೆಯೆಂದರೆ 1,10-ಫೆನಾಂತ್ರೊಲಿನ್ನೊಂದಿಗೆ ಕಬ್ಬಿಣದ (II) ಥಿಯೋಸೈನೇಟ್ ಸಂಕೀರ್ಣ, ಇದು ಕಡಿಮೆ ತಾಪಮಾನದಲ್ಲಿ ಹೆಚ್ಚು-ಸ್ಪಿನ್ (ಪ್ಯಾರಾಮ್ಯಾಗ್ನೆಟಿಕ್) ಮತ್ತು ಎತ್ತರದ ತಾಪಮಾನದಲ್ಲಿ ಕಡಿಮೆ-ಸ್ಪಿನ್ (ಡಯಾಮ್ಯಾಗ್ನೆಟಿಕ್) (M. ಮಾರ್ಚಿವಿ, ಪಿ. ಗುಯೋನ್ಯೂ, ಜೆ. ಎ. ಕೆ. ಹೊವಾರ್ಡ್ , ಜಿ. ಚಾಸ್ಟಾನೆಟ್, ಜೆ.-ಎಫ್. ಲೆಟರ್ಡ್, ಎ. ಇ. ಗೊಯೆಟಾ, ಡಿ. ಚಾಸ್ಸೋ, ಜೆ. ಆಮ್. ಕೆಮ್. ಸೊಕ್., 2002, ವಿ. 124, ಪುಟ 194). ಮಲ್ಟಿಪ್ಲಿಸಿಟಿಯಲ್ಲಿನ ಬದಲಾವಣೆಯು ಅಂತರ ಪರಮಾಣು ಅಂತರಗಳು ಮತ್ತು ಸಮನ್ವಯ ಪರಿಸರದ ರೇಖಾಗಣಿತದ ಬದಲಾವಣೆಯೊಂದಿಗೆ ಇರುತ್ತದೆ: ಕಡಿಮೆ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣವು ನಿಯಮಿತ ಆಕ್ಟಾಹೆಡ್ರನ್ ಆಗಿದೆ ಮತ್ತು ಹೆಚ್ಚಿನ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣವು ವಿಕೃತವಾಗಿದೆ. ಹೆಚ್ಚಿನ ಒತ್ತಡ ಅಥವಾ ವಿಕಿರಣದ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ ಸ್ಥಿತಿಗೆ ಹಿಮ್ಮುಖ ಪರಿವರ್ತನೆಯು ಸಾಧ್ಯ. ಪ್ರಸ್ತುತ, ಅಂತಹ ಹಲವಾರು ಡಜನ್ ವ್ಯವಸ್ಥೆಗಳು ತಿಳಿದಿವೆ.
ಲಿಗಂಡ್ನ σ-ದಾನಿ ಮತ್ತು π-ಸ್ವೀಕರಿಸುವ ಗುಣಲಕ್ಷಣಗಳ ಬಗ್ಗೆ ಮಾತನಾಡುತ್ತಾ, ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳಿಗೆ ಅನ್ವಯಿಸಿದಂತೆ ಆಣ್ವಿಕ ಕಕ್ಷೀಯ ವಿಧಾನದ ವಿಧಾನಗಳನ್ನು ಬಳಸಿಕೊಂಡು ನಾವು TCP ಯನ್ನು ಮೀರಿ ಹೋದೆವು (ಸಂಪುಟ 1). ಡಿ-ಆರ್ಬಿಟಲ್ಗಳ ವಿಭಜನೆಯ ಚಿತ್ರವು ಆಕ್ಟಾಹೆಡ್ರಲ್ ಕಾಂಪ್ಲೆಕ್ಸ್ನಲ್ಲಿನ ಆಣ್ವಿಕ ಕಕ್ಷೆಗಳ ಸಾಮಾನ್ಯ ಯೋಜನೆಯ ಒಂದು ಭಾಗವಾಗಿದೆ, ಅಲ್ಲಿ t 2g ಆರ್ಬಿಟಲ್ಗಳನ್ನು ನಾನ್-ಬಾಂಡಿಂಗ್ ಎಂದು ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ ಮತ್ತು e g - ಆಂಟಿಬಾಂಡಿಂಗ್ (ಚಿತ್ರ. ಸಂಪುಟ 1) .
ಆಕ್ಟಾಹೆಡ್ರಲ್ ಕಾಂಪ್ಲೆಕ್ಸ್ನಲ್ಲಿ π-ಬಂಧವಿಲ್ಲದೆ ಬಂಧಗಳ ರಚನೆಯು ಲೋಹದ s-, p- ಮತ್ತು d-ಕಕ್ಷೆಗಳನ್ನು ಮತ್ತು ಪ್ರತಿ ಲಿಗಂಡ್ನಿಂದ ಒಂದು ಕಕ್ಷೆಯನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ. 15 ಪರಮಾಣು ಕಕ್ಷೆಗಳಿಂದ, 15 ಆಣ್ವಿಕ ಕಕ್ಷೆಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ, ಅವುಗಳಲ್ಲಿ ಆರು (a 1 g, t 1 u, e g (ಅಡಿಟಿಪ್ಪಣಿ: ಕಕ್ಷೆಗಳ ಪದನಾಮದಲ್ಲಿರುವ ಅಕ್ಷರವು ಅವುಗಳ ಅವನತಿಯ ಮಟ್ಟವನ್ನು ಸೂಚಿಸುತ್ತದೆ: t - ಮೂರು ಬಾರಿ ಅವನತಿ, ಇ - ದ್ವಿಗುಣವಾಗಿ ಕ್ಷೀಣಿಸಲು, a - ಕ್ಷೀಣಗೊಳ್ಳದ, ಮತ್ತು ಸಮ್ಮಿತಿಯ ಕೇಂದ್ರದ ಉಪಸ್ಥಿತಿ: g - ಸಮ್ಮಿತೀಯ, u - ಅಸಮಪಾರ್ಶ್ವದ)) σ-ಬಂಧ, ಮೂರು (t 2 g) - ಬಂಧವಲ್ಲದ, ಮತ್ತು ಆರು (e g *, t 1 u *, a 1 g *) σ-ಸಡಿಲಗೊಳಿಸುವಿಕೆ. ಬಾಂಡಿಂಗ್ ಆರ್ಬಿಟಲ್ಗಳು ಶಕ್ತಿಯಲ್ಲಿ ಲಿಗಾಂಡ್ ಕಕ್ಷೆಗಳಿಗೆ ಹತ್ತಿರದಲ್ಲಿವೆ, ಆದರೆ ಬಂಧವಿಲ್ಲದ ಕಕ್ಷೆಗಳು ಪ್ರಧಾನವಾಗಿ ಲೋಹದ ಪರಮಾಣುವಿನ ಮೇಲೆ ಸ್ಥಳೀಕರಿಸಲ್ಪಡುತ್ತವೆ. ಲೋಹದ ಕಕ್ಷೆಗಳ ಶಕ್ತಿ d xy, d xz, d yz (t 2 g) ಸಂಕೀರ್ಣದ ರಚನೆಯ ಸಮಯದಲ್ಲಿ ಪ್ರಾಯೋಗಿಕವಾಗಿ ಬದಲಾಗುವುದಿಲ್ಲ.
ಲಿಗಾಂಡ್ನಲ್ಲಿ ಕಡಿಮೆ-ಶಕ್ತಿಯ ಖಾಲಿ ಕಕ್ಷೆಯ ಉಪಸ್ಥಿತಿಯು, ಲೋಹದ ಕಕ್ಷೆಗಳಿಗೆ ಸಮರೂಪದಲ್ಲಿ, t 2g ಕಕ್ಷೆಗಳ ಶಕ್ತಿಯಲ್ಲಿ ಇಳಿಕೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ, ಪ್ರಾಯೋಗಿಕವಾಗಿ ಪರಿಣಾಮ ಬೀರದೆ ಉದಾ, ಇದರಿಂದಾಗಿ ΔO (Fig. 1.29. MO ತುಣುಕುಗಳು σ-ಡೋನರ್ ಲಿಗಾಂಡ್ (a) ಮತ್ತು σ-ದಾನಿ, π-ಅಕ್ಸೆಪ್ಟರ್ ಲಿಗಾಂಡ್ (b)) ನೊಂದಿಗೆ ಕೋಬಾಲ್ಟ್(III) ಸಂಕೀರ್ಣದ ರೇಖಾಚಿತ್ರ.
ಜಾನ್-ಟೆಲ್ಲರ್ ಪರಿಣಾಮ. 1937 ರಲ್ಲಿ, ಯಾಂಗ್ ಮತ್ತು ಟೆಲ್ಲರ್ ಪ್ರಮೇಯವನ್ನು ಸಾಬೀತುಪಡಿಸಿದರು, ಅದರ ಪ್ರಕಾರ ಕ್ಷೀಣಗೊಂಡ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸ್ಥಿತಿಯಲ್ಲಿ ಯಾವುದೇ ರೇಖಾತ್ಮಕವಲ್ಲದ ಅಣು ಅಸ್ಥಿರವಾಗಿರುತ್ತದೆ ಮತ್ತು ಸ್ವಯಂಪ್ರೇರಿತವಾಗಿ ಅದರ ಸಮ್ಮಿತಿಯನ್ನು ಕಡಿಮೆ ಮಾಡುತ್ತದೆ ಮತ್ತು ಅವನತಿಯನ್ನು ತೆಗೆದುಹಾಕಲು ಕಾರಣವಾಗುತ್ತದೆ. ಪ್ರಮೇಯವು ಅವನತಿಯನ್ನು ತೆಗೆದುಹಾಕುವ ಸತ್ಯವನ್ನು ಮಾತ್ರ ಊಹಿಸುತ್ತದೆ, ಆದರೆ ಅದನ್ನು ಹೇಗೆ ತೆಗೆದುಹಾಕಲಾಗುತ್ತದೆ ಎಂಬುದನ್ನು ಸೂಚಿಸುವುದಿಲ್ಲ. ಈ ಪ್ರಮೇಯದ ಆಧಾರದ ಮೇಲೆ, ಹಲವಾರು ಸಂಕೀರ್ಣಗಳ ಆಕ್ಟಾಹೆಡ್ರಲ್ ಜ್ಯಾಮಿತಿಯ ಅಸ್ಪಷ್ಟತೆಯನ್ನು ವಿವರಿಸಲಾಗಿದೆ, ಮತ್ತು ಅಂತಹ ಅಸ್ಪಷ್ಟತೆಯ ಉಪಸ್ಥಿತಿಯ ಸತ್ಯವನ್ನು ಜಾನ್-ಟೆಲ್ಲರ್ ಪರಿಣಾಮ ಎಂದು ಕರೆಯಲಾಯಿತು. ಒಂದು ಉದಾಹರಣೆಯನ್ನು ನೋಡೋಣ. d9 ಸಂರಚನೆಯೊಂದಿಗೆ ತಾಮ್ರ (II) ಸಂಕೀರ್ಣಗಳು, ನಿಯಮದಂತೆ, ನಿಯಮಿತ ಆಕ್ಟಾಹೆಡ್ರನ್ ಅನ್ನು ಪ್ರತಿನಿಧಿಸುವುದಿಲ್ಲ, ಆದರೆ ಅಕ್ಷಗಳಲ್ಲಿ ಒಂದರ ಉದ್ದಕ್ಕೂ ಉದ್ದವಾದ ಅಥವಾ ಸಂಕುಚಿತಗೊಳಿಸಲಾಗುತ್ತದೆ (ಚಿತ್ರ 1.30. ತಾಮ್ರ (II) ಸಂಕೀರ್ಣಗಳಲ್ಲಿ ಆಕ್ಟಾಹೆಡ್ರಲ್ ಜ್ಯಾಮಿತಿಯ ಅಸ್ಪಷ್ಟತೆ). ಪ್ರೋಲೇಟ್ ಆಕ್ಟಾಹೆಡ್ರನ್ನ ಪ್ರಕರಣವನ್ನು ನಾವು ಪರಿಗಣಿಸೋಣ. z ಅಕ್ಷದ ಉದ್ದಕ್ಕೂ ಇರುವ ಲಿಗಂಡ್ಗಳನ್ನು ತೆಗೆಯುವುದು ಕಕ್ಷೆಗಳ ಶಕ್ತಿಗಳಲ್ಲಿನ ಬದಲಾವಣೆಯಿಂದಾಗಿ ಅವನತಿಯನ್ನು ತೆಗೆದುಹಾಕಲು ಕಾರಣವಾಗುತ್ತದೆ. z ಅಕ್ಷದ ಉದ್ದಕ್ಕೂ ನಿರ್ದೇಶಿಸಲಾದ ಕಕ್ಷೆಗಳು (d xz, d yz, d z 2) z ಘಟಕವನ್ನು ಹೊಂದಿರದ ಕಕ್ಷೆಗಳಿಗೆ ಹೋಲಿಸಿದರೆ ಲಿಗಂಡ್ಗಳ ಕಕ್ಷೆಗಳೊಂದಿಗೆ ದುರ್ಬಲವಾಗಿ ಸಂವಹನ ನಡೆಸುತ್ತವೆ (d xy, d x 2 -y 2), ಮತ್ತು ಆದ್ದರಿಂದ ಅವುಗಳ ಶಕ್ತಿಯನ್ನು ಕಡಿಮೆ ಮಾಡುತ್ತದೆ. z-ಘಟಕ (d xz, d yz) ಹೊಂದಿರುವ ಒಂದೇ ಸಮರೂಪದ ಜೋಡಿ ಕಕ್ಷೆಗಳು ಕ್ಷೀಣಗೊಳ್ಳುತ್ತವೆ ಮತ್ತು ಹೆಚ್ಚಿದ ಶಕ್ತಿಯನ್ನು ಪಡೆದುಕೊಳ್ಳುತ್ತವೆ. (ಚಿತ್ರ 1.31. ಆಕ್ಟಾಹೆಡ್ರಾನ್ ವಿರೂಪಗೊಂಡಾಗ ಡಿ-ಆರ್ಬಿಟಲ್ಗಳ ಶಕ್ತಿಗಳಲ್ಲಿ ಬದಲಾವಣೆ). ಜಾನ್-ಟೆಲ್ಲರ್ ಪರಿಣಾಮವು ಅಸಮಾನವಾಗಿ ತುಂಬಿದ eg ಕಕ್ಷೆಗಳೊಂದಿಗೆ ಸಂಕೀರ್ಣಗಳಲ್ಲಿ ಹೆಚ್ಚು ಬಲವಾಗಿ ಪ್ರಕಟವಾಗುತ್ತದೆ, ಅಂದರೆ, t 2g 3 e g 1 (ದುರ್ಬಲ ಕ್ಷೇತ್ರದಲ್ಲಿ d 4 ಅಯಾನ್ಗೆ ಅನುಗುಣವಾಗಿ: CrCl 2, K 3 MnF 6) ಮತ್ತು t 2g 6 e g 3 ( d 9 ion ಗೆ ಅನುರೂಪವಾಗಿದೆ: ಬಹುತೇಕ ಎಲ್ಲಾ ತಾಮ್ರ (II) ಸಂಕೀರ್ಣಗಳು) ಮತ್ತು t 2g 6 e g 1 (ಬಲವಾದ ಕ್ಷೇತ್ರದಲ್ಲಿ d 7 ಅಯಾನುಗಳಿಗೆ ಅನುರೂಪವಾಗಿದೆ, ಅಪರೂಪದ, K 3 NiF 6), ಅತ್ಯಲ್ಪ ಜಾನ್-ಟೆಲ್ಲರ್ ಪರಿಣಾಮವು ಅಸಮಾನವಾಗಿ ತುಂಬಿದ t 2g ಆರ್ಬಿಟಲ್ಗಳನ್ನು ಹೊಂದಿರುವ ಸಂಕೀರ್ಣಗಳಿಗೆ ವಿಶಿಷ್ಟವಾಗಿದೆ, ಅಂದರೆ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಕಾನ್ಫಿಗರೇಶನ್ಗಳಿಗೆ t 2g 1 (d 1), t 2g 2 (d 2), t 2g 4 (ಬಲವಾದ ಕ್ಷೇತ್ರದಲ್ಲಿ d 4) , t 2g 5 (ಬಲವಾದ ಕ್ಷೇತ್ರದಲ್ಲಿ d 5), t 2g 5 e g 1 (ದುರ್ಬಲ ಕ್ಷೇತ್ರದಲ್ಲಿ d 6), t 2g 5 e g 2 (d 7 ದುರ್ಬಲ ಕ್ಷೇತ್ರದಲ್ಲಿ). ದುರ್ಬಲ ಕ್ಷೇತ್ರದಲ್ಲಿ d 3 ಮತ್ತು d 5 ಸಂರಚನೆಗಳನ್ನು ಹೊಂದಿರುವ ಅಯಾನುಗಳು, ಬಲವಾದ ಕ್ಷೇತ್ರದಲ್ಲಿ d 3 ಮತ್ತು d 6, d 8 ಮತ್ತು d 10 ಯಾವುದೇ ಸಂದರ್ಭಗಳಲ್ಲಿ ಜಾನ್-ಟೆಲ್ಲರ್ ಆಗಿರುವುದಿಲ್ಲ.
ಜಾನ್-ಟೆಲ್ಲರ್ ಪರಿಣಾಮವು ಅನೇಕ ತಾಮ್ರ(II) ಮತ್ತು ಮ್ಯಾಂಗನೀಸ್(III) ಸಂಕೀರ್ಣಗಳಲ್ಲಿನ ಬಂಧದ ಉದ್ದಗಳ ಅಸಮಾನತೆಯಲ್ಲಿ ಮತ್ತು ಸಂಕೀರ್ಣಗಳ ಹಂತ ಹಂತದ ಸ್ಥಿರತೆಯ ಸ್ಥಿರತೆಗಳಲ್ಲಿನ ಏಕರೂಪದ ಬದಲಾವಣೆಯಲ್ಲಿ ಸ್ವತಃ ಸ್ಪಷ್ಟವಾಗಿ ಗೋಚರಿಸುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, ಜಲರಹಿತ ತಾಮ್ರ(II) ಕ್ಲೋರೈಡ್ನಲ್ಲಿ, ತಾಮ್ರದ ಪರಮಾಣು ಆರು ಕ್ಲೋರಿನ್ ಪರಮಾಣುಗಳಿಂದ ಆವೃತವಾಗಿದೆ, ಅವುಗಳಲ್ಲಿ ನಾಲ್ಕು 0.230 nm ದೂರದಲ್ಲಿವೆ ಮತ್ತು ಇತರ ಎರಡು ಅದರಿಂದ 0.295 nm ದೂರದಲ್ಲಿವೆ.
ತಾಮ್ರ(II) ಸಂಕೀರ್ಣಗಳು (Cl 2, (C 6 H 5 SO 3) 2, ಇತ್ಯಾದಿ.) ಹಲವಾರು ಸ್ಫಟಿಕಶಾಸ್ತ್ರೀಯವಾಗಿ ಸಮಾನವಲ್ಲದ ಜಾನ್-ಟೆಲ್ಲರ್ ಅಯಾನುಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತವೆ, ಪ್ರತಿಯೊಂದೂ ತನ್ನದೇ ಆದ ರೀತಿಯ ಅಸ್ಪಷ್ಟತೆಯೊಂದಿಗೆ ಪರಸ್ಪರ ಬದಲಾಗುತ್ತವೆ, ಅವುಗಳು ಬದಲಾಗುತ್ತವೆ. ಮೆಟಲ್-ಲಿಗಾಂಡ್ ದೂರವು ಎಷ್ಟು ವೇಗವಾಗಿರುತ್ತದೆ ಎಂದರೆ ಒಟ್ಟಾರೆ ಎಲ್ಲಾ ಮೆಟಲ್-ಲಿಗಂಡ್ ದೂರಗಳು ಒಂದೇ ಆಗಿರುತ್ತವೆ. ಈ ಪ್ರಕರಣವನ್ನು ಕರೆಯಲಾಯಿತು ಡೈನಾಮಿಕ್ ಅಥವಾ ಪಲ್ಸೇಟಿಂಗ್ ಜಾನ್-ಟೆಲ್ಲರ್ ಪರಿಣಾಮ(P. E. M. Wijnands, J. S. Wood, J. Redijk, W. J. A. Maaskant, Inorg. Chem., 1986, 35, 1214) .
ಆದಾಗ್ಯೂ, ಜಾನ್-ಟೆಲ್ಲರ್ ಪರಿಣಾಮವು ಸಾರ್ವತ್ರಿಕ ಕಾನೂನಲ್ಲ. ಪ್ರಸ್ತುತ, ಜಾನ್-ಟೆಲ್ಲರ್ ಸಂರಚನೆಯೊಂದಿಗೆ ಸಂಕೀರ್ಣ ಅಯಾನುಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ, ಅವುಗಳು ವಿರೂಪಗೊಳ್ಳದ ಆಕ್ಟಾಹೆಡ್ರಾ: 4–, 3+.
ಆಕ್ಟಾಹೆಡ್ರಲ್ ಹೊರತುಪಡಿಸಿ ಸಮ್ಮಿತಿಯೊಂದಿಗೆ ಕ್ಷೇತ್ರಗಳಲ್ಲಿ ವಿಭಜನೆ.
ಅಷ್ಟಮುಖಿಗಳ ಜೊತೆಗೆ, ವಿಭಿನ್ನ ಜ್ಯಾಮಿತಿಯೊಂದಿಗೆ ಅನೇಕ ತಿಳಿದಿರುವ ಸಂಕೀರ್ಣಗಳಿವೆ - ಚದರ-ಸಮತಲ, ಟೆಟ್ರಾಹೆಡ್ರಲ್, ತ್ರಿಕೋನ-ಪಿರಮಿಡ್, ಚದರ-ಪಿರಮಿಡ್, ರೇಖೀಯ, ಇತ್ಯಾದಿ. ಈ ಪ್ರತಿಯೊಂದು ಕ್ಷೇತ್ರಗಳಲ್ಲಿನ ವಿಭಜನೆಯು ಅಷ್ಟಾಹೆಡ್ರನ್ಗಿಂತ ಭಿನ್ನವಾಗಿರುತ್ತದೆ; ಅದು ಸಮನ್ವಯ ಪಾಲಿಹೆಡ್ರನ್ನ ಸಮ್ಮಿತಿಯಿಂದ ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ.
ಸ್ಕ್ವೇರ್-ಪ್ಲ್ಯಾನರ್ ಸಂಕೀರ್ಣಗಳನ್ನು ಆಕ್ಟಾಹೆಡ್ರಲ್ ಜ್ಯಾಮಿತಿಯ ಟೆಟ್ರಾಗೋನಲ್ ಅಸ್ಪಷ್ಟತೆಯ ವಿಪರೀತ ಪ್ರಕರಣವೆಂದು ಪರಿಗಣಿಸಬಹುದು, ನಿರ್ದೇಶಾಂಕದ ಅಕ್ಷಗಳಲ್ಲಿ ಒಂದರ ಉದ್ದಕ್ಕೂ ಇರುವ ಲಿಗಂಡ್ಗಳನ್ನು ಅನಂತತೆಗೆ ತೆಗೆದುಹಾಕಿದಾಗ (Fig. 1.27b). ಕಕ್ಷೆಗಳ ಪದನಾಮಗಳನ್ನು ಚಿತ್ರದಲ್ಲಿ ತೋರಿಸಲಾಗಿದೆ. ಪ್ಲ್ಯಾನರ್-ಸ್ಕ್ವೇರ್ ಸಂಕೀರ್ಣಗಳು ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಕಾನ್ಫಿಗರೇಶನ್ d 8 - Ni 2+, Pd 2+, Pt 2+, Au 3+ ನೊಂದಿಗೆ ಅಯಾನುಗಳಿಗೆ ಹೆಚ್ಚು ವಿಶಿಷ್ಟವಾಗಿದೆ. ಹೆಚ್ಚುತ್ತಿರುವ Δ ನೊಂದಿಗೆ ಅವುಗಳ ಸ್ಥಿರತೆಯು ತೀವ್ರವಾಗಿ ಹೆಚ್ಚಾಗುತ್ತದೆ, ಅಂದರೆ, 3d ಸರಣಿಯ ಅಂಶಗಳಿಂದ ಭಾರೀ ಪರಿವರ್ತನೆಯ ಅಂಶಗಳಿಗೆ ಚಲಿಸುವಾಗ. ಆದ್ದರಿಂದ, ಉದಾಹರಣೆಗೆ, ಪಲ್ಲಾಡಿಯಮ್, ಪ್ಲಾಟಿನಂ ಮತ್ತು ಚಿನ್ನವು ನಾಲ್ಕು ಚೌಕಗಳ ಸಮನ್ವಯ ಸಂಖ್ಯೆಯೊಂದಿಗೆ ಬಹುತೇಕ ಎಲ್ಲಾ ಸಂಕೀರ್ಣಗಳನ್ನು ಹೊಂದಿದ್ದರೆ, ನಂತರ ನಿಕಲ್ ಉನ್ನತ-ಕ್ಷೇತ್ರದ ಲಿಗಂಡ್ಗಳೊಂದಿಗೆ ಮಾತ್ರ ಸಮತಲ-ಚದರ ಸಂಕೀರ್ಣಗಳನ್ನು ರೂಪಿಸುತ್ತದೆ: 2–, Ni (dmg) 2. ಹ್ಯಾಲೊಜೆನ್ಗಳಂತಹ ಕಡಿಮೆ-ಕ್ಷೇತ್ರದ ಲಿಗಂಡ್ಗಳನ್ನು ಹೊಂದಿರುವ ನಿಕಲ್(II) ಸಂಕೀರ್ಣಗಳು ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಜ್ಯಾಮಿತಿಯನ್ನು ಹೊಂದಿವೆ.
ಕೆಲವು ಚದರ-ಪ್ಲಾನರ್ ಪರಿವರ್ತನೆಯ ಲೋಹದ ಸಂಕೀರ್ಣಗಳು ಬ್ರಿಡ್ಜಿಂಗ್ ಲಿಗಂಡ್ಗಳೊಂದಿಗೆ ಘನ ರೂಪದಲ್ಲಿ ಸರಪಳಿಗಳನ್ನು ರೂಪಿಸುತ್ತವೆ, ಉದಾಹರಣೆಗೆ K 2 Br 0.3 ರಲ್ಲಿ Pt-CN-Pt, ಅಲ್ಲಿ ಪ್ಲಾಟಿನಂ ಪರಮಾಣುಗಳು ಭಾಗಶಃ +4 ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿಯಲ್ಲಿರುತ್ತವೆ. 5d ಕಕ್ಷೆಗಳ ಹೆಚ್ಚಿನ ನುಗ್ಗುವ ಸಾಮರ್ಥ್ಯವು ಒಂದೇ ಶಕ್ತಿಯ ಬ್ಯಾಂಡ್ನ ರಚನೆಯೊಂದಿಗೆ ಅವುಗಳ ಅತಿಕ್ರಮಣವನ್ನು ಖಾತ್ರಿಗೊಳಿಸುತ್ತದೆ ಮತ್ತು ಪರಿಣಾಮವಾಗಿ, ಸರಪಳಿಯ ದಿಕ್ಕಿನಲ್ಲಿ ಲೋಹೀಯ ವಾಹಕತೆ. ಅಂತಹ ಆಣ್ವಿಕ ಸಂಕೀರ್ಣಗಳು ವಿದ್ಯುತ್ ಪ್ರವಾಹವನ್ನು ನಡೆಸುವ ಸಾಮರ್ಥ್ಯವನ್ನು ಹೊಂದಿವೆ ಮತ್ತು ಪ್ರಸ್ತುತ ತೀವ್ರವಾಗಿ ಅಧ್ಯಯನ ಮಾಡಲಾಗುತ್ತಿದೆ.
ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಸಮ್ಮಿತಿಯ ಕ್ಷೇತ್ರದಲ್ಲಿ, ಕಕ್ಷೆಗಳು d xy, d yz, d xz ಗರಿಷ್ಠ ಶಕ್ತಿಯನ್ನು ಹೊಂದಿರುತ್ತವೆ, ಅವುಗಳನ್ನು t 2-ಕಕ್ಷೆಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ, ಮತ್ತು ಕನಿಷ್ಠ ಶಕ್ತಿಯು ಕಕ್ಷೆಗಳು d x 2 –y 2 ಮತ್ತು d z 2 ಆಗಿದೆ, ಅವುಗಳನ್ನು e ಎಂದು ಸೂಚಿಸಲಾಗುತ್ತದೆ. . ಕಡಿಮೆ ಸಂಖ್ಯೆಯ ಲಿಗಂಡ್ಗಳ ಉಪಸ್ಥಿತಿ ಮತ್ತು ಅವುಗಳ ವಿಭಿನ್ನ ವ್ಯವಸ್ಥೆಯಿಂದಾಗಿ, ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಕ್ಷೇತ್ರ (ಚಿತ್ರ 1.32. ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಮತ್ತು ಆಕ್ಟಾಹೆಡ್ರಲ್ ಕ್ಷೇತ್ರಗಳಲ್ಲಿನ ವಿಭಜನೆಗಳ ಹೋಲಿಕೆ) ಆಕ್ಟಾಹೆಡ್ರಲ್ ಒಂದಕ್ಕಿಂತ 2.25 ಪಟ್ಟು ದುರ್ಬಲವಾಗಿರುತ್ತದೆ: .
ಹೆಚ್ಚಿನ ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳು ಹೈ-ಸ್ಪಿನ್ ಆಗಿರುತ್ತವೆ (ಅಡಿಟಿಪ್ಪಣಿ - ಕಡಿಮೆ-ಸ್ಪಿನ್ ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳ ಹಲವಾರು ಉದಾಹರಣೆಗಳು ತಿಳಿದಿವೆ, ಉದಾಹರಣೆಗೆ, Cr(N(Si(CH 3) 3) 2 ) 3 NO (ಕ್ರೋಮಿಯಂ(II), d 4 ; D. C. ಬ್ರಾಡ್ಲಿ, ಕೆಮ್. ಬರ್., 1979 , 11, 393); CoL 4, ಅಲ್ಲಿ L 1-ನಾರ್ಬೋರ್ನಿಲ್ (ಕೋಬಾಲ್ಟ್(IV), d 5; E. K: ಬ್ರೂನ್, D. S. ರಿಚೆಸನ್, K. H. ಥಿಯೋಪೋಲ್ಡ್, ಕೆಮ್. ಕಮ್ಯೂನ್., 1986 , 1491)). ಸ್ಫಟಿಕದಂತಹ ಕ್ಷೇತ್ರದಿಂದ ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಪರಿಸರದ ಗರಿಷ್ಠ ಸ್ಥಿರೀಕರಣವನ್ನು d 2 (FeO 4 2–, MnO 4 3–) ಮತ್ತು d 7 (2–) ಸಂರಚನೆಗಳೊಂದಿಗೆ ಸಾಧಿಸಲಾಗುತ್ತದೆ. ತುಲನಾತ್ಮಕವಾಗಿ ಕಡಿಮೆ ಸ್ಥಿರೀಕರಣ ಶಕ್ತಿಯಿಂದಾಗಿ, ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳು ಹೆಚ್ಚಾಗಿ ಸಂರಚನೆಗಳೊಂದಿಗೆ ಅಯಾನುಗಳಿಂದ ರೂಪುಗೊಳ್ಳುತ್ತವೆ d 0 (TiCl 4, MnO 4 –, CrO 4 2–), d 5 ದುರ್ಬಲ ಕ್ಷೇತ್ರದಲ್ಲಿ (FeCl 4 –) ಮತ್ತು d 10 (ZnCl 4 2–) ಶೂನ್ಯ ESKP ಜೊತೆಗೆ, ಹಾಗೆಯೇ ಪರಿವರ್ತನೆಯಲ್ಲದ ಲೋಹದ ಅಯಾನುಗಳು (AlCl 4 -). ಆಕ್ಟಾಹೆಡ್ರಲ್ ಪದಗಳಿಗಿಂತ ಹೋಲಿಸಿದರೆ ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳ ರಚನೆಯು ಹೆಚ್ಚಾಗಿ ಸ್ಟೆರಿಕ್ ಅಂಶದಿಂದ ಒಲವು ತೋರುತ್ತದೆ, ಉದಾಹರಣೆಗೆ, ಅಯಾನು 3- ಗಿಂತ ಹೆಚ್ಚು ಸ್ಥಿರವಾಗಿರುತ್ತದೆ.
ಸಂಕೀರ್ಣಗಳ ಸ್ಥಿರತೆಯನ್ನು ವಿವರಿಸಲು TCP ಅನ್ನು ಬಳಸುವುದು. ಇರ್ವಿಂಗ್-ವಿಲಿಯಮ್ಸ್ ಸರಣಿ.ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರ ಸಿದ್ಧಾಂತವು ಆಕ್ಸೈಡ್ಗಳು ಮತ್ತು ಹಾಲೈಡ್ಗಳ ಸ್ಫಟಿಕ ಜಾಲರಿಯ ಶಕ್ತಿಗಳಲ್ಲಿನ ಬದಲಾವಣೆಗಳ ಏಕತಾನತೆಯಲ್ಲದ ಸ್ವರೂಪವನ್ನು ವಿವರಿಸಲು ಸಾಧ್ಯವಾಗಿಸುತ್ತದೆ, ಸಂಕೀರ್ಣಗಳ ಸ್ಥಿರತೆ ಸ್ಥಿರತೆಗಳು ಇತ್ಯಾದಿ. 3d ಲೋಹಗಳ ದ್ವಿಗುಣವಾಗಿ ಚಾರ್ಜ್ಡ್ ಕ್ಯಾಟಯಾನುಗಳ ಜಲಸಂಚಯನ ಶಕ್ತಿಗಳಲ್ಲಿನ ಬದಲಾವಣೆಯ ಕ್ರಮ ಸಾಮಾನ್ಯವಾಗಿ ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳಲ್ಲಿ ESC ಯಲ್ಲಿನ ಬದಲಾವಣೆಗಳ ಸ್ವರೂಪದೊಂದಿಗೆ ಹೊಂದಿಕೆಯಾಗುತ್ತದೆ (Fig. 1.33. 3d ಸರಣಿಯ (a) ದ್ವಿಗುಣವಾಗಿ ಚಾರ್ಜ್ ಮಾಡಲಾದ ಕ್ಯಾಟಯಾನ್ಸ್ ಲೋಹಗಳ ಜಲಸಂಚಯನ ಶಕ್ತಿಯ ಬದಲಾವಣೆ ಮತ್ತು ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳಲ್ಲಿ ESC ಬದಲಾವಣೆ (b) ), ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದಿಂದ ಬಲವಾದ ಸ್ಥಿರೀಕರಣ, ಹೆಚ್ಚಿನ ಜಲಸಂಚಯನ. ದುರ್ಬಲ-ಕ್ಷೇತ್ರದ ಲಿಗಂಡ್ L ನಿಂದ ನೀರಿನ ಅಣುವಿನ ಪರ್ಯಾಯದ ಸ್ಥಿರಾಂಕಗಳು ಎಂದು ತಿಳಿದಿದೆ
2+ + L x– = (2-x)+ + H 2 O
ಇರ್ವಿಂಗ್-ವಿಲಿಯಮ್ಸ್ ಸರಣಿಯನ್ನು ಅನುಸರಿಸಿ: Mn 2+< Fe 2+ < Co 2+ < Ni 2+ < Cu 2+ < Zn 2+ (Рис. 1.34. Зависимость первой константы устойчивости комплекса от природы 3d-металла). Согласно этому ряду, наибольшей устойчивостью обладают комплексы меди(II) и никеля(II). Простейший вариант ЭСКП предсказывает наибольшую устойчивость никелевых комплексов. При этом надо учитывать, что комплексы меди(II) имеют сильно искаженную октаэдрическую геометрию, что вносит существенный вклад в величину константы устойчивости.
ನೆಫೆಲೋಕ್ಸೆಟಿಕ್ ಪರಿಣಾಮ.ಪರಮಾಣುವನ್ನು ಲಿಗಂಡ್ಗಳ ಕ್ಷೇತ್ರದಲ್ಲಿ ಇರಿಸಿದಾಗ ಡಿ-ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಪರಸ್ಪರ ವಿಕರ್ಷಣೆ ದುರ್ಬಲಗೊಳ್ಳುತ್ತದೆ ಎಂದು ಕಂಡುಹಿಡಿಯಲಾಯಿತು. ಲೋಹದ ಪರಮಾಣುವಿನ ಡಿ-ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಮೇಲೆ ಲಿಗಂಡ್ನ ಈ ಪರಿಣಾಮವನ್ನು ಗ್ರೀಕ್ ಪದಗಳಾದ νεφελη - ಕ್ಲೌಡ್ ಮತ್ತು αυξανω - ಹೆಚ್ಚಳದಿಂದ ನೆಫೆಲೋಕ್ಸೆಟಿಕ್ ಪರಿಣಾಮ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಲೋಹದ ಕಕ್ಷೆಗಳ ಮೇಲೆ ತಮ್ಮ ಪ್ರಭಾವವನ್ನು ಹೆಚ್ಚಿಸುವ ಸಲುವಾಗಿ ಜೋಡಿಸಲಾದ ಲಿಗಂಡ್ಗಳ ಸರಣಿಯು ರೋಹಿತ ರಾಸಾಯನಿಕ ಸರಣಿಗೆ ಸಂಪೂರ್ಣವಾಗಿ ಅನುರೂಪವಾಗಿದೆ. ನೆಫೆಲೋಕ್ಸೆಟಿಕ್ ಪರಿಣಾಮಕ್ಕೆ ಕಾರಣವೆಂದರೆ ಲಿಗಂಡ್ಗಳ ಕಕ್ಷೆಗಳೊಂದಿಗೆ ಲೋಹದ ಡಿ-ಆರ್ಬಿಟಲ್ಗಳ ಅತಿಕ್ರಮಣ, ಈ ಕಾರಣದಿಂದಾಗಿ ಡಿ-ಕ್ಲೌಡ್ ಬಾಹ್ಯಾಕಾಶದಲ್ಲಿ ವಿಸ್ತರಿಸುತ್ತದೆ. ಈ ಪರಿಣಾಮದ ಉಪಸ್ಥಿತಿಯು ಸರಳವಾದ ಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ ಮಾದರಿಯ ಮಿತಿಗಳನ್ನು ಸ್ಪಷ್ಟವಾಗಿ ತೋರಿಸುತ್ತದೆ - ಸ್ಫಟಿಕದಂತಹ ಕ್ಷೇತ್ರ ಸಿದ್ಧಾಂತ, ಇದು ಲಿಗ್ನೇಡ್ಗಳು ಪಾಯಿಂಟ್ ಋಣಾತ್ಮಕ ಶುಲ್ಕಗಳು ಎಂದು ಊಹಿಸುತ್ತದೆ.
ಲಿಗಾಂಡ್ ಕ್ಷೇತ್ರ ಸಿದ್ಧಾಂತ.ಕ್ರಿಸ್ಟಲ್ ಫೀಲ್ಡ್ ಸಿದ್ಧಾಂತವನ್ನು 1929 ರಲ್ಲಿ ಬೆಥೆ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದರು. ಪ್ರಸ್ತುತ, ಲೋಹದ-ಲಿಗಂಡ್ ಬಂಧದ ಕೆಲವು ಕೋವೆಲೆನ್ಸಿಗೆ ತಿದ್ದುಪಡಿಗಳೊಂದಿಗೆ ಮಾರ್ಪಡಿಸಿದ ರೂಪದಲ್ಲಿ ಇದನ್ನು ವ್ಯಾಪಕವಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ. ಈ ಸಿದ್ಧಾಂತವನ್ನು ಲಿಗಾಂಡ್ ಫೀಲ್ಡ್ ಸಿದ್ಧಾಂತ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಕೋವೆಲನ್ಸಿಯ ಕೊಡುಗೆಯ ಉಪಸ್ಥಿತಿಯು TCP ಯಿಂದ ಲೆಕ್ಕಾಚಾರ ಮಾಡಲಾದ ಹೋಲಿಸಿದರೆ ಲೋಹದ ಕಕ್ಷೆಗಳ ಶಕ್ತಿಯನ್ನು ಬದಲಾಯಿಸುತ್ತದೆ. ಪ್ರಾಯೋಗಿಕ ಮೌಲ್ಯಗಳನ್ನು ಲೆಕ್ಕ ಹಾಕಿದ ಮೌಲ್ಯಗಳೊಂದಿಗೆ ಸಮೀಕರಿಸಲು ಸಾಧ್ಯವಾಗುವಂತೆ ತಿದ್ದುಪಡಿ ಅಂಶಗಳನ್ನು ಪರಿಚಯಿಸುವ ಮೂಲಕ ಕೋವೆಲೆನ್ಸಿಯ ಅನುಪಾತವನ್ನು ಗಣನೆಗೆ ತೆಗೆದುಕೊಳ್ಳಲಾಗುತ್ತದೆ.
ಸಂಕೀರ್ಣಗಳ ಬಣ್ಣ.
ಡಿ-ಟ್ರಾನ್ಸಿಶನ್ ಎಲಿಮೆಂಟ್ ಕಾಂಪ್ಲೆಕ್ಸ್ಗಳ ಬಣ್ಣವು ಒಂದು ಡಿ-ಆರ್ಬಿಟಲ್ನಿಂದ ಇನ್ನೊಂದಕ್ಕೆ ಎಲೆಕ್ಟ್ರಾನ್ ಪರಿವರ್ತನೆಗಳೊಂದಿಗೆ ಸಂಬಂಧಿಸಿದೆ. ಪಠ್ಯಪುಸ್ತಕದ ಮೊದಲ ಸಂಪುಟದಲ್ಲಿ ಚರ್ಚಿಸಲಾದ Ti 3+ ಐಯಾನ್ನ ಉದಾಹರಣೆಯಿಂದ ಇದನ್ನು ಸ್ಪಷ್ಟವಾಗಿ ವಿವರಿಸಲಾಗಿದೆ. ಗೋಚರ ವರ್ಣಪಟಲದ ನೀಲಿ ಮತ್ತು ಹಸಿರು ಭಾಗಗಳಿಗೆ ಅನುಗುಣವಾದ ಶಕ್ತಿಯನ್ನು ಹೀರಿಕೊಳ್ಳುವ ಮೂಲಕ, Ti 3+ ಅಯಾನುಗಳಲ್ಲಿರುವ ಏಕೈಕ d-ಎಲೆಕ್ಟ್ರಾನ್ e g ಕಕ್ಷೆಗೆ ಚಲಿಸುತ್ತದೆ (Fig. 1.35. 3+ ಅಯಾನಿನ ಸ್ಪೆಕ್ಟ್ರಮ್). ಅಯಾನಿನ ಬಣ್ಣವು ಹೆಚ್ಚುವರಿ ಬಣ್ಣಗಳಿಂದಾಗಿರುತ್ತದೆ - ಕೆಂಪು ಮತ್ತು ನೇರಳೆ. (ಅಡಿಟಿಪ್ಪಣಿ - ಗಮನಿಸುವ ಓದುಗರು ಹೀರಿಕೊಳ್ಳುವ ಬ್ಯಾಂಡ್ನ ಕೆಲವು ಅಸಿಮ್ಮೆಟ್ರಿಯನ್ನು ಗಮನಿಸುತ್ತಾರೆ. ಇದು ಜಾನ್-ಟೆಲ್ಲರ್ ಪರಿಣಾಮದಿಂದ ಉಂಟಾದ t 2g ಮಟ್ಟದ ಸ್ವಲ್ಪ ವಿಭಜನೆಯ ಪರಿಣಾಮವಾಗಿದೆ). ಪೂರಕ ಬಣ್ಣಗಳನ್ನು ತೋರಿಸುವ ಮತ್ತು ಪ್ರತಿಯೊಬ್ಬ ಕಲಾವಿದರಿಗೂ ತಿಳಿದಿರುವ ರೇಖಾಚಿತ್ರವನ್ನು ಪಠ್ಯಪುಸ್ತಕದ ಎರಡನೇ ಫ್ಲೈಲೀಫ್ನಲ್ಲಿ ಪ್ರಸ್ತುತಪಡಿಸಲಾಗಿದೆ. ಸಂಕ್ರಮಣ ಶಕ್ತಿ, ಪರಸ್ಪರ ಸೆಂಟಿಮೀಟರ್ಗಳಲ್ಲಿ (1000 cm –1 = 12 kJ) ವ್ಯಕ್ತಪಡಿಸಲಾಗುತ್ತದೆ, ವಿಭಜಿಸುವ ನಿಯತಾಂಕ Δο ಗೆ ಅನುರೂಪವಾಗಿದೆ - ಇದನ್ನು ಹೆಚ್ಚಾಗಿ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸ್ಪೆಕ್ಟ್ರಾದಿಂದ ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ. ತರಂಗಾಂತರವು ಶಕ್ತಿಗೆ ವಿಲೋಮ ಅನುಪಾತದಲ್ಲಿರುತ್ತದೆ:
 .
.
ಹೆಚ್ಚಿನ ಸಂಖ್ಯೆಯ ಎಲೆಕ್ಟ್ರಾನ್ಗಳೊಂದಿಗೆ ಸಂಕೀರ್ಣಗಳ ಸಂದರ್ಭದಲ್ಲಿ, ಸ್ಪೆಕ್ಟ್ರಮ್ ಚಿತ್ರವು ಹೆಚ್ಚು ಜಟಿಲವಾಗಿದೆ, ಮತ್ತು ಹೆಚ್ಚುವರಿ ಬ್ಯಾಂಡ್ಗಳು ಅದರಲ್ಲಿ ಕಾಣಿಸಿಕೊಳ್ಳುತ್ತವೆ. ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಯಾವ ಎರಡು ಡಿ-ಆರ್ಬಿಟಲ್ಗಳಲ್ಲಿವೆ ಎಂಬುದರ ಆಧಾರದ ಮೇಲೆ ಉತ್ತೇಜಿತ ಸ್ಥಿತಿ t 2g 1 e g 1 ಅನ್ನು ಹಲವಾರು ರೀತಿಯಲ್ಲಿ ಅರಿತುಕೊಳ್ಳಬಹುದು ಎಂಬುದು ಇದಕ್ಕೆ ಕಾರಣ. ಉದಾಹರಣೆಗೆ, ಎಲೆಕ್ಟ್ರಾನ್ಗಳು d xy ಮತ್ತು d x 2 –y 2 ಕಕ್ಷೆಗಳನ್ನು ಆಕ್ರಮಿಸುವ ಸ್ಥಿತಿಯು x ಅಕ್ಷದ ಉದ್ದಕ್ಕೂ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಹೆಚ್ಚಿನ ವಿಕರ್ಷಣೆಯಿಂದಾಗಿ d xy 1 d z 2 1 ಸ್ಥಿತಿಗಿಂತ ಹೆಚ್ಚಿನ ಶಕ್ತಿಯಾಗಿರುತ್ತದೆ. ಕಡಿಮೆ ಶಕ್ತಿಯೊಂದಿಗೆ ಬ್ಯಾಂಡ್ಗೆ ಅನುಗುಣವಾದ ಶಕ್ತಿಯು ವಿಭಜಿಸುವ ಪ್ಯಾರಾಮೀಟರ್ Δo ಗೆ ಸಮಾನವಾಗಿರುತ್ತದೆ.
ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸ್ಪೆಕ್ಟ್ರಾವನ್ನು ಹೆಚ್ಚು ವಿವರವಾಗಿ ವಿವರಿಸಲು, ಕೆಲವು ಪರಿಕಲ್ಪನೆಗಳನ್ನು ಪರಿಚಯಿಸುವುದು ಅವಶ್ಯಕ. ಉಪಮಟ್ಟದಲ್ಲಿರುವ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಯಾವುದೇ ಜೋಡಣೆಯನ್ನು ಮೈಕ್ರೋಸ್ಟೇಟ್ ಎಂದು ಕರೆಯೋಣ. ಮೈಕ್ರೊಸ್ಟೇಟ್ಗಳ ಸಂಖ್ಯೆ N, ಇದರಲ್ಲಿ n ಎಲೆಕ್ಟ್ರಾನ್ಗಳು x ಆರ್ಬಿಟಲ್ಗಳನ್ನು ಆಕ್ರಮಿಸುತ್ತವೆ, ಇದು ಸಮಾನವಾಗಿರುತ್ತದೆ

ಪ್ರತಿಯೊಂದು ಮೈಕ್ರೋಸ್ಟೇಟ್ ತನ್ನದೇ ಆದ ಸ್ಪಿನ್ ಮತ್ತು ಕೋನೀಯ ಆವೇಗದ ಮೌಲ್ಯಗಳಿಂದ ನಿರೂಪಿಸಲ್ಪಟ್ಟಿದೆ. ಒಂದೇ ರೀತಿಯ ಶಕ್ತಿಯೊಂದಿಗೆ ಮೈಕ್ರೊಸ್ಟೇಟ್ಗಳ ಗುಂಪನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ಅವಧಿ, ಉದಾಹರಣೆಗೆ, 3 P, 5 D, 1 S. ಡಿಜಿಟಲ್ ಸೂಚ್ಯಂಕವು ಬಹುತ್ವವನ್ನು ಸೂಚಿಸುತ್ತದೆ, ಇದನ್ನು ಹೀಗೆ ಲೆಕ್ಕಹಾಕಲಾಗುತ್ತದೆ:
ಗುಣಾಕಾರ = ನೆಲದ ಸ್ಥಿತಿಯಲ್ಲಿ ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆ + 1.
ಪದಗಳ ಹೆಸರುಗಳನ್ನು ಬಹುಸಂಖ್ಯೆಯ ಸೂಚನೆಯೊಂದಿಗೆ ಓದಲಾಗುತ್ತದೆ: "ಟ್ರಿಪಲ್ ಪಿ", "ಕ್ವಿಂಟೆಟ್ ಡಿ", "ಸಿಂಗಲ್ ಎಸ್". ಅಕ್ಷರವು ಪರಮಾಣು ಅಥವಾ ಅಯಾನಿನ ಒಟ್ಟು ಕೋನೀಯ ಆವೇಗ L ಅನ್ನು ಸೂಚಿಸುತ್ತದೆ, ಇದು ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಆಕ್ರಮಿಸಿಕೊಂಡಿರುವ ಪ್ರತ್ಯೇಕ ಕಕ್ಷೆಗಳ ಕೋನೀಯ ಮೊಮೆಂಟ m l ಮೊತ್ತದ ಗರಿಷ್ಠ ಮೌಲ್ಯಕ್ಕೆ ಸಮಾನವಾಗಿರುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, Ti 3+ ಅಯಾನು ಒಂದು d-ಎಲೆಕ್ಟ್ರಾನ್ ಅನ್ನು ಹೊಂದಿರುತ್ತದೆ, ಮೈಕ್ರೋಸ್ಟೇಟ್ಗಳ ಸಂಖ್ಯೆ N = (2´5)!/1!(2´5 - 1)! = 10, L = 2(D) (d-ಆರ್ಬಿಟಲ್ m l = –2, –1, 0, 1, 2, ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆ 1 ಆಗಿರುವುದರಿಂದ, ಗರಿಷ್ಠ ಮೊತ್ತ m l ಇದರ ದೊಡ್ಡ ಮೌಲ್ಯಕ್ಕೆ ಸಮಾನವಾಗಿರುತ್ತದೆ m l), ಗುಣಾಕಾರ 1 + 1 = 2. ಆದ್ದರಿಂದ, ನೆಲದ ಸ್ಥಿತಿಯ ಪದವು (ಕಡಿಮೆ ಶಕ್ತಿಯೊಂದಿಗೆ) 2 D. ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸಂರಚನೆಯೊಂದಿಗೆ ಅಯಾನಿನ ಸಂದರ್ಭದಲ್ಲಿ d 2 N = (2´5)!/2!( 2'5 - 2)! = 45, L = 3(F) (ಡಿ-ಆರ್ಬಿಟಲ್ m l = –2, –1, 0, 1, 2, ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆ 2 ಆಗಿರುವುದರಿಂದ, ಎರಡು ದೊಡ್ಡ ಮೌಲ್ಯಗಳ ಗರಿಷ್ಠ ಮೊತ್ತ m l ಗೆ ಸಮಾನವಾಗಿರುತ್ತದೆ), ಗುಣಾಕಾರ 2 + 1 = 3. ಪರಿಣಾಮವಾಗಿ, ನೆಲದ ಮೈಕ್ರೊಸ್ಟೇಟ್ನ ಪದವು 3 ಎಫ್ ಆಗಿದೆ. ಡಿ-ಸಬ್ಲೆವೆಲ್ನಲ್ಲಿ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿಭಿನ್ನ ಜೋಡಣೆಯೊಂದಿಗೆ, ಇತರ ಪದಗಳಿಂದ ವಿವರಿಸಲಾದ ಸ್ಥಿತಿಗಳನ್ನು ಸಾಧಿಸಲಾಗುತ್ತದೆ - 3 ಪಿ, 1 ಜಿ , 1 ಡಿ, 1 ಎಸ್, ಇತ್ಯಾದಿ. L ನ ಸಂಖ್ಯಾತ್ಮಕ ಮೌಲ್ಯಗಳು ಮತ್ತು ವರ್ಣಮಾಲೆಯ ಚಿಹ್ನೆಗಳ ನಡುವಿನ ಸಂಬಂಧವನ್ನು ಕೆಳಗೆ ನೀಡಲಾಗಿದೆ:
L = 0 1 2 3 4 5 6 7
ಅಂತೆಯೇ, ಡಿ-ಎಲಿಮೆಂಟ್ಗಳ ಇತರ ಅಯಾನುಗಳಿಗೆ ನಾವು ನೆಲದ ಮತ್ತು ಉತ್ಸುಕ ಸ್ಥಿತಿಗಳ ಪದಗಳನ್ನು ಪಡೆಯಬಹುದು (ಕೋಷ್ಟಕ 1.5.). d n ಮತ್ತು d 10-n ಸಂರಚನೆಯೊಂದಿಗೆ ಅಯಾನುಗಳ ನಿಯಮಗಳು ಒಂದೇ ಆಗಿರುತ್ತವೆ ಎಂಬುದನ್ನು ದಯವಿಟ್ಟು ಗಮನಿಸಿ.
ಟೇಬಲ್. 1.5
ಡಿ-ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿವಿಧ ಸಂರಚನೆಗಳಿಗಾಗಿ ನೆಲದ ನಿಯಮಗಳು ಮತ್ತು ಹತ್ತಿರದ ಉತ್ಸುಕ ಸ್ಥಿತಿಗಳು.
ಪದಗಳನ್ನು ಕಕ್ಷೆಗಳಂತೆ ಅಷ್ಟಹೆಡ್ರಲ್ ಕ್ಷೇತ್ರದಲ್ಲಿ ವಿಭಜಿಸಲಾಗಿದೆ, ಒಂದೇ ರೀತಿಯ ಅಕ್ಷರಗಳಿಂದ ಸೂಚಿಸಲಾಗುತ್ತದೆ. D ಪದಗಳನ್ನು d-ಆರ್ಬಿಟಲ್ಗಳಂತಹ T 2 g ಮತ್ತು E g ಘಟಕಗಳಾಗಿ ವಿಭಜಿಸಲಾಗಿದೆ, F ಪದಗಳು - T 1 g, T 2 g ಮತ್ತು A 2 g, ಎಫ್-ಆರ್ಬಿಟಲ್ಗಳಂತೆ. S ಮತ್ತು P ನಿಯಮಗಳು ವಿಭಜನೆಯಾಗಿಲ್ಲ. ವಿವಿಧ ರಾಜ್ಯಗಳ ನಡುವೆ ಎಲೆಕ್ಟ್ರಾನ್ ಪರಿವರ್ತನೆಯ ಸಾಧ್ಯತೆಗಳು ಆಯ್ಕೆ ನಿಯಮಗಳಿಂದ ಸೀಮಿತವಾಗಿವೆ. ಹೀಗಾಗಿ, ಸಂಕೀರ್ಣಗಳಲ್ಲಿ ಒಂದೇ ಬಹುಸಂಖ್ಯೆಯೊಂದಿಗೆ ರಾಜ್ಯಗಳ ನಡುವಿನ ಪರಿವರ್ತನೆಗಳನ್ನು ಮಾತ್ರ ಅನುಮತಿಸಲಾಗುತ್ತದೆ. ಅಂತಹ ಪ್ರತಿಯೊಂದು ಪರಿವರ್ತನೆಯು ಹೀರಿಕೊಳ್ಳುವ ವರ್ಣಪಟಲದಲ್ಲಿನ ಬ್ಯಾಂಡ್ಗೆ ಅನುರೂಪವಾಗಿದೆ. ಉದಾಹರಣೆಯಾಗಿ, ಸಂಕೀರ್ಣ 3+ ನ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸ್ಪೆಕ್ಟ್ರಮ್ ಅನ್ನು ಪರಿಗಣಿಸಿ (Fig. 1.36. ಸಂಕೀರ್ಣ 3+ ನ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸ್ಪೆಕ್ಟ್ರಮ್). ಮೂರು ಬ್ಯಾಂಡ್ಗಳು ಮೂರು ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಪರಿವರ್ತನೆಗಳ ಕಾರಣದಿಂದಾಗಿವೆ: 4 A 2 g ® 4 T 2 g, 4 A 2 g ® 4 T 1 g, 4 A 2 g ® 4 T 1 g (P). ಕಡಿಮೆ ಶಕ್ತಿಯೊಂದಿಗೆ ಪರಿವರ್ತನೆಯು ವಿಭಜಿಸುವ ನಿಯತಾಂಕದ ಮೌಲ್ಯಕ್ಕೆ ಅನುರೂಪವಾಗಿದೆ: Δo = 17400 cm-1. ಸಂಕೀರ್ಣವು ಕೆಂಪು (17400 cm-1) ಮತ್ತು ನೀಲಿ (23000 cm-1) ಗೋಚರ ವರ್ಣಪಟಲದ ಭಾಗಗಳಲ್ಲಿ ಮತ್ತು ಹತ್ತಿರದ ನೇರಳಾತೀತ (37800 cm-1) ನಲ್ಲಿ ಬೆಳಕನ್ನು ಹೀರಿಕೊಳ್ಳುತ್ತದೆ, ಆದ್ದರಿಂದ, ಇದು ನೇರಳೆ ಬಣ್ಣವನ್ನು ಹೊಂದಿರುತ್ತದೆ.
ಲ್ಯಾಪೋರ್ಟೆಯ ನಿಯಮದ ಪ್ರಕಾರ, s-s, p-p, d-d, f-f ಪರಿವರ್ತನೆಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ಒಂದೇ ಸಮಾನತೆಯೊಂದಿಗೆ ರಾಜ್ಯಗಳ ನಡುವಿನ ಪರಿವರ್ತನೆಗಳು ಅಸಂಭವವಾಗಿದೆ, ಅಥವಾ, ಸ್ಪೆಕ್ಟ್ರೋಸ್ಕೋಪಿ ಭಾಷೆಯಲ್ಲಿ, ಅಕ್ಟಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳಲ್ಲಿ ಅವುಗಳನ್ನು ನಿಷೇಧಿಸಲಾಗಿದೆ. ನಿಷೇಧಿತ ಪರಿವರ್ತನೆಗಳು ಸಾಧ್ಯ, ಆದರೆ ಕಡಿಮೆ ತೀವ್ರತೆಯೊಂದಿಗೆ ಸಂಭವಿಸುತ್ತವೆ. ಅದಕ್ಕಾಗಿಯೇ ಪರಿವರ್ತನೆಯ ಲೋಹದ ಲವಣಗಳು ಕೇಂದ್ರೀಕೃತ ದ್ರಾವಣಗಳಲ್ಲಿ ಮಾತ್ರ ಗಮನಾರ್ಹ ಬಣ್ಣವನ್ನು ಹೊಂದಿರುತ್ತವೆ. ಇದು ಪರ್ಮಾಂಗನೇಟ್ ಅಥವಾ ಡೈಕ್ರೋಮೇಟ್ನ ಬಣ್ಣಕ್ಕಿಂತ ಹಲವು ಪಟ್ಟು ದುರ್ಬಲವಾಗಿರುತ್ತದೆ, ಅದರ ಅಯಾನುಗಳು ಡಿ-ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವುದಿಲ್ಲ.
ಲ್ಯಾಪೋರ್ಟೆಯ ನಿಯಮವು ಸಮ್ಮಿತಿಯ ಕೇಂದ್ರವನ್ನು ಹೊಂದಿರುವ ಸಂಕೀರ್ಣಗಳ ಸಂದರ್ಭದಲ್ಲಿ ಮಾತ್ರ ಅನ್ವಯಿಸುತ್ತದೆ. ಆಕ್ಟಾಹೆಡ್ರನ್ ವಿರೂಪಗೊಂಡಾಗ, ಸಮ್ಮಿತಿಯ ಕೇಂದ್ರವು ಕಣ್ಮರೆಯಾಗುತ್ತದೆ, ಲ್ಯಾಪೋರ್ಟೆ ನಿಷೇಧವನ್ನು ತೆಗೆದುಹಾಕಲಾಗುತ್ತದೆ ಮತ್ತು ಬಣ್ಣವು ಕಾಣಿಸಿಕೊಳ್ಳುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, 3+ ಅಯಾನು ಬಣ್ಣರಹಿತವಾಗಿರುತ್ತದೆ, ಆದರೆ ಕಬ್ಬಿಣದ (III) ಲವಣಗಳ ದ್ರಾವಣಗಳು ಸಾಮಾನ್ಯವಾಗಿ ಹಳದಿ-ಕಿತ್ತಳೆ ಬಣ್ಣದಲ್ಲಿ ಜಲವಿಚ್ಛೇದನದಿಂದಾಗಿ ವಿರೂಪಗೊಂಡ ಅಷ್ಟಮುಖ ಪರಿಸರದೊಂದಿಗೆ ಅಸಮಪಾರ್ಶ್ವದ ಕಣಗಳ ರಚನೆಗೆ ಕಾರಣವಾಗುತ್ತವೆ.
ಸಂಕೀರ್ಣಗಳ ಬಣ್ಣ, ಒಂದು ಲೋಹದ ಡಿ-ಆರ್ಬಿಟಲ್ನಿಂದ ಇನ್ನೊಂದಕ್ಕೆ ಡಿ-ಡಿ ಪರಿವರ್ತನೆಗಳ ಜೊತೆಗೆ (ಆಕ್ಟಾಹೆಡ್ರಲ್ ಕಾಂಪ್ಲೆಕ್ಸ್ಗಳಲ್ಲಿ t 2g ನಿಂದ e g ವರೆಗೆ), ಇನ್ನೂ ಎರಡು ಅಂಶಗಳಿಂದ ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ: ಲಿಗಾಂಡ್ ಆರ್ಬಿಟಲ್ಗಳಿಂದ ಲೋಹದ ಕಕ್ಷೆಗಳಿಗೆ ಪರಿವರ್ತನೆಗಳು (ಅವುಗಳನ್ನು ಚಾರ್ಜ್ ವರ್ಗಾವಣೆ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ) ಮತ್ತು ಲಿಗಾಂಡ್ ಕಕ್ಷೆಗಳ ಒಳಗೆ ಪರಿವರ್ತನೆಗಳು. ಈ ಪರಿವರ್ತನೆಗಳು ಲ್ಯಾಪೋರ್ಟೆಯ ಆಳ್ವಿಕೆಯ ಅಡಿಯಲ್ಲಿ ಬರುವುದಿಲ್ಲ ಮತ್ತು ಆದ್ದರಿಂದ, ಹೆಚ್ಚಿನ ತೀವ್ರತೆಯನ್ನು ಹೊಂದಿರುತ್ತವೆ.
ಚಾರ್ಜ್ ವರ್ಗಾವಣೆ ಬ್ಯಾಂಡ್ ಯಾವುದೇ ಸಂಯುಕ್ತದ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸ್ಪೆಕ್ಟ್ರಮ್ನಲ್ಲಿ ಇರುತ್ತದೆ, ಆದಾಗ್ಯೂ, ಕೆಲವು ಸಂದರ್ಭಗಳಲ್ಲಿ ಇದು ಸ್ಪೆಕ್ಟ್ರಮ್ನ ನೇರಳಾತೀತ ಭಾಗದಲ್ಲಿದೆ ಮತ್ತು ನಮ್ಮಿಂದ ಬಣ್ಣವಾಗಿ ಗ್ರಹಿಸಲ್ಪಡುವುದಿಲ್ಲ. ಲಿಗಾಂಡ್ ಕಕ್ಷೆಗಳು ಮತ್ತು ಲೋಹದ ಕಕ್ಷೆಗಳ ಶಕ್ತಿಗಳ ನಡುವಿನ ವ್ಯತ್ಯಾಸವು ಕಡಿಮೆಯಾದರೆ, ಚಾರ್ಜ್ ವರ್ಗಾವಣೆ ಬ್ಯಾಂಡ್ ಸ್ಪೆಕ್ಟ್ರಮ್ನ ಗೋಚರ ಭಾಗಕ್ಕೆ ಬೀಳುತ್ತದೆ. ಇದು ಪರ್ಮಾಂಗನೇಟ್, ಡೈಕ್ರೋಮೇಟ್, ಪಾದರಸದ ಸಲ್ಫೈಡ್, ಟೈಟಾನಿಯಂ(IV) ಪೆರಾಕ್ಸೊ ಕಾಂಪ್ಲೆಕ್ಸ್ಗಳು ಮತ್ತು ಖಾಲಿ ಡಿ-ಆರ್ಬಿಟಲ್ಗಳೊಂದಿಗಿನ ಅನೇಕ ಇತರ ಸಂಯುಕ್ತಗಳ ತೀವ್ರವಾದ ಬಣ್ಣವನ್ನು ವಿವರಿಸುವ ಚಾರ್ಜ್ ವರ್ಗಾವಣೆಯಾಗಿದೆ. ಕೆಲವು ಸಂದರ್ಭಗಳಲ್ಲಿ, ಬೆಳಕಿನ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ, ಲಿಗಂಡ್ನ ಕಕ್ಷೆಗಳಿಂದ ಲೋಹದ ಕಕ್ಷೆಗಳಿಗೆ ಚಾರ್ಜ್ ವರ್ಗಾವಣೆಯು ಬದಲಾಯಿಸಲಾಗದಂತೆ ಸಂಭವಿಸುತ್ತದೆ, ಅಂದರೆ, ಇದು ರಾಸಾಯನಿಕ ಪ್ರಕ್ರಿಯೆಯೊಂದಿಗೆ ಇರುತ್ತದೆ. ಬೆಳ್ಳಿ ಹಾಲೈಡ್ಗಳ ದ್ಯುತಿರಾಸಾಯನಿಕ ವಿಘಟನೆಯು ಒಂದು ಉದಾಹರಣೆಯಾಗಿದೆ, ಇದು ಕಪ್ಪು ಮತ್ತು ಬಿಳಿ ಛಾಯಾಗ್ರಹಣದ ಆಧಾರವಾಗಿದೆ: Ag + Br – ¾® Ag 0 + Br 0 .
ಪೊಟ್ಯಾಸಿಯಮ್ ಪರ್ಮಾಂಗನೇಟ್ನ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸ್ಪೆಕ್ಟ್ರಮ್ನಲ್ಲಿ, ನಾಲ್ಕು ಬ್ಯಾಂಡ್ಗಳನ್ನು ಗಮನಿಸಲಾಗಿದೆ, ಇದು ಮುಖ್ಯವಾಗಿ ಲಿಗಾಂಡ್ನಲ್ಲಿ (a 1, t 2 σ ಆರ್ಬಿಟಲ್ಗಳು ಮತ್ತು e, t 1, t 2 π ಆರ್ಬಿಟಲ್ಗಳು) e*, t2 ಗೆ ಸ್ಥಳೀಕರಿಸಲ್ಪಟ್ಟ ನಾನ್ಬಾಂಡಿಂಗ್ ಆರ್ಬಿಟಲ್ಗಳಿಂದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಪರಿವರ್ತನೆಗಳಿಗೆ ಅನುಗುಣವಾಗಿರುತ್ತದೆ. '' ಲೋಹದ ಪರಮಾಣುವಿನ ಮೇಲೆ ಸ್ಥಳೀಕರಿಸಲಾದ ಆಂಟಿಬಾಂಡಿಂಗ್ ಆರ್ಬಿಟಲ್ಸ್ ಆರ್ಬಿಟಲ್ಸ್ ((ಚಿತ್ರ 1.37. ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಅಯಾನ್ MnO 4 ರ ಶಕ್ತಿಯ ರೇಖಾಚಿತ್ರ - π-ಬಂಧದೊಂದಿಗೆ. ಎಲೆಕ್ಟ್ರಾನ್ ಪರಿವರ್ತನೆಗಳನ್ನು ಬಾಣಗಳಿಂದ ತೋರಿಸಲಾಗಿದೆ):
ν 1 , Mn(e*) ¾ O(t 1) 17700 cm –1
ν 2 , Mn(t 2 '') ¾ O(t 1) 29500 cm –1
ν 3 , Mn(e*) ¾ O(t 2) 30300 cm –1
ν 4 , Mn(t 2 '') ¾ O(t 2) 44400 cm –1
ಕಡಿಮೆ ಶಕ್ತಿಯೊಂದಿಗೆ ಬ್ಯಾಂಡ್ ಸ್ಪೆಕ್ಟ್ರಮ್ನ ಗೋಚರ ಭಾಗದಲ್ಲಿ ಬೀಳುತ್ತದೆ (λ = 107/17700 = 565 nm), ಇದು ಹಸಿರು ಬೆಳಕಿನ ಹೀರಿಕೊಳ್ಳುವಿಕೆ ಮತ್ತು ಕಡುಗೆಂಪು-ಕೆಂಪು ಬೆಳಕಿನ ಪ್ರಸರಣಕ್ಕೆ ಅನುರೂಪವಾಗಿದೆ.
3. ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಕಾರ್ಯವಿಧಾನಗಳು.
ಬಹುಪಾಲು ರಾಸಾಯನಿಕ ಪ್ರಕ್ರಿಯೆಗಳು ಕೆಲವು ಪ್ರಾಥಮಿಕ ಹಂತಗಳ ಅನುಕ್ರಮ ಸರಪಳಿಯಾಗಿ ಸಂಭವಿಸುತ್ತವೆ ಮತ್ತು ಪ್ರತಿಕ್ರಿಯೆ ಸಮೀಕರಣವು ಕ್ರಿಯೆಯ ಮುಖ್ಯ ಅಂತಿಮ ಉತ್ಪನ್ನಗಳ ಬಗ್ಗೆ ಮಾಹಿತಿಯನ್ನು ಮಾತ್ರ ಹೊಂದಿರುತ್ತದೆ. ಆರಂಭಿಕ ಪದಾರ್ಥಗಳಿಂದ ಉತ್ಪನ್ನಗಳಿಗೆ ದಾರಿಯಲ್ಲಿ ಪ್ರಾಥಮಿಕ ರೂಪಾಂತರಗಳ ಈ ಅನುಕ್ರಮವನ್ನು ಯಾಂತ್ರಿಕತೆ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಮಧ್ಯಂತರ, ಸಾಮಾನ್ಯವಾಗಿ ಅಸ್ಥಿರ ಸಂಯುಕ್ತಗಳನ್ನು ಪ್ರತಿಕ್ರಿಯಾಕಾರಿಗಳಿಂದ ಉತ್ಪನ್ನಗಳಿಗೆ ಸಾಗುವ ಮಾರ್ಗವನ್ನು ಮಧ್ಯಂತರ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಯಾವುದೇ ಮಧ್ಯಂತರವು ಒಂದು ನಿರ್ದಿಷ್ಟ ಜೀವಿತಾವಧಿಯನ್ನು ಹೊಂದಿರುತ್ತದೆ, ಸಾಮಾನ್ಯವಾಗಿ ಅತ್ಯಂತ ಕಡಿಮೆ, 10 -14 ಸೆ. ಕ್ರಿಯೆಯ ಶಕ್ತಿಯ ಪ್ರೊಫೈಲ್ನಲ್ಲಿ ಇದು ಕನಿಷ್ಟ (Fig. a) ಗೆ ಅನುರೂಪವಾಗಿದೆ (Fig. 1.38. ಮೂಲಕ ಮುಂದುವರಿಯುವ ಪ್ರತಿಕ್ರಿಯೆಯ ಶಕ್ತಿಯ ಪ್ರೊಫೈಲ್ಗಳು: (a) ಮಧ್ಯಂತರ, (b) ಪರಿವರ್ತನೆಯ ಸ್ಥಿತಿ.). ನಿಯಮದಂತೆ, ಸ್ಪೆಕ್ಟ್ರಲ್ ವಿಧಾನಗಳಿಂದ ಪ್ರತಿಕ್ರಿಯೆ ಮಿಶ್ರಣದಲ್ಲಿ ಮಧ್ಯವರ್ತಿಗಳನ್ನು ಕಂಡುಹಿಡಿಯಬಹುದು ಮತ್ತು ಅಪರೂಪದ ಸಂದರ್ಭಗಳಲ್ಲಿ ಮಾತ್ರ ಅವುಗಳನ್ನು ಪ್ರತ್ಯೇಕ ರೂಪದಲ್ಲಿ ಪ್ರತ್ಯೇಕಿಸಬಹುದು. ಆದ್ದರಿಂದ, ಪ್ರತಿಕ್ರಿಯೆ ಕಾರ್ಯವಿಧಾನದ ಬಗ್ಗೆ ಮುಖ್ಯ ಮಾಹಿತಿಯನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ಅದರ ಚಲನಶಾಸ್ತ್ರವನ್ನು ಅಧ್ಯಯನ ಮಾಡುವ ಮೂಲಕ ಪಡೆಯಲಾಗುತ್ತದೆ - ದರ ಸ್ಥಿರಾಂಕಗಳನ್ನು ನಿರ್ಧರಿಸುವುದು ಮತ್ತು ಸಕ್ರಿಯಗೊಳಿಸುವ ನಿಯತಾಂಕಗಳನ್ನು ಲೆಕ್ಕಾಚಾರ ಮಾಡುವುದು (ಎಂಥಾಲ್ಪಿ, ಎಂಟ್ರೊಪಿ, ಪರಿಮಾಣ). ಈ ಸಂದರ್ಭದಲ್ಲಿ, ಯಾಂತ್ರಿಕತೆಯು ಚಲನಶಾಸ್ತ್ರದ ದತ್ತಾಂಶಕ್ಕೆ ಅನುಗುಣವಾಗಿರುವ ಒಂದು ಮಾದರಿಯಾಗಿದೆ, ಒಂದು ಮಾದರಿಯನ್ನು ಸುಧಾರಿಸಬಹುದು, ಮಾರ್ಪಡಿಸಬಹುದು, ಪರಿಷ್ಕರಿಸಬಹುದು.
ಕೆಲವು ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ, ಮಧ್ಯಂತರಗಳು ರೂಪುಗೊಳ್ಳುವುದಿಲ್ಲ, ಮತ್ತು ಪ್ರತಿಕ್ರಿಯಾಕಾರಿಗಳಿಂದ ಉತ್ಪನ್ನಗಳಿಗೆ ಪರಿವರ್ತನೆಯು ಅನುಕ್ರಮವಾಗಿ ಸಂಭವಿಸುತ್ತದೆ - ಪರಮಾಣುಗಳಲ್ಲಿ ಒಂದನ್ನು ಕ್ರಮೇಣ ತೆಗೆದುಹಾಕಲಾಗುತ್ತದೆ, ಮತ್ತು ಇನ್ನೊಂದು ವಿಧಾನಗಳು. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ಪ್ರತಿಕ್ರಿಯೆಯು ಮುಂದುವರಿಯುತ್ತದೆ ಎಂದು ಹೇಳಲಾಗುತ್ತದೆ ಪರಿವರ್ತನೆಯ ಸ್ಥಿತಿಅಥವಾ ಸಕ್ರಿಯ ಸಂಕೀರ್ಣ. ಇದು ಪ್ರತಿಕ್ರಿಯೆಯ ಶಕ್ತಿಯ ಪ್ರೊಫೈಲ್ನಲ್ಲಿ ಗರಿಷ್ಠ ಅನುರೂಪವಾಗಿದೆ (Fig. B).
ಸೇರ್ಪಡೆ: ಲೇಬಲ್ ಮತ್ತು ಜಡ ಸಂಕೀರ್ಣಗಳು
ಕಣದ ಥರ್ಮೋಡೈನಾಮಿಕ್ ಸ್ಥಿರತೆಯನ್ನು ಅದರ ವಿಘಟನೆಯ ಪ್ರತಿಕ್ರಿಯೆಗಾಗಿ ಗಿಬ್ಸ್ ಶಕ್ತಿಯ ಬದಲಾವಣೆಯಿಂದ ಅಥವಾ ಈ ಪ್ರಕ್ರಿಯೆಯ ಸ್ಥಿರತೆಯ ಸ್ಥಿರತೆಯ ಮೌಲ್ಯದಿಂದ ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ. ನೀಡಿದ ಕಣವು ಇತರ ಕಣಗಳೊಂದಿಗೆ ಎಷ್ಟು ಬೇಗನೆ ಸಂವಹನ ನಡೆಸುತ್ತದೆ ಅಥವಾ ಕೊಳೆಯುವಿಕೆಗೆ ಒಳಗಾಗುತ್ತದೆ ಎಂಬುದನ್ನು ಚಲನ ಸ್ಥಿರತೆ ತೋರಿಸುತ್ತದೆ. ರಾಸಾಯನಿಕ ಕಣವನ್ನು ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ ಜಡ, ಇದು 1 ನಿಮಿಷಕ್ಕಿಂತ ಹೆಚ್ಚಿನ ಅರ್ಧ-ಜೀವಿತಾವಧಿಯೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸಿದರೆ. ಹೆಚ್ಚಿನ ದರದಲ್ಲಿ ಪ್ರತಿಕ್ರಿಯಿಸುವ ಕಣಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ಲೇಬಲ್. ಚಲನ ಮತ್ತು ಥರ್ಮೋಡೈನಾಮಿಕ್ ಸ್ಥಿರತೆಯು ಒಂದಕ್ಕೊಂದು ಅವಲಂಬಿತವಾಗಿಲ್ಲ ಎಂದು ನೆನಪಿನಲ್ಲಿಡಬೇಕು, ಅಂದರೆ, ಅದೇ ವಸ್ತುವು ಹೆಚ್ಚಿನ ಸ್ಥಿರತೆಯ ಸ್ಥಿರತೆಯನ್ನು ಹೊಂದಿರುತ್ತದೆ ಮತ್ತು ಅದೇ ಸಮಯದಲ್ಲಿ ಜಡವಾಗಿರಬಹುದು, ಅಥವಾ ಇದಕ್ಕೆ ವಿರುದ್ಧವಾಗಿ ಲೇಬಲ್ ಆಗಿರಬಹುದು. ಅಂತಹ ಕೆಲವು ಉದಾಹರಣೆಗಳನ್ನು ಕೋಷ್ಟಕ 1.6 ರಲ್ಲಿ ನೀಡಲಾಗಿದೆ.
ಕೋಷ್ಟಕ 1.6. ಸ್ಥಿರತೆ ಸ್ಥಿರಾಂಕಗಳು ಮತ್ತು ಕೆಲವು ಲೋಹಗಳ ಸೈನೋ-ಸಂಕೀರ್ಣಗಳಲ್ಲಿ ಲಿಗಂಡ್ ಪರ್ಯಾಯದ ದರಗಳು.
ಹೆನ್ರಿ ಟೌಬ್ ಆಕ್ಟಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳ ಚಲನ ಸ್ಥಿರತೆ ಮತ್ತು ಆಕ್ಟಾಹೆಡ್ರಲ್ ಕ್ಷೇತ್ರದಲ್ಲಿ ಕೇಂದ್ರ ಅಯಾನಿನ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸಂರಚನೆಯ ನಡುವಿನ ಸಂಪರ್ಕವನ್ನು ತೋರಿಸಿದರು. ಟೌಬ್ ಪ್ರಕಾರ, ಈ ಕೆಳಗಿನ ಸಂಕೀರ್ಣಗಳು ಲೇಬಲ್ ಆಗಿವೆ:
ಕನಿಷ್ಠ ಒಂದು ಖಾಲಿ t 2g ಕಕ್ಷೆಯನ್ನು ಹೊಂದಿರುವುದು - ಅವರು ಅದನ್ನು ಸಹಾಯಕ (A, I a) ಕಾರ್ಯವಿಧಾನದ ಪ್ರಕಾರ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ ಬಳಸಬಹುದು, ಅಥವಾ
e g ಕಕ್ಷೆಯಲ್ಲಿ ಕನಿಷ್ಠ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ಅನ್ನು ಹೊಂದಿರುವುದು - ಇದು ವಿಘಟಿತ (D, I d) ಕಾರ್ಯವಿಧಾನದಿಂದ ಪ್ರತಿಕ್ರಿಯೆಯನ್ನು ಉತ್ತೇಜಿಸುತ್ತದೆ, ಏಕೆಂದರೆ e g ಕಕ್ಷೆಯಿಂದ ಎಲೆಕ್ಟ್ರಾನ್ ಅನ್ನು ತೆಗೆದುಹಾಕುವುದು ಪರಿವರ್ತನೆಯ ಸ್ಥಿತಿಯ ಶಕ್ತಿಯನ್ನು ಕಡಿಮೆ ಮಾಡುತ್ತದೆ.
ಹೀಗಾಗಿ, ಕ್ರೋಮಿಯಂ (III) (t 2g 3), ಕಬ್ಬಿಣದ ಕಡಿಮೆ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳು (II) (t 2g 6) ಮತ್ತು ಕಬ್ಬಿಣ (III) (t 2g 5), ಹಾಗೆಯೇ 4d-, 5d- ಸಂಕೀರ್ಣಗಳ ಆಕ್ಟಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳು ಪರಿವರ್ತನಾ ಅಂಶಗಳನ್ನು ಎರಡಕ್ಕಿಂತ ಹೆಚ್ಚು ಡಿ-ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯೊಂದಿಗೆ ಜಡ ಎಂದು ವರ್ಗೀಕರಿಸಲಾಗಿದೆ.
ಅಡೆಂಡಮ್ ಅಂತ್ಯ
ಅಜೈವಿಕ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಏಕೀಕೃತ ವರ್ಗೀಕರಣವನ್ನು ಇನ್ನೂ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿಲ್ಲ. ಸಾಂಪ್ರದಾಯಿಕವಾಗಿ, ನಾವು ಈ ಕೆಳಗಿನ ಯೋಜನೆಯನ್ನು ಪ್ರಸ್ತಾಪಿಸಬಹುದು (ಚಿತ್ರ 1.39. ಅಜೈವಿಕ ಪ್ರತಿಕ್ರಿಯೆಗಳ ವರ್ಗೀಕರಣವನ್ನು ವಿವರಿಸುವ ಯೋಜನೆ):
1) ಲಿಗಂಡ್ಗಳ ಪರ್ಯಾಯ, ಸೇರ್ಪಡೆ ಅಥವಾ ನಿರ್ಮೂಲನದ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಲೋಹದ ಸಮನ್ವಯ ಗೋಳದಲ್ಲಿನ ಬದಲಾವಣೆಯ ಮೇಲೆ ಪರಿಣಾಮ ಬೀರುತ್ತವೆ,
2) ರೆಡಾಕ್ಸ್ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಲೋಹದ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಕಾನ್ಫಿಗರೇಶನ್ನಲ್ಲಿನ ಬದಲಾವಣೆಯೊಂದಿಗೆ ಸಂಬಂಧ ಹೊಂದಿವೆ, ಆದರೆ ಅದರ ಸಮನ್ವಯ ಪರಿಸರದ ಮೇಲೆ ಪರಿಣಾಮ ಬೀರುವುದಿಲ್ಲ,
3) ಸಂಯೋಜಿತ ಲಿಗಂಡ್ಗಳ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಸಂಕೀರ್ಣದ ಸಮನ್ವಯ ಗೋಳವನ್ನು ಬದಲಾಯಿಸದೆ ಲಿಗಂಡ್ನಲ್ಲಿ ಬದಲಾವಣೆಯನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ.
ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು.ವಿಶಾಲ ಅರ್ಥದಲ್ಲಿ, ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಎಂದರೆ ಲೋಹದ ಸಮನ್ವಯ ಕ್ಷೇತ್ರದಲ್ಲಿ ಕೆಲವು ಲಿಗಂಡ್ಗಳನ್ನು ಇತರರೊಂದಿಗೆ ಬದಲಾಯಿಸುವ ಪ್ರಕ್ರಿಯೆಗಳು. ಅಂತಹ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿಯಲ್ಲಿ ಬದಲಾವಣೆಯೊಂದಿಗೆ ಅಥವಾ ಇಲ್ಲದೆ ಸಂಭವಿಸಬಹುದು. ಮೇಲಿನ ವರ್ಗೀಕರಣವನ್ನು ಅನುಸರಿಸಿ, ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿಗಳಲ್ಲಿ ಬದಲಾವಣೆಯಿಲ್ಲದೆ ಸಂಭವಿಸುವ ಪ್ರತಿಕ್ರಿಯೆಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಮಾತ್ರ ನಾವು ಈ ಪದವನ್ನು ಬಳಸುತ್ತೇವೆ.
ಅಜೈವಿಕ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳ ವರ್ಗೀಕರಣವನ್ನು ಲ್ಯಾಂಗ್ಫೋರ್ಡ್ ಮತ್ತು ಗ್ರೇ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದ್ದಾರೆ. ಇದು ಸೀಮಿತಗೊಳಿಸುವ ಕಾರ್ಯವಿಧಾನದ ವ್ಯಾಖ್ಯಾನವನ್ನು ಆಧರಿಸಿದೆ ಮತ್ತು ನಿರ್ದಿಷ್ಟ ಕಾರ್ಯವಿಧಾನದ ವಿವರಣೆಯ ಮೇಲೆ ಅಲ್ಲ. ಮೊದಲಿಗೆ, ಸ್ಟೊಚಿಯೊಮೆಟ್ರಿಕ್ ಕಾರ್ಯವಿಧಾನವನ್ನು ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ, ಮತ್ತು ನಂತರ ಆಂತರಿಕ ಒಂದು. ಸ್ಟೊಚಿಯೊಮೆಟ್ರಿಕ್ ಯಾಂತ್ರಿಕತೆಆರಂಭಿಕ ಪದಾರ್ಥಗಳಿಂದ ಉತ್ಪನ್ನಗಳಿಗೆ ಪರಿವರ್ತನೆಯಲ್ಲಿ ಪ್ರಾಥಮಿಕ ಹಂತಗಳ ಅನುಕ್ರಮವಾಗಿದೆ. ಇದು ವಿಘಟಿತ (D), ಸಹಾಯಕ (A) ಮತ್ತು ವಿನಿಮಯ (ಪರಸ್ಪರ ವಿನಿಮಯ, I) ಆಗಿರಬಹುದು. ವಿಘಟಿತ ಮತ್ತು ಸಹಾಯಕ ಪ್ರಕ್ರಿಯೆಗಳು ಒಂದಕ್ಕೊಂದು ನೇರವಾಗಿ ವಿರುದ್ಧವಾಗಿ ಎರಡು ಸೀಮಿತಗೊಳಿಸುವ ಪ್ರಕರಣಗಳನ್ನು ಪ್ರತಿನಿಧಿಸುತ್ತವೆ. ಮಧ್ಯಂತರ ರಚನೆಯ ಮೂಲಕ ಎರಡೂ ಪ್ರಕ್ರಿಯೆಗಳು ಎರಡು ಹಂತಗಳಲ್ಲಿ ಸಂಭವಿಸುತ್ತವೆ.
ವಿಘಟಿತ (ಡಿ)
ಪ್ರಕ್ರಿಯೆಯು ಎರಡು-ಹಂತವಾಗಿದೆ, ಸೀಮಿತಗೊಳಿಸುವ ಸಂದರ್ಭದಲ್ಲಿ ಇದು ಕಡಿಮೆ ಸಾಂದ್ರತೆಯೊಂದಿಗೆ ಮಧ್ಯಂತರ ಮೂಲಕ ಮುಂದುವರಿಯುತ್ತದೆ:
ML 6 + L, + Y ¾® ML 5 Y
ಸಹಾಯಕ (ಎ)
ಪ್ರಕ್ರಿಯೆಯು ಎರಡು-ಹಂತವಾಗಿದೆ, ಹೆಚ್ಚಿದ ಸಾಂದ್ರತೆಯೊಂದಿಗೆ ಮಧ್ಯಂತರ ರಚನೆಯಿಂದ ನಿರೂಪಿಸಲ್ಪಟ್ಟಿದೆ:
ML 6 + Y, ¾® ML 5 Y + L
ಪರಸ್ಪರ ವಿನಿಮಯ (I)
ಹೆಚ್ಚಿನ ವಿನಿಮಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಈ ಕಾರ್ಯವಿಧಾನದ ಮೂಲಕ ಮುಂದುವರಿಯುತ್ತವೆ. ಪ್ರಕ್ರಿಯೆಯು ಒಂದು ಹಂತವಾಗಿದೆ ಮತ್ತು ಮಧ್ಯಂತರ ರಚನೆಯೊಂದಿಗೆ ಇರುವುದಿಲ್ಲ. ಪರಿವರ್ತನೆಯ ಸ್ಥಿತಿಯಲ್ಲಿ, ಕಾರಕ ಮತ್ತು ಹೊರಹೋಗುವ ಗುಂಪು ಪ್ರತಿಕ್ರಿಯೆ ಕೇಂದ್ರದೊಂದಿಗೆ ಸಂಬಂಧ ಹೊಂದಿದೆ, ಅದರ ಹತ್ತಿರದ ಸಮನ್ವಯ ಗೋಳವನ್ನು ನಮೂದಿಸಿ, ಮತ್ತು ಪ್ರತಿಕ್ರಿಯೆಯ ಸಮಯದಲ್ಲಿ ಒಂದು ಗುಂಪನ್ನು ಇನ್ನೊಂದರಿಂದ ಸ್ಥಳಾಂತರಿಸಲಾಗುತ್ತದೆ, ಎರಡು ಲಿಗಂಡ್ಗಳ ವಿನಿಮಯ ಸಂಭವಿಸುತ್ತದೆ:
ML 6 + Y ML 5 Y + L.
ಪರಿವರ್ತನೆಯ ಸ್ಥಿತಿಯು ಬಾಹ್ಯ-ಗೋಳದ ಸಂಕೀರ್ಣವಾಗಿದೆ ಅಥವಾ ಚಾರ್ಜ್ಡ್ ಲಿಗಂಡ್ಗಳ ಸಂದರ್ಭದಲ್ಲಿ, ಅಯಾನು ಜೋಡಿ MX 5 L + Y - .
ಆಂತರಿಕ ಕಾರ್ಯವಿಧಾನ (ಎಅಥವಾ ಡಿ) ಆಣ್ವಿಕ ಮಟ್ಟದಲ್ಲಿ ಲಿಗಂಡ್ ಪರ್ಯಾಯದ ಪ್ರಕ್ರಿಯೆಯನ್ನು ನಿರೂಪಿಸುತ್ತದೆ. ಎರಡು ಪ್ರಕ್ರಿಯೆಗಳಲ್ಲಿ ಯಾವುದು - ಪರಿವರ್ತನೆಯ ಸ್ಥಿತಿಯಲ್ಲಿ ಬಂಧದ ರಚನೆ ಅಥವಾ ಛಿದ್ರ - ಸೀಮಿತವಾಗಿದೆ ಎಂಬುದನ್ನು ಇದು ತೋರಿಸುತ್ತದೆ. ಪ್ರತಿಕ್ರಿಯೆ ದರವನ್ನು ಪ್ರತಿಕ್ರಿಯೆ ಕೇಂದ್ರ ಮತ್ತು ಕಾರಕದ ನಡುವಿನ ಬಂಧದ ರಚನೆಯಿಂದ ನಿರ್ಧರಿಸಿದರೆ, ನಾವು ಸಹಾಯಕ ಸಕ್ರಿಯಗೊಳಿಸುವಿಕೆಯ ಬಗ್ಗೆ ಮಾತನಾಡುತ್ತೇವೆ. ಇಲ್ಲದಿದ್ದರೆ, ಸೀಮಿತಗೊಳಿಸುವ ಅಂಶವು ಪ್ರತಿಕ್ರಿಯೆ ಕೇಂದ್ರ ಮತ್ತು ಹೊರಹೋಗುವ ಗುಂಪಿನ ನಡುವಿನ ಸಂಪರ್ಕದ ಛಿದ್ರವಾದಾಗ, ಪ್ರಕ್ರಿಯೆಯು ವಿಘಟಿತ ಸಕ್ರಿಯಗೊಳಿಸುವಿಕೆಯೊಂದಿಗೆ ಮುಂದುವರಿಯುತ್ತದೆ. ಸ್ಟೊಚಿಯೊಮೆಟ್ರಿಕ್ ಕಾರ್ಯವಿಧಾನಕ್ಕೆ ತಿರುಗಿದರೆ, ವಿಘಟಿತ ಪ್ರಕ್ರಿಯೆಯು ಯಾವಾಗಲೂ ವಿಘಟಿತ ಸಕ್ರಿಯಗೊಳಿಸುವಿಕೆಗೆ ಅನುರೂಪವಾಗಿದೆ ಎಂಬುದನ್ನು ಗಮನಿಸುವುದು ಸುಲಭ, ಮತ್ತು ಸಹಾಯಕ ಪ್ರಕ್ರಿಯೆಯು ಯಾವಾಗಲೂ ಸಹಾಯಕ ಸಕ್ರಿಯಗೊಳಿಸುವಿಕೆಗೆ ಅನುರೂಪವಾಗಿದೆ, ಅಂದರೆ, ಆಂತರಿಕ ಕಾರ್ಯವಿಧಾನದ ಪರಿಕಲ್ಪನೆಯು ಮಾಹಿತಿಯುಕ್ತವಾಗಿ ಹೊರಹೊಮ್ಮುತ್ತದೆ ಪರಸ್ಪರ ವಿನಿಮಯ ಕಾರ್ಯವಿಧಾನ - ಇದು ವಿಘಟಿತ (I d) ಮತ್ತು ಸಹಾಯಕ (I a) ಸಕ್ರಿಯಗೊಳಿಸುವಿಕೆ ಎರಡರಲ್ಲೂ ಸಂಭವಿಸಬಹುದು. ಅಸೋಸಿಯೇಟಿವ್ ಆಕ್ಟಿವೇಷನ್ (Ia) ನೊಂದಿಗೆ ಪರಸ್ಪರ ವಿನಿಮಯ ಕಾರ್ಯವಿಧಾನದ ಸಂದರ್ಭದಲ್ಲಿ, ಪ್ರತಿಕ್ರಿಯೆ ದರವು Y ಯ ಸ್ವರೂಪವನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ. ಪರಿವರ್ತನೆಯ ಸ್ಥಿತಿಯಲ್ಲಿ, ಲೋಹದ ಪರಮಾಣು ಹೊರಹೋಗುವ ಗುಂಪು ಮತ್ತು ಆಕ್ರಮಣಕಾರಿ ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್ ಎರಡಕ್ಕೂ ಬಿಗಿಯಾಗಿ ಬಂಧಿಸಲ್ಪಡುತ್ತದೆ. ಪ್ಲಾಟಿನಂ ಕಾಂಪ್ಲೆಕ್ಸ್ನಲ್ಲಿ ಡೈಥೈಲೆನೆಟ್ರಿಯಾಮೈನ್ (ಡೈನ್) ನೊಂದಿಗೆ ಕ್ಲೋರಿನ್ ಪರಮಾಣುವನ್ನು ಬ್ರೋಮಿನ್ ಮತ್ತು ಅಯೋಡಿನ್ನೊಂದಿಗೆ ಬದಲಾಯಿಸುವ ಪ್ರಕ್ರಿಯೆಯು ಒಂದು ಉದಾಹರಣೆಯಾಗಿದೆ:
Y - ¾¾® + + Cl -
Y = Br, I ವೇಗಗಳು ಬಹಳವಾಗಿ ಬದಲಾಗುತ್ತವೆ.
ವಿಘಟಿತ ಸಕ್ರಿಯಗೊಳಿಸುವಿಕೆ (I d) ಯೊಂದಿಗೆ ಪರಸ್ಪರ ವಿನಿಮಯ ಕಾರ್ಯವಿಧಾನದ ಸಂದರ್ಭದಲ್ಲಿ, ಪ್ರತಿಕ್ರಿಯೆ ದರವು ಕಾರಕ Y ಯ ಸ್ವರೂಪವನ್ನು ಅವಲಂಬಿಸಿರುವುದಿಲ್ಲ. ಪರಿವರ್ತನೆಯ ಸ್ಥಿತಿಯಲ್ಲಿ ಆಕ್ರಮಣ ಮಾಡುವ ಮತ್ತು ಬಿಡುವ ಗುಂಪುಗಳು ಕೇಂದ್ರ ಅಯಾನಿಗೆ ದುರ್ಬಲವಾಗಿ ಬಂಧಿಸಲ್ಪಡುತ್ತವೆ. ಅನೇಕ ಪರಿವರ್ತನಾ ಲೋಹಗಳ ಆಕ್ವಾ ಸಂಕೀರ್ಣಗಳಲ್ಲಿ ನೀರನ್ನು ಅಮೈನ್ನೊಂದಿಗೆ ಬದಲಾಯಿಸಲು ಈ ಕಾರ್ಯವಿಧಾನವನ್ನು ಬಳಸಲಾಗುತ್ತದೆ, ಉದಾಹರಣೆಗೆ, ನಿಕಲ್:
2+ + Y ¾¾® 2+ + H 2 O
Y = NH 3, py ವೇಗಗಳು ಹತ್ತಿರದಲ್ಲಿವೆ.
ಅನೇಕ ಲೋಹಗಳ ಸಂಕೀರ್ಣಗಳಲ್ಲಿ ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಕಾರ್ಯವಿಧಾನಗಳ ಅಧ್ಯಯನವು ಆರಂಭಿಕ ಹಂತದಲ್ಲಿ ಮಾತ್ರ. ಪ್ಲಾಟಿನಂ ಮತ್ತು ಕ್ರೋಮಿಯಂ (III) ಮತ್ತು ಕೋಬಾಲ್ಟ್ (III) ನ ಆಕ್ಟಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳ ಚದರ-ಪ್ಲಾನರ್ ಸಂಕೀರ್ಣಗಳಿಗೆ ಮಾತ್ರ ಸಮಗ್ರ ಮಾಹಿತಿಯನ್ನು ಪಡೆಯಲಾಗಿದೆ. ಪ್ಲಾಟಿನಂ (II) ಸಂಕೀರ್ಣಗಳಲ್ಲಿ, ಪರ್ಯಾಯವು ತ್ರಿಕೋನ ಬೈಪಿರಮಿಡ್ ರೂಪದಲ್ಲಿ ಮಧ್ಯಂತರ ಅಥವಾ ಪರಿವರ್ತನೆಯ ಸ್ಥಿತಿಯ ಮೂಲಕ ಸಹಾಯಕ ಕಾರ್ಯವಿಧಾನದ (A, Ia) ಪ್ರಕಾರ ಸಂಭವಿಸುತ್ತದೆ ಎಂದು ದೃಢವಾಗಿ ಸ್ಥಾಪಿತವಾಗಿದೆ ಎಂದು ಪರಿಗಣಿಸಬಹುದು. ಆಕ್ಟಾಹೆಡ್ರಲ್ ಕೋಬಾಲ್ಟ್(III) ಸಂಕೀರ್ಣಗಳು ವಿಘಟಿತವಾಗಿ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತವೆ (D, I d ಕಾರ್ಯವಿಧಾನಗಳು). ಈ ಅಂಶಗಳ ರಸಾಯನಶಾಸ್ತ್ರವನ್ನು ವಿವರಿಸುವಾಗ ಅಂತಹ ಪ್ರತಿಕ್ರಿಯೆಗಳ ನಿರ್ದಿಷ್ಟ ಉದಾಹರಣೆಗಳನ್ನು ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ.
ರೆಡಾಕ್ಸ್ ಪ್ರತಿಕ್ರಿಯೆಗಳು.ಹೆಚ್ಚಿನ ರೆಡಾಕ್ಸ್ ಪ್ರಕ್ರಿಯೆಗಳು ಪ್ರತ್ಯೇಕ ಪ್ರಾಥಮಿಕ ಹಂತಗಳ ಸಂಕೀರ್ಣ ಸಂಯೋಜನೆಯಾಗಿದೆ, ಪ್ರತಿಯೊಂದೂ ಒಂದು ಅಥವಾ ಕಡಿಮೆ ಆಗಾಗ್ಗೆ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವರ್ಗಾವಣೆಯನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ. ದ್ರಾವಣಗಳಲ್ಲಿ ಹೆಚ್ಚಿನ ಸಂಖ್ಯೆಯ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಏಕಕಾಲಿಕ ವರ್ಗಾವಣೆ ಅಸಾಧ್ಯ.
ಏಕ-ಎಲೆಕ್ಟ್ರಾನ್ ವರ್ಗಾವಣೆಯು ಎರಡು ಕಾರ್ಯವಿಧಾನಗಳಲ್ಲಿ ಒಂದರ ಮೂಲಕ ಸಂಭವಿಸಬಹುದು: ಹೊರ-ಗೋಳ, ಅಂದರೆ, ಸುರಂಗ, ಅಥವಾ ಒಳ-ಗೋಳ, ಸೇತುವೆಯ ಲಿಗಂಡ್ ಮೂಲಕ. ಹಾಲೈಡ್ಗಳು, ಹೈಡ್ರಾಕ್ಸೈಡ್ ಅಯಾನುಗಳು ಮತ್ತು ಲೋಹಗಳ ನಡುವಿನ ಸೇತುವೆಗಳಾಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸಬಲ್ಲ ಕಾರ್ಬಾಕ್ಸಿಲ್ ಗುಂಪುಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ಸಂಕೀರ್ಣಗಳಲ್ಲಿ ಅಂತರ್ಗೋಳದ ಕಾರ್ಯವಿಧಾನವನ್ನು ಅರಿತುಕೊಳ್ಳಲಾಗುತ್ತದೆ. ಪೆಂಟಮೈನ್ ಕ್ಲೋರೊಕೊಬಾಲ್ಟ್ (III) ಮತ್ತು ಹೆಕ್ಸಾಕ್ವಾಕ್ರೋಮ್ (II) ಅಯಾನುಗಳ ನಡುವಿನ ಪ್ರತಿಕ್ರಿಯೆಯು ಒಂದು ಉದಾಹರಣೆಯಾಗಿದೆ. ಪ್ರಕ್ರಿಯೆಯನ್ನು ಸ್ಥೂಲವಾಗಿ ಮೂರು ಹಂತಗಳಾಗಿ ವಿಂಗಡಿಸಬಹುದು: ಬ್ರಿಡ್ಜಿಂಗ್ ಕ್ಲೋರೈಡ್ ಅಯಾನು, ಎಲೆಕ್ಟ್ರಾನ್ ವರ್ಗಾವಣೆ ಮತ್ತು ಬ್ರಿಡ್ಜಿಂಗ್ ಸಂಕೀರ್ಣದ ವಿಭಜನೆಯೊಂದಿಗೆ ಹೆಟೆರೊಮೆಟಾಲಿಕ್ ಸಂಕೀರ್ಣದ ರಚನೆ. ಪರಿಣಾಮವಾಗಿ 2+ ಅಯಾನು, ಲೇಬಲ್ ಆಗಿರುವುದರಿಂದ, ತಕ್ಷಣವೇ ಆಕ್ವಾ ಸಂಕೀರ್ಣವಾಗಿ ಬದಲಾಗುತ್ತದೆ, ಮತ್ತು ಜಡ [(H 2 O) 5 CrCl] 2+ ನೀರಿನೊಂದಿಗೆ ಸಂವಹನ ಮಾಡುವುದಿಲ್ಲ:

ಸೇತುವೆಗಳಾಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸುವ ವ್ಯವಸ್ಥೆಯಲ್ಲಿ ಯಾವುದೇ ಕಣಗಳಿಲ್ಲದಿದ್ದರೆ, ಪ್ರಕ್ರಿಯೆಯು ಬಾಹ್ಯ ಗೋಳದಲ್ಲಿ ಮುಂದುವರಿಯುತ್ತದೆ:
2+ + 3+ = 3+ + 2+ .
ಅಧ್ಯಾಯ 6 ರಲ್ಲಿ ಚರ್ಚಿಸಲಾದ ಆಕ್ಸಿಡೇಟಿವ್ ಸೇರ್ಪಡೆ ಮತ್ತು ರಿಡಕ್ಟಿವ್ ಎಲಿಮಿನೇಷನ್ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಹೈಲೈಟ್ ಮಾಡುವುದು ವಿಶೇಷವಾಗಿ ಅವಶ್ಯಕವಾಗಿದೆ.
ಸಂಘಟಿತ ಲಿಗಂಡ್ಗಳ ಪ್ರತಿಕ್ರಿಯೆಗಳು.ಈ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಗುಂಪು ಲೋಹದ ಅಯಾನುಗಳಿಂದ ಸಂಯೋಜಿಸಲ್ಪಟ್ಟ ಲಿಗಂಡ್ಗಳ ಮಾರ್ಪಾಡು ಪ್ರಕ್ರಿಯೆಗಳನ್ನು ಒಳಗೊಂಡಿದೆ. ಉದಾಹರಣೆಗೆ, ಉಚಿತ ಡೈಕೆಟೋನ್ಗಳಂತಹ ಡಿಕೆಟೋನೇಟ್ ಸಂಕೀರ್ಣಗಳನ್ನು ನೈಟ್ರೇಟ್, ಅಸಿಲೇಟೆಡ್ ಅಥವಾ ಹ್ಯಾಲೊಜೆನೇಟ್ ಮಾಡಬಹುದು. ಸಂಘಟಿತ ಲಿಗಂಡ್ಗಳ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಅತ್ಯಂತ ಆಸಕ್ತಿದಾಯಕ ಮತ್ತು ಅಸಾಮಾನ್ಯ ಉದಾಹರಣೆಯಾಗಿದೆ ಟೆಂಪ್ಲೇಟ್ ಸಂಶ್ಲೇಷಣೆ- ಲೋಹದ ಅಯಾನಿನ ಮೇಲೆ ಲಿಗಂಡ್ ಅನ್ನು "ಜೋಡಿಸುವ" ಒಂದು ಅನನ್ಯ ವಿಧಾನ. ತಾಮ್ರ (II) ಅಯಾನುಗಳ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಸಂಭವಿಸುವ ಥಾಲಿಕ್ ಆಮ್ಲ ನೈಟ್ರೈಲ್ನಿಂದ ಥಾಲೋಸೈನೈನ್ಗಳ ಸಂಶ್ಲೇಷಣೆ ಮತ್ತು ನಿಕಲ್ (II) ಅಯಾನುಗಳ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಸಂಭವಿಸುವ 2-ಅಮಿನೊಬೆನ್ಜಾಲ್ಡಿಹೈಡ್ನಿಂದ ಮ್ಯಾಕ್ರೋಸೈಕ್ಲಿಕ್ ಸ್ಕಿಫ್ ಬೇಸ್ನ ಸಂಶ್ಲೇಷಣೆ ಒಂದು ಉದಾಹರಣೆಯಾಗಿದೆ:

ಲೋಹದ ಅನುಪಸ್ಥಿತಿಯಲ್ಲಿ, ಪ್ರಕ್ರಿಯೆಯು ವಿಭಿನ್ನ ಹಾದಿಯಲ್ಲಿ ಮುಂದುವರಿಯುತ್ತದೆ, ಮತ್ತು ಅಪೇಕ್ಷಿತ ಉತ್ಪನ್ನವು ಪ್ರತಿಕ್ರಿಯೆ ಮಿಶ್ರಣದಲ್ಲಿ ಅಲ್ಪ ಪ್ರಮಾಣದಲ್ಲಿ ಮಾತ್ರ ಇರುತ್ತದೆ. ಲೋಹದ ಅಯಾನು ಟೆಂಪ್ಲೇಟ್ ಸಂಶ್ಲೇಷಣೆಯಲ್ಲಿ ಮ್ಯಾಟ್ರಿಕ್ಸ್ ("ಟೆಂಪ್ಲೇಟ್") ಆಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸುತ್ತದೆ, ಪರಸ್ಪರ ಸಮತೋಲನದಲ್ಲಿರುವ ಉತ್ಪನ್ನಗಳಲ್ಲಿ ಒಂದನ್ನು ಸ್ಥಿರಗೊಳಿಸುತ್ತದೆ ಮತ್ತು ಅದರ ರಚನೆಯ ಕಡೆಗೆ ಸಮತೋಲನವನ್ನು ಬದಲಾಯಿಸುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, X + Y ¾® ಪ್ರತಿಕ್ರಿಯೆಯಲ್ಲಿ A ಮತ್ತು B ಉತ್ಪನ್ನಗಳ ಮಿಶ್ರಣವು ರೂಪುಗೊಳ್ಳುತ್ತದೆ, ಇದರಲ್ಲಿ ಕಡಿಮೆ ಶಕ್ತಿಯನ್ನು ಹೊಂದಿರುವ B, ಮೇಲುಗೈ ಸಾಧಿಸುತ್ತದೆ. ಲೋಹದ ಅಯಾನುಗಳ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ, ವಸ್ತು A ವು M ನೊಂದಿಗೆ ಸಂಕೀರ್ಣ ರೂಪದಲ್ಲಿ ಪ್ರತಿಕ್ರಿಯೆ ಉತ್ಪನ್ನಗಳಲ್ಲಿ ಮೇಲುಗೈ ಸಾಧಿಸುತ್ತದೆ (ಚಿತ್ರ 1.40. ಲೋಹದ ಅಯಾನು (ಎಡ) ಮತ್ತು ಅದರ ಅನುಪಸ್ಥಿತಿಯಲ್ಲಿ X ಮತ್ತು Y ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಶಕ್ತಿ ರೇಖಾಚಿತ್ರ ಉಪಸ್ಥಿತಿ (ಬಿ)).
ಪ್ರಶ್ನೆಗಳು ಮತ್ತು ಕಾರ್ಯಗಳು
1. ಈ ಕೆಳಗಿನ ಯಾವ ಸಂಯುಕ್ತಗಳು ಪೆರೋವ್ಸ್ಕೈಟ್ ರಚನೆಯನ್ನು ಹೊಂದಿದೆ? BaTiO 3, LiNbO 3, LaCrO 3, FeTiO 3, Na 2 WO 4, CuLa 2 O 4, La 2 MgRuO 6. ಅಯಾನಿಕ್ ತ್ರಿಜ್ಯಗಳ ಕೋಷ್ಟಕವನ್ನು ಅನುಬಂಧದಲ್ಲಿ ನೀಡಲಾಗಿದೆ. ಸಂಕೀರ್ಣ ಆಕ್ಸೈಡ್ ಹಂತಗಳಲ್ಲಿ, ಬಿ ಸ್ಥಾನಗಳು ಎರಡು ವಿಭಿನ್ನ ಲೋಹಗಳ ಕ್ಯಾಟಯಾನುಗಳನ್ನು ಹೊಂದಿರಬಹುದು ಎಂಬುದನ್ನು ನೆನಪಿನಲ್ಲಿಡಿ.
2. TCP ಬಳಸಿ, ಈ ಕೆಳಗಿನ ಸ್ಪಿನೆಲ್ಗಳು ನೇರ ಅಥವಾ ತಲೆಕೆಳಗಾದವು ಎಂಬುದನ್ನು ನಿರ್ಧರಿಸಿ: ZnFe 2 O 4, CoFe 2 O 4, Co 3 O 4, Mn 3 O 4, CuRh 2 O 4.
3. ಥಿಯೋಸೈನೇಟ್ ಅಯಾನ್ SCN - ಎರಡು ದಾನಿ ಕೇಂದ್ರಗಳನ್ನು ಹೊಂದಿದೆ - ಕಠಿಣ ಮತ್ತು ಮೃದು. ಕ್ಯಾಲ್ಸಿಯಂ ಮತ್ತು ತಾಮ್ರದ(I) ಥಿಯೋಸೈನೇಟ್ ಸಂಕೀರ್ಣಗಳು ಯಾವ ರಚನೆಯನ್ನು ಹೊಂದಿರುತ್ತವೆ ಎಂಬುದನ್ನು ಊಹಿಸಿ. ತಾಮ್ರ (II) ಥಿಯೋಸೈನೇಟ್ ಅನ್ನು ಪಡೆಯಲು ಏಕೆ ಸಾಧ್ಯವಿಲ್ಲ?
4. Cr 2+ ಆಕ್ವಾ ಅಯಾನ್ನ (ಗ್ರೌಂಡ್ ಸ್ಟೇಟ್ ಟರ್ಮ್ 5 D) ಸ್ಪೆಕ್ಟ್ರಮ್ ಎರಡು ಬ್ಯಾಂಡ್ಗಳನ್ನು ಹೊಂದಿದೆ (Fig. 1.41. Cr 2+ ಆಕ್ವಾ ಅಯಾನ್ನ ಸ್ಪೆಕ್ಟ್ರಮ್), ಆದರೂ ಹತ್ತಿರದ ಉತ್ಸುಕ ಸ್ಥಿತಿಗಳ ನಿಯಮಗಳಲ್ಲಿ ಒಂದೂ ಇಲ್ಲ ಅದೇ ಬಹುತ್ವ. ಇದನ್ನು ಏನು ವಿವರಿಸುತ್ತದೆ? ಈ ಅಯಾನು ಯಾವ ಬಣ್ಣವನ್ನು ಹೊಂದಿದೆ?
5. ಕೆಳಗಿನ Δο ಮೌಲ್ಯಗಳನ್ನು ಬಳಸಿ, kJ/mol ನಲ್ಲಿ ಕೆಳಗಿನ ಸಂಕೀರ್ಣಗಳಿಗಾಗಿ ESC ಅನ್ನು ಲೆಕ್ಕಹಾಕಿ:
(a) 2–, Δο = 15000 cm–1,
(b) 2+, Δο = 13000 cm–1,
(c) 2–, Δο (4–ಕ್ಕೆ)= 21000 cm–1,
19000 cm –1, 1 kJ/mol = 83 cm –1 ಗೆ ಸಮನಾದ ಜೋಡಣೆಯ ಶಕ್ತಿಯನ್ನು ತೆಗೆದುಕೊಳ್ಳಿ. ಅವರ ಕಾಂತೀಯ ಕ್ಷಣಗಳನ್ನು ಲೆಕ್ಕಾಚಾರ ಮಾಡಿ (ಸ್ಪಿನ್ ಘಟಕ).
6. TCP ಬಳಸಿ, CN - ಅಯಾನ್ ಹೆಕ್ಸಾಕ್ವಾನಿಕಲ್(III) ಅಯಾನ್ನೊಂದಿಗೆ ಹೆಕ್ಸಾಕ್ವಾನಿಕಲ್ (II) ಮತ್ತು ಹೆಕ್ಸಾಕ್ವಾನಿಕಲ್ (II) ಅಯಾನ್ನೊಂದಿಗೆ ಟೆಟ್ರಾಸಿಯಾನೊನಿಕೆಲೇಟ್ (II) ಅನ್ನು ರೂಪಿಸಲು ಏಕೆ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತದೆ ಎಂಬುದನ್ನು ವಿವರಿಸಿ.
7. ತಾಮ್ರ(II) ಆಕ್ವಾ ಕಾಂಪ್ಲೆಕ್ಸ್ನಲ್ಲಿ ನೀರನ್ನು ಅಮೋನಿಯದೊಂದಿಗೆ ಅನುಕ್ರಮವಾಗಿ ಬದಲಾಯಿಸುವ ಪ್ರತಿಕ್ರಿಯೆಯ ಸ್ಥಿರಾಂಕಗಳನ್ನು ಕೆಳಗೆ ನೀಡಲಾಗಿದೆ: K 1 = 2´10 4 , K 2 = 4´10 3 , K 3 = 1´10 3 , K 4 = 2´10 2 , K5 = 3´10 –1, K6<< 1. Чем объясняется трудность вхождения пятой и шестой молекул аммиака в координационную сферу меди?
8. 3d ಸಾಲಿನಲ್ಲಿ ಚಲಿಸುವಾಗ ಕ್ಯಾಟಯಾನುಗಳ ಬಿಗಿತವು ಹೇಗೆ ಬದಲಾಗುತ್ತದೆ? ಸಂಕೀರ್ಣಗಳ ಸ್ಥಿರತೆಯ ಸ್ಥಿರಾಂಕಗಳಲ್ಲಿನ ಬದಲಾವಣೆಯ ಕ್ರಮಕ್ಕೆ ಇದು ಸ್ಥಿರವಾಗಿದೆಯೇ (ಇರ್ವಿಂಗ್-ವಿಲಿಯಮ್ಸ್ ಸರಣಿ, ಚಿತ್ರ 1.34).
9. ಹೆಕ್ಸಾಕ್ವಾಟಿಕ್ ಐರನ್ (III) ಅಯಾನು ಬಣ್ಣರಹಿತವಾಗಿದೆ ಮತ್ತು ಕಬ್ಬಿಣದ (III) ಲವಣಗಳ ದ್ರಾವಣಗಳನ್ನು ಏಕೆ ಬಣ್ಣಿಸಲಾಗಿದೆ ಎಂಬುದನ್ನು ವಿವರಿಸಿ.
10. 3– + 3– = 4– + 2– ಪ್ರತಿಕ್ರಿಯೆಗೆ ಕಾರ್ಯವಿಧಾನವನ್ನು ಸೂಚಿಸಿ, ದ್ರಾವಣದಲ್ಲಿ ಥಿಯೋಸೈನೇಟ್ ಅಯಾನುಗಳ ಪರಿಚಯವು ಪ್ರತಿಕ್ರಿಯೆ ದರದಲ್ಲಿ ಬದಲಾವಣೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ ಎಂದು ತಿಳಿದಿದ್ದರೆ ಮತ್ತು ದರವು ಪ್ರಾಯೋಗಿಕವಾಗಿ ಸ್ವತಂತ್ರವಾಗಿರುತ್ತದೆ ಅಮೋನಿಯ ಉಪಸ್ಥಿತಿ. ಈ ಸತ್ಯಗಳಿಗೆ ವಿವರಣೆಯನ್ನು ನೀಡಿ.
ಅವುಗಳನ್ನು ಸುತ್ತುವರೆದಿರುವ ಚಾರ್ಜ್ಡ್ ಕಣಗಳ ವಿದ್ಯುತ್ ಕ್ಷೇತ್ರದ ಕ್ರಿಯೆಯ ಅಡಿಯಲ್ಲಿ ಪರಿವರ್ತನೆಯ ಲೋಹದ ಅಯಾನುಗಳ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆಯಲ್ಲಿನ ಬದಲಾವಣೆಗಳ ಪರಿಕಲ್ಪನೆಯನ್ನು ಬೆಕ್ವೆರೆಲ್ ಪ್ರಸ್ತಾಪಿಸಿದರು ಮತ್ತು ಎಚ್.ಎ. ಆರಂಭದಲ್ಲಿ ಬೆಥೆ ಮತ್ತು ಜೆ. ವ್ಯಾನ್ ವ್ಲೆಕ್ XX ವಿ. ಈ ಪರಿಕಲ್ಪನೆಗಳನ್ನು ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆ ಮತ್ತು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳ ಗುಣಲಕ್ಷಣಗಳ ವಿವರಣೆಗೆ ಮಧ್ಯದಲ್ಲಿ ಮಾತ್ರ ಅನ್ವಯಿಸಲಾಗಿದೆ XX ಶತಮಾನದಲ್ಲಿ H. ಹಾರ್ಟ್ಮನ್ ಮತ್ತು ಮಾದರಿಯನ್ನು "ಕ್ರಿಸ್ಟಲ್ ಫೀಲ್ಡ್ ಥಿಯರಿ" (CFT) ಎಂದು ಕರೆಯಲಾಯಿತು.
ಪರಿವರ್ತನೆ ಸಂಕೀರ್ಣಗಳಿಗೆ TCH ನ ಮೂಲ ನಿಬಂಧನೆಗಳು d ಲೋಹಗಳು ಚಿತ್ರ. 24):
1. - ಲಿಗಂಡ್ಗಳೊಂದಿಗಿನ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ ಪರಸ್ಪರ ಕ್ರಿಯೆಯಿಂದಾಗಿ ಸಂಕೀರ್ಣವು ಅಸ್ತಿತ್ವದಲ್ಲಿದೆ ಮತ್ತು ಸ್ಥಿರವಾಗಿರುತ್ತದೆ.
2. - ಲಿಗಂಡ್ಗಳನ್ನು ಅವುಗಳ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆಯನ್ನು ಪಾಯಿಂಟ್ ಚಾರ್ಜ್ಗಳು ಅಥವಾ ದ್ವಿಧ್ರುವಿಗಳಾಗಿ ಪರಿಗಣಿಸದೆ ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ.
3. - ಲಿಗಂಡ್ಗಳ ವಿದ್ಯುತ್ ಕ್ಷೇತ್ರದ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ, ವೇಲೆನ್ಸಿ ಐದು ಪಟ್ಟು ಕ್ಷೀಣಿಸುತ್ತದೆ ( n -1) ಡಿ ಲಿಗಾಂಡ್ ಪರಿಸರದ ಸಮ್ಮಿತಿಯನ್ನು ಅವಲಂಬಿಸಿ ಕಕ್ಷೆಗಳನ್ನು ವಿಭಜಿಸಲಾಗಿದೆ.
4. - ವಿಭಜನೆಯ ನಡುವೆ ಲೋಹದ ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿತರಣೆ ( n -1) ಡಿ ಕಕ್ಷೆಗಳು ಸ್ಪಿನ್-ಜೋಡಿಸುವಿಕೆಯ ಶಕ್ತಿ ಮತ್ತು ವಿಭಜಿಸುವ ಶಕ್ತಿಯ ಅನುಪಾತವನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ.
ಉದಾಹರಣೆಗೆ, ಐದು ಪಟ್ಟು ಕ್ಷೀಣಗೊಳ್ಳುವ ಶಕ್ತಿಯಲ್ಲಿನ ಬದಲಾವಣೆಯನ್ನು ಪರಿಗಣಿಸಿ ( n -1) ಡಿ ಕೇಂದ್ರ ಲೋಹದ ಅಯಾನಿನ ಕಕ್ಷೆಗಳು M n+ , ಋಣಾತ್ಮಕ ಆವೇಶದ ಲಿಗಂಡ್ಗಳ ಆಕ್ಟಾಹೆಡ್ರಲ್ ಕ್ಷೇತ್ರದ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ನಿರ್ದೇಶಾಂಕಗಳ ಕೇಂದ್ರದಲ್ಲಿದೆ [ ML 6] z , ನಿರ್ದೇಶಾಂಕ ಅಕ್ಷಗಳ ಮೇಲೆ ಇದೆ (ಚಿತ್ರ 25). ಲೋಹದ ಸುತ್ತ ಋಣಾತ್ಮಕ ಆವೇಶದ ಏಕರೂಪದ ವಿತರಣೆಯೊಂದಿಗೆ ಋಣಾತ್ಮಕ ಆವೇಶದ ಲಿಗಂಡ್ಗಳಿಂದ ಲೋಹದ ವೇಲೆನ್ಸಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿಕರ್ಷಣೆಯ ಪರಿಣಾಮವಾಗಿ (ಗೋಳಾಕಾರದ ಸಮ್ಮಿತೀಯ ವಿದ್ಯುತ್ ಕ್ಷೇತ್ರ), ಎಲ್ಲಾ ಐದರ ಶಕ್ತಿಡಿ ಉಚಿತ M ಗೆ ಹೋಲಿಸಿದರೆ ಕಕ್ಷೆಗಳು E 0 ಪ್ರಮಾಣದಲ್ಲಿ ಹೆಚ್ಚಾಗುತ್ತದೆ n+ ಅಯಾನು. ಏಕೆಂದರೆ ದಿಡಿ ಕಕ್ಷೆಗಳು ವಿಭಿನ್ನ ಪ್ರಾದೇಶಿಕ ದೃಷ್ಟಿಕೋನಗಳನ್ನು ಹೊಂದಿವೆ, ನಂತರ ನಿರ್ದೇಶಾಂಕ ಅಕ್ಷಗಳ ಮೇಲೆ ಇರುವ ಲಿಗಂಡ್ಗಳ ಮೇಲೆ ನಕಾರಾತ್ಮಕ ಶುಲ್ಕಗಳ ಸಾಂದ್ರತೆಯೊಂದಿಗೆ, ಅವುಗಳ ಶಕ್ತಿಯ ಹೆಚ್ಚಳವು ಭಿನ್ನವಾಗಿರುತ್ತದೆ. ಶಕ್ತಿ ಬೂಸ್ಟ್ d z 2 ಮತ್ತು d x 2- y 2 ನಿರ್ದೇಶಾಂಕ ಅಕ್ಷಗಳ ಮೇಲಿನ ಲಿಗಂಡ್ಗಳ ಕಡೆಗೆ ನಿರ್ದೇಶಿಸಲಾದ ಕಕ್ಷೆಗಳು ಹೆಚ್ಚಿನ ಶಕ್ತಿಯ ಹೆಚ್ಚಳವನ್ನು ಹೊಂದಿರುತ್ತವೆ dxy, dxz ಮತ್ತು dyz ನಿರ್ದೇಶಾಂಕ ಅಕ್ಷಗಳ ನಡುವೆ ನಿರ್ದೇಶಿಸಲಾದ ಕಕ್ಷೆಗಳು.
ವಿದಳನದ ಶಕ್ತಿಐದು ಪಟ್ಟು ಅವನತಿಎನ್ -1) ಕಕ್ಷೆಗಳು ದ್ವಿಗುಣವಾಗಿ ಕ್ಷೀಣಗೊಳ್ಳುತ್ತವೆ d x 2- y 2, z 2 ಕಕ್ಷೆಗಳು ಮತ್ತು ಮೂರು ಬಾರಿ ಅವನತಿ d xy, xz, yz ಕಕ್ಷೆಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ (ಚಿತ್ರ 26) ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರ ವಿಭಜಿಸುವ ನಿಯತಾಂಕ.ವಿಭಜನೆಯ ಶಕ್ತಿಯಿಂದಡಿ ಗೋಳಾಕಾರದ ಸಮ್ಮಿತೀಯ ವಿದ್ಯುತ್ ಕ್ಷೇತ್ರಕ್ಕೆ ಹೋಲಿಸಿದರೆ ಲಿಗಂಡ್ಗಳ ಆಕ್ಟಾಹೆಡ್ರಲ್ ಕ್ಷೇತ್ರದಲ್ಲಿ ಕಕ್ಷೆಗಳು ಬದಲಾಗುವುದಿಲ್ಲ, ನಂತರ ಎರಡರ ಶಕ್ತಿಯ ಹೆಚ್ಚಳ d x 2- y 2, z 2 ಕಕ್ಷೆಗಳು 0.6 ರಲ್ಲಿ ಸಂಭವಿಸುತ್ತವೆಡಿ 0 ಮತ್ತು ಮೂರು ಶಕ್ತಿಯಲ್ಲಿ ಇಳಿಕೆ d xy , xz , yz ಆರ್ಬಿಟಲ್ಸ್ 0.4 ಡಿ 0 .
ಲಿಗಂಡ್ಗಳ ವಿದ್ಯುತ್ ಕ್ಷೇತ್ರದ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ವಿಭಜನೆಯಾದ ಲೋಹದ ಕಕ್ಷೆಗಳ ಅವನತಿ ಮತ್ತು ಸಮ್ಮಿತಿಯ ಮಟ್ಟವನ್ನು ಸೂಚಿಸಲು, ವಿಶೇಷ ಚಿಹ್ನೆಗಳನ್ನು ಬಳಸಲಾಗುತ್ತದೆ. ಸಮ್ಮಿತಿಯ ಕೇಂದ್ರಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ ಟ್ರಿಪಲ್ ಡಿಜೆನೆರೇಟ್ ಮತ್ತು ಸಮ್ಮಿತೀಯ ಮತ್ತು ನಿರ್ದೇಶಾಂಕ ಅಕ್ಷಗಳ ಸುತ್ತ ತಿರುಗುವಿಕೆ d xy, xz, yz t 2 ಗ್ರಾಂ ", ದ್ವಿಗುಣವಾಗಿ ಕ್ಷೀಣಿಸುವಾಗ ಮತ್ತು ಸಮ್ಮಿತಿಯ ಕೇಂದ್ರಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ ಸಮ್ಮಿತೀಯವಾಗಿದೆ d x 2- y 2, z 2 ಕಕ್ಷೆಗಳನ್ನು ಚಿಹ್ನೆಯಿಂದ ಗೊತ್ತುಪಡಿಸಲಾಗಿದೆ "ಇ ಜಿ " ಹೀಗಾಗಿ, ಲಿಗಂಡ್ಗಳ ಅಷ್ಟಹೆಡ್ರಲ್ ವಿದ್ಯುತ್ ಕ್ಷೇತ್ರದ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ, ಐದು ಪಟ್ಟು ಕ್ಷೀಣಿಸುತ್ತದೆ ( n -1) ಡಿ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಕಕ್ಷೆಗಳನ್ನು ಮೂರು ಬಾರಿ ಮತ್ತು ದ್ವಿಗುಣವಾಗಿ ಕ್ಷೀಣಿಸುವ ವಿಭಿನ್ನ ಶಕ್ತಿಗಳಾಗಿ ವಿಂಗಡಿಸಲಾಗಿದೆ t 2 g ಮತ್ತು e g ಕಕ್ಷೆಗಳು.
ಐದು ಪಟ್ಟು ಕ್ಷೀಣತೆಯ ಶಕ್ತಿಯ ಬದಲಾವಣೆಯ ಇದೇ ರೀತಿಯ ಪರಿಗಣನೆ ( n -1) ಡಿ ಲಿಗಂಡ್ಗಳ ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಪರಿಸರದಲ್ಲಿ ಮುಕ್ತ ಲೋಹದ ಅಯಾನಿನ ಕಕ್ಷೆಗಳು [ ML 4 ]z ಸಂಕೀರ್ಣಗಳು (ಚಿತ್ರ 27) ಅವುಗಳ ವಿಭಜನೆಯನ್ನು ಎರಡು ಪಟ್ಟು (ಇ) ಮತ್ತು ಮೂರು ಪಟ್ಟು ತೋರಿಸುತ್ತವೆ (ಇ)ಟಿ ) ಕ್ಷೀಣಿಸುವ ಕಕ್ಷೆಗಳು, ಆದಾಗ್ಯೂ, ವಿರುದ್ಧ ಶಕ್ತಿಯ ಸ್ಥಾನದೊಂದಿಗೆ. ಸಬ್ಸ್ಕ್ರಿಪ್ಟ್"ಜಿ "ಇ" ಮತ್ತು " ಗೊತ್ತುಪಡಿಸಿದಾಗಟಿ » ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣವು ಸಮ್ಮಿತಿಯ ಕೇಂದ್ರವನ್ನು ಹೊಂದಿಲ್ಲದ ಕಾರಣ ಕಕ್ಷೆಗಳನ್ನು ಸೂಚಿಸಲಾಗುವುದಿಲ್ಲ. ಆಕ್ಟಾಹೆಡ್ರಲ್ ಕಾಂಪ್ಲೆಕ್ಸ್ಗೆ ಹೋಲಿಸಿದರೆ ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಕಾಂಪ್ಲೆಕ್ಸ್ನ ಲಿಗಂಡ್ಗಳ ಸಂಖ್ಯೆಯಲ್ಲಿನ ಇಳಿಕೆಯು ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದ ವಿಭಜನೆಯ ನಿಯತಾಂಕದಲ್ಲಿ ನೈಸರ್ಗಿಕ ಇಳಿಕೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ:ಡಿಟಿ = 4/9 ಡಿಸುಮಾರು .
ಲೋಹದ ಲಿಗಂಡ್ ಪರಿಸರದ ಸಮ್ಮಿತಿಯನ್ನು ಕಡಿಮೆ ಮಾಡುವುದು, ಉದಾಹರಣೆಗೆ, ಅಷ್ಟಹೆಡ್ರಲ್ನ ಚತುರ್ಭುಜ ಅಸ್ಪಷ್ಟತೆ [ ML 6] z ಅಕ್ಷೀಯ ಲಿಗಂಡ್ಗಳೊಂದಿಗೆ ಲೋಹದ-ಲಿಗಂಡ್ ಬಂಧಗಳ ವಿಸ್ತರಣೆಗೆ ಸಂಬಂಧಿಸಿದ ಸಂಕೀರ್ಣಗಳು [ ML 4 X 2 ] z ಮತ್ತು ಪ್ಲೇನ್-ಸ್ಕ್ವೇರ್ನ ಸೀಮಿತಗೊಳಿಸುವ ಸಂದರ್ಭದಲ್ಲಿ ರಚನೆ [ ML 4 ]z ಸಂಕೀರ್ಣಗಳು, ಲೀಡ್ಸ್ (ಚಿತ್ರ 28) ವೇಲೆನ್ಸಿಯ ಹೆಚ್ಚುವರಿ ವಿಭಜನೆಗೆ ( n -1) ಡಿ ಲೋಹದ ಕಕ್ಷೆಗಳು.
ವಿಭಜನೆಯನ್ನು ತುಂಬುವುದು ( n -1) ಡಿ ಲೋಹದ ಕಕ್ಷೆಗಳು ಪೌಲಿ ತತ್ವಗಳು ಮತ್ತು ಕನಿಷ್ಠ ಶಕ್ತಿಗೆ ಅನುಗುಣವಾಗಿ ಸಂಭವಿಸುತ್ತವೆ. ಜೊತೆಗೆ ಆಕ್ಟಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳಿಗೆ d 1, d 2 ಮತ್ತು d 3 ಲೋಹದ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸಂರಚನೆ, ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು, ಹಂಡ್ನ ನಿಯಮಕ್ಕೆ ಅನುಗುಣವಾಗಿ, ಜನಪ್ರಿಯಗೊಳಿಸುತ್ತವೆಟಿ 2 ಗ್ರಾಂ ಸಮಾನಾಂತರ ಸ್ಪಿನ್ಗಳೊಂದಿಗೆ ಕಕ್ಷೆಗಳು, ಕಾರಣವಾಗುತ್ತದೆ t 2 g 1, t 2 g 2 ಮತ್ತು t 2 g 3 ಸಂಕೀರ್ಣಗಳ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆ.
ಡಿ 4 ಹೊಂದಿರುವ ಲೋಹಗಳಿಗೆ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಕಾನ್ಫಿಗರೇಶನ್, ಮೂರು ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಸಹ ಜನಪ್ರಿಯವಾಗಿವೆಟಿ 2 ಗ್ರಾಂ ಸಮಾನಾಂತರ ಸ್ಪಿನ್ಗಳೊಂದಿಗೆ ಕಕ್ಷೆಗಳು. ನಾಲ್ಕನೇ ಎಲೆಕ್ಟ್ರಾನ್ನ ಜನಸಂಖ್ಯೆಯು ಜನಸಂಖ್ಯೆಯ ಸಮಯದಲ್ಲಿ ಸ್ಪಿನ್ ಪೇರಿಂಗ್ ಎನರ್ಜಿ (E sp.-sp.) ಮೌಲ್ಯದ ಶಕ್ತಿಯ ವೆಚ್ಚವನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ.ಟಿ 2 ಗ್ರಾಂ ಆಂಟಿಪ್ಯಾರಲಲ್ ಸ್ಪಿನ್ ಮತ್ತು ಹಂಡ್ ನಿಯಮದ ಉಲ್ಲಂಘನೆಯೊಂದಿಗೆ ಕಕ್ಷೆಗಳು, ಅಥವಾ ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದಿಂದ ವಿಭಜಿಸುವ ಶಕ್ತಿಯನ್ನು ಮೀರಿಸುವುದುಡಿ o ಚೆಕ್-ಇನ್ ಆದ ಮೇಲೆ g ಹಂಡ್ ನಿಯಮಕ್ಕೆ ಅನುಗುಣವಾಗಿ ಸಮಾನಾಂತರ ಸ್ಪಿನ್ ಹೊಂದಿರುವ ಕಕ್ಷೆಗಳು. ಮೊದಲ ಸಂದರ್ಭದಲ್ಲಿ, ಒಂದು ಸಂಕೀರ್ಣವು ರಚನೆಯಾಗುತ್ತದೆಟಿ 2 ಗ್ರಾಂ 4 ಉಚಿತ ಲೋಹ 2 ಕ್ಕೆ ಹೋಲಿಸಿದರೆ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆ ಮತ್ತು ಕಡಿಮೆ ಸ್ಪಿನ್ ಮಲ್ಟಿಪ್ಲಿಸಿಟಿಎಸ್ +1 = 3 (ಎಸ್ - ಒಟ್ಟು ಸ್ಪಿನ್), ಕರೆಯಲಾಗುತ್ತದೆ ಕಡಿಮೆ ಸ್ಪಿನ್. ಹಂಡ್ನ ನಿಯಮವನ್ನು ಪೂರೈಸಿದಾಗ ಮತ್ತು ನಾಲ್ಕನೇ ಎಲೆಕ್ಟ್ರಾನ್ನಲ್ಲಿ ಜನಸಂಖ್ಯೆಯುಂಟಾಗುತ್ತದೆಇ ಜಿ ಕಕ್ಷೆಗಳು, ಒಂದು ಸಂಕೀರ್ಣವು ರಚನೆಯಾಗುತ್ತದೆ t 2 g 3 e g 1 ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆ ಮತ್ತು ಉಚಿತ ಲೋಹದಂತಹ ಸ್ಪಿನ್ ಮಲ್ಟಿಪ್ಲೆಟ್ 2ಎಸ್ +1 = 5. ಅಂತಹ ಸಂಕೀರ್ಣಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ಹೆಚ್ಚಿನ ಸ್ಪಿನ್.
ಅಂತೆಯೇ, ವೇಲೆನ್ಸ್ ಅನ್ನು ವಿತರಿಸುವಾಗ d5, d6 ಮತ್ತು d7 ಲೋಹದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳುಟಿ 2 ಗ್ರಾಂ ಮತ್ತು ಇ ಜಿ E sp.-sp ಅನುಪಾತವನ್ನು ಅವಲಂಬಿಸಿ ಆಕ್ಟಾಡ್ರಿಕ್ ಸಂಕೀರ್ಣಗಳ ಕಕ್ಷೆಗಳು. ಮತ್ತುಡಿಓ ಎರಡು ರೀತಿಯ ಸಂಕೀರ್ಣಗಳ ರಚನೆಯು ಸಾಧ್ಯ:
E sp.-sp ನಲ್ಲಿ. > ಡಿಓ ಲೋಹದ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆಯೊಂದಿಗೆ ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ t 2 g 3 e g 2, t 2 g 4 e g 2, t 2 g 5 e g 2 ಹಂಡ್ನ ನಿಯಮ ಮತ್ತು ಉಚಿತ ಲೋಹದಂತಹ ಸ್ಪಿನ್ ಮಲ್ಟಿಪ್ಲಿಸಿಟಿ ಪ್ರಕಾರ - 2ಎಸ್ +1 = 6, 5, 4;
E sp.-sp.< ಡಿಓ ಲೋಹದ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆಯೊಂದಿಗೆ ಕಡಿಮೆ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ t 2 g 5 e g 0 , t 2 g 6 e g 0 , t 2 g 6 e g 1 ಮತ್ತು ಉಚಿತ ಮೆಟಲ್ 2 ಗೆ ಹೋಲಿಸಿದರೆ ಕಡಿಮೆ ಸ್ಪಿನ್ ಮಲ್ಟಿಪ್ಲಿಸಿಟಿ S +1 = 2, 1, 2.
ಜೊತೆ ಲೋಹದ ಸಂಕೀರ್ಣಗಳು d 8, d 9 ಮತ್ತು d 10 ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸಂರಚನೆಯನ್ನು ಒಂದು ರೀತಿಯ ಎಲೆಕ್ಟ್ರಾನ್ ವಿತರಣೆಯಿಂದ ನಿರೂಪಿಸಲಾಗಿದೆ - t 2 g 6 e g 2, t 2 g 6 e g 3, t 2 g 6 e g 4 ಉಚಿತ ಲೋಹದಂತೆಯೇ ಸ್ಪಿನ್ ಬಹುಸಂಖ್ಯೆಯೊಂದಿಗೆ: 2 S +1 = 3, 2 ಮತ್ತು 0.
ಆದ್ದರಿಂದ ನಿಯತಾಂಕಡಿ, ವಿಭಜನೆಯನ್ನು ನಿರೂಪಿಸುವುದು ( n -1) ಡಿ ಲಿಗಂಡ್ಗಳ ವಿದ್ಯುತ್ ಕ್ಷೇತ್ರದ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ಲೋಹದ ಕಕ್ಷೆಗಳು ಉಚಿತ ಲೋಹದ ಅಯಾನುಗಳಿಗೆ ಹೋಲಿಸಿದರೆ ಸಂಕೀರ್ಣಗಳ ಗುಣಲಕ್ಷಣಗಳಲ್ಲಿನ ಬದಲಾವಣೆಗಳ ಮುಖ್ಯ ಗುಣಲಕ್ಷಣಗಳಲ್ಲಿ ಒಂದಾಗಿದೆ. ಇದು ಪ್ಯಾರಾಮೀಟರ್ ಮೌಲ್ಯವಾಗಿದೆಡಿಲೋಹದ ಹಲವಾರು ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸಂರಚನೆಗಳನ್ನು ನಿರ್ಧರಿಸುತ್ತದೆ ವಿಭಜಿತ ಕಕ್ಷೆಗಳು ಮತ್ತು ವಿಭಿನ್ನ ಗುಣಲಕ್ಷಣಗಳ ಮೇಲೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿಭಿನ್ನ ವಿತರಣೆಗಳೊಂದಿಗೆ ಹೆಚ್ಚಿನ ಅಥವಾ ಕಡಿಮೆ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳ ರಚನೆಯ ಸಾಧ್ಯತೆಯನ್ನು ನಿರ್ಧರಿಸುತ್ತದೆ.
ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದ ವಿಭಜಿಸುವ ನಿಯತಾಂಕದ ಮೌಲ್ಯಡಿಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಲೋಹದ ಸ್ವರೂಪ, ಅದರ ಸುತ್ತಲಿನ ಲಿಗಂಡ್ಗಳು ಮತ್ತು ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಸುತ್ತಲಿನ ಅವುಗಳ ಪ್ರಾದೇಶಿಕ ಸ್ಥಾನವನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ:
1. ಪ್ಯಾರಾಮೀಟರ್ ಅನ್ನು ಹೆಚ್ಚಿಸುವ ಕ್ರಮದಲ್ಲಿ ಲಿಗಂಡ್ಗಳುಡಿಒಂದೇ ಲೋಹದ ಸಂಕೀರ್ಣಗಳು ಮತ್ತು ಒಂದೇ ರೀತಿಯ ಜ್ಯಾಮಿತೀಯ ರಚನೆಯು ಸ್ಪೆಕ್ಟ್ರೋಕೆಮಿಕಲ್ ಸರಣಿ ಎಂದು ಕರೆಯಲ್ಪಡುತ್ತದೆ:ನಾನು -< Br - < Cl - < F - < OH - < C 2 O 4 2- ~ H 2 O < NCS - < NH 3 ~ En < NO 2 - < CN - < CO . ಸಾಲಿನ ಆರಂಭದಲ್ಲಿ “ದುರ್ಬಲ ಕ್ಷೇತ್ರ” ಲಿಗಂಡ್ಗಳಿವೆ - ಹಾಲೈಡ್ ಅಯಾನುಗಳು, ಹೈಡ್ರಾಕ್ಸೈಡ್ ಮತ್ತು ಆಕ್ಸಲೇಟ್ ಅಯಾನುಗಳು, ನೀರು, ಇದು ಪ್ರಧಾನವಾಗಿ ಹೈ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳನ್ನು ರೂಪಿಸುತ್ತದೆ. ಸರಣಿಯ ಬಲಭಾಗದಲ್ಲಿರುವ ಲಿಗಂಡ್ಗಳು: ಕಾರ್ಬನ್ ಮಾನಾಕ್ಸೈಡ್, ಸೈನೈಡ್ ಮತ್ತು ನೈಟ್ರೈಟ್ ಅಯಾನುಗಳನ್ನು "ಹೈ ಫೀಲ್ಡ್" ಲಿಗಂಡ್ಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ ಮತ್ತು ಕಡಿಮೆ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳ ರಚನೆಯಿಂದ ವಿಶಿಷ್ಟವಾಗಿ ನಿರೂಪಿಸಲ್ಪಡುತ್ತವೆ. ಸರಣಿಯ ಮಧ್ಯದಲ್ಲಿರುವ ಲಿಗಂಡ್ಗಳಿಗೆ - ಥಿಯೋಸೈನೇಟ್ ಅಯಾನು, ಅಮೋನಿಯಾ, ಎಥಿಲೆನೆಡಿಯಮೈನ್, ಲೋಹದ ಸ್ವರೂಪವನ್ನು ಅವಲಂಬಿಸಿ, ಹೆಚ್ಚಿನ ಅಥವಾ ಕಡಿಮೆ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ.
2. ಲಿಗಂಡ್ಗಳ ವಿದ್ಯುತ್ ಕ್ಷೇತ್ರದ ದಕ್ಷತೆಯನ್ನು ಹೆಚ್ಚಿಸುವುದುಡಿ ಲೋಹದ ಕಕ್ಷೆಗಳು ಅವುಗಳ ಗಾತ್ರವನ್ನು ಸಾಲು 3 ರಲ್ಲಿ ಹೆಚ್ಚಿಸುತ್ತವೆಡಿ<< 4 d < 5 d , ಹಾಗೆಯೇ ಲೋಹದ ಆಕ್ಸಿಡೀಕರಣದ ಮಟ್ಟದಲ್ಲಿ ಹೆಚ್ಚಳವು ನಿಯತಾಂಕದ ಹೆಚ್ಚಳಕ್ಕೆ ಕಾರಣವಾಗುತ್ತದೆಡಿಸರಣಿಯಲ್ಲಿ: Mn(II)< Ni (II ) < Co (II ) < Fe (II ) < V (II ) < Fe (III ) < Co (III ) < Mn (IV ) < Mo (III ) < Rh (III ) < Ru (III ) < Pd (IV ) < Ir (III ) < Pt (IV ).
3. ಪ್ಯಾರಾಮೀಟರ್ ಡಿಟೆಟ್ರಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳಿಗೆ ನಿಯತಾಂಕದ 4/9 ಮಾತ್ರಡಿಅಷ್ಟಮುಖ ಸಂಕೀರ್ಣಗಳು.
"ಭಾರೀ" ಸಂಕೀರ್ಣಗಳು 4ಡಿ ಮತ್ತು 5 ಡಿ ಲೋಹಗಳು, ಲಿಗಂಡ್ಗಳ ಸ್ವರೂಪವನ್ನು ಲೆಕ್ಕಿಸದೆ, ಪ್ರಧಾನವಾಗಿ ಕಡಿಮೆ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳನ್ನು ರೂಪಿಸುತ್ತವೆ, ಆದರೆ ಕಡಿಮೆ- ಅಥವಾ ಹೆಚ್ಚಿನ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳ ರಚನೆಯು "ಬೆಳಕು" 3ಡಿ ಲೋಹಗಳನ್ನು ಮುಖ್ಯವಾಗಿ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರದ ಬಲದಿಂದ ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ.
MMS ಗೆ ವ್ಯತಿರಿಕ್ತವಾಗಿ, ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರ ಸಿದ್ಧಾಂತವು ವಿಭಿನ್ನ ಲಿಗಂಡ್ ಪರಿಸರಗಳೊಂದಿಗೆ ಒಂದೇ ಲೋಹದ ಅಯಾನಿನ ಸಂಕೀರ್ಣಗಳ ಕಾಂತೀಯ ಗುಣಲಕ್ಷಣಗಳಲ್ಲಿನ ವ್ಯತ್ಯಾಸವನ್ನು ಸಮರ್ಥಿಸುತ್ತದೆ, ಉದಾಹರಣೆಗೆ, ಡಯಾಮ್ಯಾಗ್ನೆಟಿಕ್ [ಫೆ(ಸಿಎನ್ ) 6 ] 4- ಮತ್ತು ಪ್ಯಾರಾಮ್ಯಾಗ್ನೆಟಿಕ್ [ಫೆ(H2O ) 6 ] 2+ ತಮ್ಮ ಇಂಟ್ರಾರ್ಬಿಟಲ್ನ ಊಹೆಯನ್ನು ಬಳಸುವುದಿಲ್ಲ (ಡಿ 2 ಎಸ್ಪಿ 3 ಹೈಬ್ರಿಡೈಸೇಶನ್) ಮತ್ತು ಹೊರ-ಕಕ್ಷೀಯ (ಎಸ್ಪಿ 3 ಡಿ 2 ಹೈಬ್ರಿಡೈಸೇಶನ್) ರಚನೆ. ಕಾಂತೀಯ ಗುಣಲಕ್ಷಣಗಳಲ್ಲಿನ ವ್ಯತ್ಯಾಸವನ್ನು 6-ವ್ಯಾಲೆಂಟ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿತರಣೆಯ ಕಡಿಮೆ ಮತ್ತು ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ ಸ್ವಭಾವದಿಂದ ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆಫೆ(II ) ವಿಭಜನೆಯಿಂದಟಿ 2 ಗ್ರಾಂ ಮತ್ತು ಇ ಜಿ ಕಕ್ಷೆಗಳು (ಚಿತ್ರ 29). ಬಲವಾದ ಮತ್ತು ದುರ್ಬಲ ಕ್ಷೇತ್ರ ಲಿಗಂಡ್ಗಳು, ಸೈನೈಡ್ ಅಯಾನುಗಳು ಮತ್ತು ನೀರಿನ ಅಣುಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆಫೆ(II ) ಜೊತೆಗೆ ಕಡಿಮೆ ಮತ್ತು ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳು t 2 g 6 e g 0 ಮತ್ತು t 2 g 4 e g 2 ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿತರಣೆ, ಇದು ಡಯಾಮ್ಯಾಗ್ನೆಟಿಸಮ್ ಅನ್ನು ನಿರ್ಧರಿಸುತ್ತದೆ [ಫೆ(ಸಿಎನ್ ) 6 ] 4- ಮತ್ತು ಪ್ಯಾರಾಮ್ಯಾಗ್ನೆಟಿಸಂ [ಫೆ(H2O 6 ] 2+ ಸಂಕೀರ್ಣಗಳು.
ಐದು ಪಟ್ಟು ಕ್ಷೀಣತೆಯ ವಿಭಜನೆ ( n -1) ಡಿ ಸಂಕೀರ್ಣಗಳು ಮತ್ತು ನಿಯತಾಂಕ ಬದಲಾವಣೆಗಳಲ್ಲಿ ಲೋಹದ ಕಕ್ಷೆಗಳುಡಿಲಿಗಂಡ್ಗಳ ಸ್ವರೂಪವನ್ನು ಅವಲಂಬಿಸಿ, ಘನ ಸ್ಥಿತಿಯಲ್ಲಿ ಮತ್ತು ದ್ರಾವಣಗಳಲ್ಲಿ ಸಂಕೀರ್ಣಗಳ ವಿಶಿಷ್ಟ ಬಣ್ಣವನ್ನು ಇದು ನಿರ್ಧರಿಸುತ್ತದೆ. ಸಂಕೀರ್ಣವು ಸ್ಪೆಕ್ಟ್ರಮ್ (400-750) nm ನ ಗೋಚರ ಪ್ರದೇಶದಲ್ಲಿ ವಿದ್ಯುತ್ಕಾಂತೀಯ ವಿಕಿರಣವನ್ನು ಹೀರಿಕೊಳ್ಳುವಾಗ, ಅದರ ಕ್ವಾಂಟಾದ ಶಕ್ತಿಯು Eಮೌಲ್ಯಕ್ಕೆ ಸಮಾನವಾಗಿರುತ್ತದೆ ಡಿ, ಎಲೆಕ್ಟ್ರಾನ್ ವರ್ಗಾವಣೆ ಸಂಭವಿಸುತ್ತದೆಇ ಜಿ ಮೇಲೆ ಟಿ 2 ಗ್ರಾಂ ಕಕ್ಷೆಗಳು. ಇದು ವರ್ಣಪಟಲದ ಗೋಚರ ಪ್ರದೇಶದ ಹೀರಿಕೊಳ್ಳದ ವಿದ್ಯುತ್ಕಾಂತೀಯ ವಿಕಿರಣವಾಗಿದ್ದು, ಗೋಚರ ವಿಕಿರಣದ ಪ್ರಾಥಮಿಕ ಮತ್ತು ದ್ವಿತೀಯಕ ಬಣ್ಣಗಳನ್ನು ತೋರಿಸುವ "ನ್ಯೂಟನ್ನ ಬಣ್ಣದ ವೃತ್ತ" (ಚಿತ್ರ 30) ಗೆ ಅನುಗುಣವಾಗಿ ಸಂಕೀರ್ಣದ ಬಣ್ಣವನ್ನು ನಿರ್ಧರಿಸುತ್ತದೆ.
ಅಕ್ವಾಕಾಂಪ್ಲೆಕ್ಸ್ ಟೈಟಾನಿಯಂ( III) [Ti (H 2 O) 6] 3+ c t 2 g 1 e g 0 ಫೋಟೊಎಕ್ಸಿಟೇಶನ್ ಪರಿಣಾಮವಾಗಿ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ವಿತರಣೆ, ಎಲೆಕ್ಟ್ರಾನ್ ಅನ್ನು ಹೆಚ್ಚಿನ ಶಕ್ತಿಗೆ ಪರಿವರ್ತನೆಗೆ ಅನುಗುಣವಾಗಿರುತ್ತದೆಇ ಜಿ ಕಕ್ಷೆಗಳು:
3+ (t 2g 1 e g 0) + hಎನ್= * 3+ (t 2g 0 e g 1)
ವರ್ಣಪಟಲದ ಹಳದಿ ಪ್ರದೇಶದಲ್ಲಿ ಬೆಳಕಿನ ಕ್ವಾಂಟಾವನ್ನು ಹೀರಿಕೊಳ್ಳುತ್ತದೆ, ಇದು ಅದರ ನೇರಳೆ ಬಣ್ಣಕ್ಕೆ ಕಾರಣವಾಗುತ್ತದೆ. ಸ್ಪೆಕ್ಟ್ರೋಕೆಮಿಕಲ್ ಸರಣಿಯಲ್ಲಿನ ಲಿಗಂಡ್ನ ಸ್ಥಾನಕ್ಕೆ ಅನುಗುಣವಾಗಿ ಲೋಹದ ಅಯಾನಿನ ಲಿಗಂಡ್ ಪರಿಸರದಲ್ಲಿನ ಬದಲಾವಣೆಯು ನಿಯತಾಂಕದಲ್ಲಿನ ಬದಲಾವಣೆಗೆ ಕಾರಣವಾಗುತ್ತದೆಡಿಮತ್ತು ಇದರ ಪರಿಣಾಮವಾಗಿ, ಸಂಕೀರ್ಣದಿಂದ ಹೀರಿಕೊಳ್ಳಲ್ಪಟ್ಟ ಕ್ವಾಂಟಾದ ಶಕ್ತಿ ಮತ್ತು ತರಂಗಾಂತರದ ಬದಲಾವಣೆಗೆ ಮತ್ತು ಸಂಕೀರ್ಣದ ವಿಶಿಷ್ಟ ಬಣ್ಣಕ್ಕೆ - ಉದಾಹರಣೆಗೆ, ಸರಣಿಯಲ್ಲಿ [ CuCl 4 ] 2- , [ Cu (H 2 O ) 4 ] 2+ , [ Cu (NH 3 ) 4 ] 2+ ಸಂಕೀರ್ಣಗಳ ಬಣ್ಣವು ಹಸಿರು ಬಣ್ಣದಿಂದ ನೀಲಿ ಮತ್ತು ನೇರಳೆ ಬಣ್ಣಕ್ಕೆ ಬದಲಾಗುತ್ತದೆ.
ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದ ವಿಭಜಿಸುವ ಶಕ್ತಿಯ ಜೊತೆಗೆಡಿ, TCH ನಲ್ಲಿ ಸಹ ಪ್ರಮುಖ ಪಾತ್ರ ವಹಿಸುತ್ತದೆ ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದ ಸ್ಥಿರೀಕರಣ ಶಕ್ತಿ(ESKP) - ಸಂಕೀರ್ಣದಲ್ಲಿ ವಿಭಜನೆಯಾದವರಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ವಿತರಿಸುವಾಗ ಶಕ್ತಿಯನ್ನು ಪಡೆಯುವುದು ( n -1) ಡಿ ಐದು ಪಟ್ಟು ಕ್ಷೀಣಗೊಳ್ಳುವ ಶಕ್ತಿಗೆ ಹೋಲಿಸಿದರೆ ಲೋಹದ ಕಕ್ಷೆಗಳು ( n -1) ಡಿ ಸಮಾನವಾದ ಗೋಲಾಕಾರದ ವಿದ್ಯುತ್ ಕ್ಷೇತ್ರದಲ್ಲಿ ಲೋಹದ ಕಕ್ಷೆಗಳು (ಚಿತ್ರ 31, 32).
ಆಕ್ಟಾಡ್ರಲ್ ಮತ್ತು ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳ ESCP.|
Mn+ |
ಆಕ್ಟಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳು |
ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳು |
|
|
ಕಡಿಮೆ ಸ್ಪಿನ್ |
ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ |
ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ |
|
|
0.4 ಡಿ o |
0.6 ಡಿಟಿ |
||
|
0.8 ಡಿ o |
1.2 ಡಿಟಿ |
||
|
1.2 ಡಿ o |
0.8 ಡಿಟಿ |
||
|
d 4 |
1.6 ಡಿ o |
0.6 ಡಿ o |
0.4 ಡಿಟಿ |
|
d 5 |
2.0 ಡಿ o |
0 ಡಿ o |
0 ಡಿಟಿ |
|
d 6 |
2.4 ಡಿ o |
0.4 ಡಿ o |
0.6 ಡಿಟಿ |
|
d 7 |
1.8 ಡಿ o |
0.8 ಡಿ o |
1.2 ಡಿಟಿ |
|
d 8 |
1.2 ಡಿ o |
0.8 ಡಿಟಿ |
|
|
d 9 |
0.6 ಡಿ o |
0.4 ಡಿಟಿ |
|
|
d 10 |
0 ಡಿ o |
||
ವಿಭಜಿಸುವ ರೇಖಾಚಿತ್ರಗಳ ಆಧಾರದ ಮೇಲೆ ಸಂಕೀರ್ಣದ EXP ಮೌಲ್ಯದ ಅಂದಾಜು ಪಡೆಯಲಾಗಿದೆ ( n -1) ಡಿ ಲಿಗಂಡ್ಗಳ ವಿದ್ಯುತ್ ಕ್ಷೇತ್ರದಲ್ಲಿ ಲೋಹದ ಕಕ್ಷೆಗಳು, ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ವಿಭಜನೆಯಾದಾಗ ಗೋಳಾಕಾರದ ವಿದ್ಯುತ್ ಕ್ಷೇತ್ರಕ್ಕೆ ಹೋಲಿಸಿದರೆ ವ್ಯವಸ್ಥೆಯ ಶಕ್ತಿಯಲ್ಲಿ ಇಳಿಕೆ ಅಥವಾ ಹೆಚ್ಚಳವನ್ನು ತೋರಿಸುತ್ತದೆ ( n -1) ಡಿ ಕಕ್ಷೆಗಳು. ಅಷ್ಟಮುಖಕ್ಕಾಗಿ [ ML 6] z ಸಂಕೀರ್ಣಗಳು (ಚಿತ್ರ 32) ಪ್ರತಿ ಎಲೆಕ್ಟ್ರಾನ್ ಜನಸಂಖ್ಯೆಟಿ 2 ಗ್ರಾಂ ಆರ್ಬಿಟಲ್ಸ್ ಸಿಸ್ಟಮ್ ಶಕ್ತಿಯಲ್ಲಿ 0.4 ರಷ್ಟು ಲಾಭಕ್ಕೆ ಕಾರಣವಾಗುತ್ತದೆಡಿಓಹ್, ಚೆಕ್-ಇನ್ ಉದಾ ಶಕ್ತಿಯ ವೆಚ್ಚದ ಅಗತ್ಯವಿದೆ 0.6ಡಿಓ . ಟೆಟ್ರಾಹೆಡ್ರಲ್ಗಾಗಿ [ ML 4 ]z ವಿರುದ್ಧ ಶಕ್ತಿಯ ಸ್ಥಾನಗಳೊಂದಿಗೆ ಸಂಕೀರ್ಣಗಳುಇ ಮತ್ತು ಟಿ ಲೋಹದ ಕಕ್ಷೆಗಳು - ವಿಭಜನೆಯ ಮೂಲಕ ಪ್ರತಿ ಎಲೆಕ್ಟ್ರಾನ್ನ ಉದ್ಯೋಗಇ ಮತ್ತು ಟಿ ಆರ್ಬಿಟಲ್ಸ್ ಸಿಸ್ಟಮ್ನ ಶಕ್ತಿಯಲ್ಲಿ 0.6 ರಷ್ಟು ಇಳಿಕೆ ಮತ್ತು ಹೆಚ್ಚಳದೊಂದಿಗೆ ಇರುತ್ತದೆಡಿಟಿ ಮತ್ತು 0.4 ಡಿಟಿ .
ಸಂಕೀರ್ಣಗಳ ಥರ್ಮೋಡೈನಾಮಿಕ್ ಸ್ಥಿರತೆಯ ಪ್ರತಿಬಿಂಬವಾಗಿರುವುದರಿಂದ, ಅವುಗಳ ESCR ಮೌಲ್ಯಗಳ ಅಂದಾಜುಗಳು ಹೈ-ಸ್ಪಿನ್ ಹೆಕ್ಸಾಫ್ಲೋರೈಡ್ ಸಂಕೀರ್ಣಗಳಿಗೆ ಸ್ಫಟಿಕ ಲ್ಯಾಟಿಸ್ನ ಶಕ್ತಿಯಲ್ಲಿನ ಬದಲಾವಣೆಗಳ ಪ್ರಾಯೋಗಿಕ ಡೇಟಾದೊಂದಿಗೆ ಸ್ಥಿರವಾಗಿರುತ್ತವೆ 3ಡಿ ಲೋಹಗಳು (ಚಿತ್ರ 33).
ESC ಮೌಲ್ಯಗಳು ನಮಗೆ ಹೆಚ್ಚು ಆದ್ಯತೆಯ ಸಮನ್ವಯ ಐಸೋಮರ್ ಅನ್ನು ನಿರ್ಧರಿಸಲು ಅನುಮತಿಸುತ್ತದೆ (ಚಿತ್ರ 34), ಉದಾಹರಣೆಗೆ [ Cu (NH 3 ) 6 ][ NiCl 4 ] ಅಥವಾ [ Ni (NH 3 ) 6 ][ CuCl 4 ]. ಇದನ್ನು ಮಾಡಲು, ಐಸೋಮರ್ಗಳ ಸಂಕೀರ್ಣ ಕ್ಯಾಷನ್ ಮತ್ತು ಅಯಾನ್ಗೆ ESC ಯಲ್ಲಿನ ವ್ಯತ್ಯಾಸವನ್ನು ಲೆಕ್ಕಹಾಕಿ. ESCR ಮೌಲ್ಯ [ Cu (NH 3 ) 6 ] 2+ ಮತ್ತು [NiCl 4 ] 2- 0.6 ಡಿ o ಮತ್ತು 0.8 ಡಿಟಿ ಕ್ರಮವಾಗಿ. ಅದನ್ನು ಪರಿಗಣಿಸಿಡಿ t = 4/9 ಡಿ o , ESCP ಮೌಲ್ಯಗಳ ನಡುವಿನ ವ್ಯತ್ಯಾಸ [ Cu (NH 3 ) 6 ] 2+ ಮತ್ತು [NiCl 4 ] 2- 19/45 ಆಗಿರುತ್ತದೆಡಿ o . ಅಂತೆಯೇ, ESKP ಯ ಮೌಲ್ಯಗಳು [ನಿ (NH 3) 6 ] 2+ ಮತ್ತು [CuCl 4 ] 2- 1.2 ಡಿ o ಮತ್ತು 0.4 ಡಿಟಿ , ಮತ್ತು ಅವುಗಳ ನಡುವಿನ ವ್ಯತ್ಯಾಸವು 28/45 ಆಗಿದೆಡಿ o . ದೊಡ್ಡ ವ್ಯತ್ಯಾಸ ESCP ಸಂಕೀರ್ಣ ಕ್ಯಾಷನ್ [ Ni (NH 3 ) 6 ] 2+ ಮತ್ತು ಅಯಾನು [CuCl 4 ] 2- ಗೆ ಹೋಲಿಸಿದರೆ [ Cu (NH 3 ) 6 ] 2+ ಮತ್ತು [NiCl 4 2- ಸಂಯೋಜನೆಯ ಐಸೋಮರ್ನ ಹೆಚ್ಚು ಆದ್ಯತೆಯ ರಚನೆಯನ್ನು ತೋರಿಸುತ್ತದೆ [ನಿ (NH 3) 6 ][ CuCl 4 ].
ಸಂಕೀರ್ಣಗಳ ಥರ್ಮೋಡೈನಾಮಿಕ್ ಸ್ಥಿರತೆಯ ಮೇಲೆ ಲೋಹದ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆಯ ಪ್ರಭಾವದ ಕಾಂತೀಯ ಮತ್ತು ಆಪ್ಟಿಕಲ್ ಗುಣಲಕ್ಷಣಗಳ ಜೊತೆಗೆ, TKP ವಿಭಜಿತ ಮೇಲೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಅಸಮ ವಿತರಣೆಯೊಂದಿಗೆ ಸಂಕೀರ್ಣಗಳ ಜ್ಯಾಮಿತೀಯ ರಚನೆಯ ಅಸ್ಪಷ್ಟತೆಯನ್ನು ಮುನ್ಸೂಚಿಸುತ್ತದೆ ( n -1) ಡಿ ಲೋಹದ ಕಕ್ಷೆಗಳು (ಚಿತ್ರ 35). ನಿಯಮಿತ ಆಕ್ಟಾಹೆಡ್ರಲ್ ರಚನೆಗೆ ವ್ಯತಿರಿಕ್ತವಾಗಿ [ Co (CN) 6 ] 3- s t 2 g 6 e g 0 ಎಲೆಕ್ಟ್ರಾನಿಕ್ ವಿತರಣೆ, ಇದೇ ರೀತಿಯ ಸಂಕೀರ್ಣದ ಚತುರ್ಭುಜ ಅಸ್ಪಷ್ಟತೆ [ Cu (CN) 6 ] 4- s t 2 g 6 e g 3 2-ಪಟ್ಟು ಕ್ಷೀಣಗೊಳ್ಳುವ ಮೇಲೆ 3 ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ವಿತರಣೆಇ ಜಿ ಕಕ್ಷೆಗಳು, ಆಕ್ಟಾಹೆಡ್ರಲ್ ಅನ್ನು ಚದರ-ಪ್ಲಾನರ್ ಸಂಕೀರ್ಣವಾಗಿ ಪರಿಣಾಮಕಾರಿಯಾಗಿ ಪರಿವರ್ತಿಸಲು ಕಾರಣವಾಗುತ್ತದೆ:
4- = 2- + 2CN - .
ಸಂಕೀರ್ಣಗಳ ಭೌತರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳನ್ನು ವಿವರಿಸಲು ಮತ್ತು ಊಹಿಸಲು TCT ಯ ಸಾಪೇಕ್ಷ ಸರಳತೆ ಮತ್ತು ವಿಶಾಲ ಸಾಮರ್ಥ್ಯಗಳು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ರಾಸಾಯನಿಕ ಬಂಧಗಳನ್ನು ವಿವರಿಸಲು ಈ ಮಾದರಿಯ ದೊಡ್ಡ ಜನಪ್ರಿಯತೆಯನ್ನು ನಿರ್ಧರಿಸುತ್ತದೆ ಎಂದು ಮೇಲಿನ ಎಲ್ಲಾ ತೋರಿಸುತ್ತದೆ. ಅದೇ ಸಮಯದಲ್ಲಿ, ಸಂಕೀರ್ಣ ರಚನೆಯ ಸಮಯದಲ್ಲಿ ಲೋಹದ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆಯಲ್ಲಿನ ಬದಲಾವಣೆಗಳ ಮೇಲೆ ಕೇಂದ್ರೀಕರಿಸುವುದು, TCP ಲಿಗಂಡ್ಗಳ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆಯನ್ನು ಗಣನೆಗೆ ತೆಗೆದುಕೊಳ್ಳುವುದಿಲ್ಲ, ಅವುಗಳನ್ನು ಪಾಯಿಂಟ್ ಋಣಾತ್ಮಕ ಶುಲ್ಕಗಳು ಅಥವಾ ದ್ವಿಧ್ರುವಿಗಳಾಗಿ ಪರಿಗಣಿಸುತ್ತದೆ. ಸಂಕೀರ್ಣಗಳ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆಯನ್ನು ವಿವರಿಸುವಾಗ ಇದು TCP ಯ ಹಲವಾರು ಮಿತಿಗಳಿಗೆ ಕಾರಣವಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, TCP ಯ ಚೌಕಟ್ಟಿನೊಳಗೆ ಸ್ಪೆಕ್ಟ್ರೋಕೆಮಿಕಲ್ ಸರಣಿಯಲ್ಲಿ ಹಲವಾರು ಲಿಗಂಡ್ಗಳು ಮತ್ತು ಲೋಹಗಳ ಸ್ಥಾನವನ್ನು ವಿವರಿಸಲು ಕಷ್ಟವಾಗುತ್ತದೆ, ಇದು ಒಂದು ನಿರ್ದಿಷ್ಟ ಮಟ್ಟದ ಕೋವೆಲೆನ್ಸಿ ಮತ್ತು ಬಹು ಲೋಹ-ಲಿಗಂಡ್ ಬಂಧಗಳ ರಚನೆಯ ಸಾಧ್ಯತೆಯೊಂದಿಗೆ ಸಂಬಂಧಿಸಿದೆ. ಆಣ್ವಿಕ ಕಕ್ಷೆಗಳ ಹೆಚ್ಚು ಸಂಕೀರ್ಣ ಮತ್ತು ಕಡಿಮೆ ದೃಶ್ಯ ವಿಧಾನವನ್ನು ಬಳಸಿಕೊಂಡು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆಯನ್ನು ಪರಿಗಣಿಸುವಾಗ ಈ ಮಿತಿಗಳನ್ನು ತೆಗೆದುಹಾಕಲಾಗುತ್ತದೆ.
ವೇಲೆನ್ಸ್ ಬಾಂಡ್ ಸಿದ್ಧಾಂತ ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳಲ್ಲಿನ ರಾಸಾಯನಿಕ ಬಂಧಗಳ ಸ್ವರೂಪವನ್ನು ಸರಿಸುಮಾರು ವಿವರಿಸಲು ಬಳಸಿದ ಕ್ವಾಂಟಮ್ ಯಾಂತ್ರಿಕ ಸಿದ್ಧಾಂತಗಳಲ್ಲಿ ಮೊದಲನೆಯದು. ಇದರ ಅಪ್ಲಿಕೇಶನ್ ಕಲ್ಪನೆಯನ್ನು ಆಧರಿಸಿದೆ ದಾನಿ-ಸ್ವೀಕರಿಸುವ ಕಾರ್ಯವಿಧಾನಲಿಗಂಡ್ ಮತ್ತು ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ನಡುವೆ ಕೋವೆಲನ್ಸಿಯ ಬಂಧಗಳ ರಚನೆ. ಲಿಗಾಂಡ್ಎಣಿಕೆ ಮಾಡುತ್ತದೆ ದಾನಿ ಕಣ, ಒಂದು ಜೋಡಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ವರ್ಗಾಯಿಸುವ ಸಾಮರ್ಥ್ಯ ಸ್ವೀಕರಿಸುವವರು – ಸಂಕೀರ್ಣ ಏಜೆಂಟ್, ಇದು ಬಂಧಗಳ ರಚನೆಗೆ ಅದರ ಶಕ್ತಿಯ ಮಟ್ಟಗಳ ಉಚಿತ ಕ್ವಾಂಟಮ್ ಕೋಶಗಳನ್ನು (ಪರಮಾಣು ಕಕ್ಷೆಗಳು) ಒದಗಿಸುತ್ತದೆ.
ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಮತ್ತು ಲಿಗಂಡ್ಗಳ ನಡುವೆ ಕೋವೆಲನ್ಸಿಯ ಬಂಧಗಳ ರಚನೆಗೆ, ಖಾಲಿಯಾಗಿರುವುದು ಅವಶ್ಯಕ ರು-, ಪ- ಅಥವಾ ಡಿಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಪರಮಾಣು ಕಕ್ಷೆಗಳು ಒಳಗಾಗಿವೆ ಹೈಬ್ರಿಡೈಸೇಶನ್ಒಂದು ನಿರ್ದಿಷ್ಟ ಪ್ರಕಾರ. ಹೈಬ್ರಿಡ್ ಕಕ್ಷೆಗಳು ಬಾಹ್ಯಾಕಾಶದಲ್ಲಿ ಒಂದು ನಿರ್ದಿಷ್ಟ ಸ್ಥಾನವನ್ನು ಪಡೆದುಕೊಳ್ಳುತ್ತವೆ ಮತ್ತು ಅವುಗಳ ಸಂಖ್ಯೆಯು ಅನುರೂಪವಾಗಿದೆ ಸಮನ್ವಯ ಸಂಖ್ಯೆಸಂಕೀರ್ಣ ಏಜೆಂಟ್.
ಇದು ಆಗಾಗ್ಗೆ ಸಂಭವಿಸುತ್ತದೆ ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಸಂಯೋಜಿಸುವುದುಜೋಡಿಯಾಗಿ ಸಂಕೀರ್ಣಗೊಳಿಸುವ ಏಜೆಂಟ್, ಇದು ನಿರ್ದಿಷ್ಟ ಸಂಖ್ಯೆಯ ಕ್ವಾಂಟಮ್ ಕೋಶಗಳನ್ನು ಬಿಡುಗಡೆ ಮಾಡಲು ಅನುವು ಮಾಡಿಕೊಡುತ್ತದೆ - ಪರಮಾಣು ಕಕ್ಷೆಗಳು, ನಂತರ ಹೈಬ್ರಿಡೈಸೇಶನ್ ಮತ್ತು ರಾಸಾಯನಿಕ ಬಂಧಗಳ ರಚನೆಯಲ್ಲಿ ಭಾಗವಹಿಸುತ್ತವೆ.
ಲಿಗಂಡ್ಗಳ ಒಂಟಿ ಜೋಡಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಹೈಬ್ರಿಡ್ ಆರ್ಬಿಟಲ್ಗಳೊಂದಿಗೆ ಸಂವಹನ ನಡೆಸುತ್ತವೆ, ಮತ್ತು ಅತಿಕ್ರಮಣಇಂಟರ್ನ್ಯೂಕ್ಲಿಯರ್ ಜಾಗದಲ್ಲಿ ಹೆಚ್ಚಿದ ಎಲೆಕ್ಟ್ರಾನ್ ಸಾಂದ್ರತೆಯ ಗೋಚರಿಸುವಿಕೆಯೊಂದಿಗೆ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಮತ್ತು ಲಿಗಂಡ್ನ ಅನುಗುಣವಾದ ಕಕ್ಷೆಗಳು. ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳು, ಲಿಗಂಡ್ನ ಖಾಲಿ ಪರಮಾಣು ಕಕ್ಷೆಗಳೊಂದಿಗೆ ಸಂವಹನ ನಡೆಸುತ್ತವೆ, ಡೇಟಿವ್ ಯಾಂತ್ರಿಕತೆಯ ಮೂಲಕ ಸಂಪರ್ಕವನ್ನು ಬಲಪಡಿಸುವುದು. ಹೀಗಾಗಿ, ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ರಾಸಾಯನಿಕ ಬಂಧವು ಸಾಮಾನ್ಯವಾಗಿದೆ ಕೋವೆಲನ್ಸಿಯಸಾಕಷ್ಟು ಸಂಪರ್ಕ ಬಾಳಿಕೆ ಬರುವಮತ್ತು ಶಕ್ತಿಯುತವಾಗಿ ಅನುಕೂಲಕರವಾಗಿದೆ.
ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಹೈಬ್ರಿಡ್ ಆರ್ಬಿಟಲ್ಗಳಲ್ಲಿ ನೆಲೆಗೊಂಡಿರುವ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳು ಬಾಹ್ಯಾಕಾಶದಲ್ಲಿ ಸ್ಥಾನವನ್ನು ಪಡೆದುಕೊಳ್ಳುತ್ತವೆ, ಇದರಲ್ಲಿ ಅವುಗಳ ಪರಸ್ಪರ ವಿಕರ್ಷಣೆಯು ಕಡಿಮೆ ಇರುತ್ತದೆ. ಇದು ಕಾರಣವಾಗುತ್ತದೆ ರಚನೆಸಂಕೀರ್ಣ ಅಯಾನುಗಳು ಮತ್ತು ಅಣುಗಳು ಒಂದು ನಿರ್ದಿಷ್ಟ ಅವಲಂಬನೆಯಲ್ಲಿ ಕಂಡುಬರುತ್ತವೆ ಹೈಬ್ರಿಡೈಸೇಶನ್ ಪ್ರಕಾರ.
ವೇಲೆನ್ಸಿ ಬಂಧಗಳ ಸಿದ್ಧಾಂತದ ದೃಷ್ಟಿಕೋನದಿಂದ ಕೆಲವು ಸಂಕೀರ್ಣಗಳ ರಚನೆಯನ್ನು ನಾವು ಪರಿಗಣಿಸೋಣ. ಮೊದಲನೆಯದಾಗಿ, ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ಗಳ ಪರಮಾಣುಗಳ ವೇಲೆನ್ಸಿ ಕಕ್ಷೆಗಳು ಶಕ್ತಿಯಲ್ಲಿ ಹತ್ತಿರದಲ್ಲಿವೆ ಎಂದು ನಾವು ಗಮನಿಸುತ್ತೇವೆ:
ಇ (ಎನ್- 1)ಡಿ » ಇ ಎನ್ಎಸ್ » ಇ ಎನ್.ಪಿ. » ಇ nd
|
ಹೈಬ್ರಿಡೈಸೇಶನ್ ಪ್ರಕಾರ |
ಸಂಕೀರ್ಣದ ಜ್ಯಾಮಿತಿ |
||
|
ರೇಖೀಯ |
-
|
||
|
ತ್ರಿಕೋನಾಕಾರದ |
- |
||
|
ಟೆಟ್ರಾಹೆಡ್ರಾನ್ |
2-
|
||
|
2-
|
|||
|
sp 3 ಡಿ(z 2) |
ತ್ರಿಕೋನ ಬೈಪಿರಮಿಡ್ |
||
|
sp 3 ಡಿ(X 2 - ವೈ 2) |
ಚದರ ಪಿರಮಿಡ್ |
3-
|
|
|
sp 3 ಡಿ 2 , |
3+ |
||
|
sp 3 ಡಿ 3 |
ಪೆಂಟಗೋನಲ್ ಬೈಪಿರಮಿಡ್ |
4-
|
ಉದಾಹರಣೆಗೆ, 2+ ಕ್ಯಾಷನ್ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಜಿಂಕ್ (II) ಅನ್ನು ಒಳಗೊಂಡಿದೆ. ಈ ಸಾಂಪ್ರದಾಯಿಕ ಅಯಾನಿನ ಎಲೆಕ್ಟ್ರಾನ್ ಶೆಲ್ ಸೂತ್ರ 3 ಅನ್ನು ಹೊಂದಿದೆ ಡಿ 10 4ರು 0 4ಪ 0 ಮತ್ತು ಸಾಂಪ್ರದಾಯಿಕವಾಗಿ ಈ ಕೆಳಗಿನಂತೆ ಚಿತ್ರಿಸಬಹುದು:
ಖಾಲಿ 4 ರು- ಮತ್ತು 4 ಪಸತು (II) ಪರಮಾಣುವಿನ ಕಕ್ಷೆಗಳು ನಾಲ್ಕು ರೂಪಗೊಳ್ಳುತ್ತವೆ sp 3-ಹೈಬ್ರಿಡ್ ಆರ್ಬಿಟಲ್ಗಳು ಟೆಟ್ರಾಹೆಡ್ರಾನ್ನ ಶೃಂಗಗಳ ಕಡೆಗೆ ಆಧಾರಿತವಾಗಿವೆ.
ಪ್ರತಿ ಅಮೋನಿಯ ಅಣುವು ಸಾರಜನಕ ಪರಮಾಣುವಿನ ಮೇಲೆ ಒಂಟಿ ಜೋಡಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಒಂಟಿ ಜೋಡಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವ ಸಾರಜನಕ ಪರಮಾಣುಗಳ ಕಕ್ಷೆಗಳು ಅತಿಕ್ರಮಿಸುತ್ತವೆ spಸತು (II) ನ 3-ಹೈಬ್ರಿಡ್ ಆರ್ಬಿಟಲ್ಗಳು, ಟೆಟ್ರಾಅಮೈನ್ ಸತು (II) 2+ ನ ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣ ಕ್ಯಾಷನ್ ಅನ್ನು ರೂಪಿಸುತ್ತವೆ:
2+ ಅಯಾನು ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿಲ್ಲವಾದ್ದರಿಂದ, ಅದು ಪ್ರದರ್ಶಿಸುತ್ತದೆ ಕಾಂತೀಯಗುಣಲಕ್ಷಣಗಳು.
ಟೆಟ್ರಾಕ್ಲೋರೊಮ್ಯಾಂಗನೇಟ್(II) ಅಯಾನ್ 2- ಪ್ರತಿ 3 ಗೆ ಐದು ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ ಡಿ-ಕಕ್ಷೆಗಳು ಮತ್ತು ಖಾಲಿ 4 ರು- ಮತ್ತು 4 ಪ- ಕಕ್ಷೆಗಳು. ಖಾಲಿ ಕಕ್ಷೆಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ sp 3-ಹೈಬ್ರಿಡ್ ಆರ್ಬಿಟಲ್ಗಳು ಅತಿಕ್ರಮಿಸುತ್ತವೆ ಪಕ್ಲೋರೈಡ್ ಅಯಾನುಗಳ ಪರಮಾಣು ಕಕ್ಷೆಗಳು: 
ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಅಯಾನ್ 2- ಹೀಗೆ ಪಡೆಯಲಾಗಿದೆ ಪರಕಾಂತೀಯ, ಇದು ಐದು ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಒಳಗೊಂಡಿರುವುದರಿಂದ.
ಸಾಂಪ್ರದಾಯಿಕ ಭವಿಷ್ಯ ಅಲ್ಗಾರಿದಮ್ ಅನ್ನು ಬಳಸುವುದು ಪರಮಾಣು ಕಕ್ಷೆಗಳ ಹೈಬ್ರಿಡೈಸೇಶನ್ ವಿಧವೇಲೆನ್ಸ್ ಬಾಂಡ್ ವಿಧಾನದ ಚೌಕಟ್ಟಿನೊಳಗೆ, ಒಬ್ಬರು ನಿರ್ಧರಿಸಬಹುದು ಸಂಕೀರ್ಣಗಳ ಜ್ಯಾಮಿತಿವಿಭಿನ್ನ ಸಂಯೋಜನೆಯ. ಇದನ್ನು ಮಾಡಲು, ಮೊದಲನೆಯದಾಗಿ, ವೇಲೆನ್ಸಿ ಮಟ್ಟಕ್ಕೆ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸೂತ್ರವನ್ನು ಬರೆಯುವುದು ಮತ್ತು ಕ್ವಾಂಟಮ್ ಕೋಶಗಳ ಮೇಲೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿತರಣೆಯ ರೇಖಾಚಿತ್ರವನ್ನು ನಿರ್ಮಿಸುವುದು ಅವಶ್ಯಕ. ಉದಾಹರಣೆಗೆ, ತಟಸ್ಥ ನಿಕಲ್ ಪರಮಾಣುಗಾಗಿ:

ಪರಿವರ್ತನೆ 4 ರು 3 ಗಾಗಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಡಿ- ಉಪಮಟ್ಟದ ರೂಪಾಂತರಗಳು ಪರಕಾಂತೀಯನಿ ಪರಮಾಣು 0 ಇಂಚು ಕಾಂತೀಯಕಣ ನಿ*: 
ಪರಿಣಾಮವಾಗಿ ಖಾಲಿಯಾದ ಕಕ್ಷೆಗಳು ಹೈಬ್ರಿಡೈಸೇಶನ್ಗೆ ಒಳಗಾಗುತ್ತವೆ, ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಸಂರಚನೆಯನ್ನು ರೂಪಿಸುತ್ತವೆ. ಅದರಂತೆ ನಿರ್ಮಿಸಲಾಗಿದೆ ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಕಾಂತೀಯಟೆಟ್ರಾಕಾರ್ಬೊನಿಲ್ನಿಕಲ್ ಸಂಕೀರ್ಣ (CN = 4), ಇದು ಗಮನಾರ್ಹ ಸ್ಥಿರತೆಯಿಂದ ನಿರೂಪಿಸಲ್ಪಟ್ಟಿದೆ.
ಎಲೆಕ್ಟ್ರಾನ್ ಸಂರಚನೆಯೊಂದಿಗೆ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ನಿಕಲ್ (II) ಆಗಿದ್ದರೆ 3 ಡಿ 8 4ರು 0 4ಪ 0, ನಂತರ 4 ರಿಂದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಚಲಿಸುವ ಅವಶ್ಯಕತೆಯಿದೆ ರುಸಮನ್ವಯ ಸಂಖ್ಯೆ 4 ಅನ್ನು ಅರಿತುಕೊಳ್ಳಲು ಸಾಕಷ್ಟು ಸಂಖ್ಯೆಯ ಖಾಲಿ ಕಕ್ಷೆಗಳು ಇರುವುದರಿಂದ ಹೈಬ್ರಿಡೈಸೇಶನ್ ಕಣ್ಮರೆಯಾಗುವ ಮೊದಲು ಸಬ್ಲೆವೆಲ್: 
ಈ ರಚನೆಯು ಅಸ್ಥಿರತೆಯನ್ನು ಹೊಂದಿದೆ ಪರಕಾಂತೀಯಟೆಟ್ರಾಬ್ರೊಮೊನಿಕೊಲೇಟ್ (II) -ಐಯಾನ್ 2- ಸಂಕೀರ್ಣ. ಆದಾಗ್ಯೂ, ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಸಂಯೋಜಿಸುವಾಗ 3 ಡಿ-ಸಬ್ಲೆವೆಲ್ ಅನ್ನು ಜೋಡಿಯಾಗಿ ಮತ್ತು ಈ ಸಬ್ಲೆವೆಲ್ನ ಕ್ವಾಂಟಮ್ ಕೋಶಗಳಲ್ಲಿ ಒಂದನ್ನು ಖಾಲಿಯಾಗಿ ಪರಿವರ್ತಿಸುವುದರಿಂದ ಹೈಬ್ರಿಡೈಸೇಶನ್ ಪ್ರಕಾರ ಮತ್ತು ಪರಿಣಾಮವಾಗಿ ಸಂಕೀರ್ಣದ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಬದಲಾಯಿಸುತ್ತದೆ: 
ಹೈಬ್ರಿಡೈಸೇಶನ್ ಪ್ರಕಾರ ಡಿಎಸ್ಪಿ 2 ಮತ್ತು ಸಂಕೀರ್ಣದ ಸಮತಲ ಚೌಕದ ಆಕಾರವು ಸ್ಥಿರತೆಯ ರಚನೆಯ ಮೇಲೆ ಅರಿತುಕೊಳ್ಳುತ್ತದೆ ಕಾಂತೀಯಸಂಕೀರ್ಣ ಟೆಟ್ರಾಸಯಾನೋನಿಕ್ಕೊಲೇಟ್(II)-ಐಯಾನ್ 2- (CN = 4): 
ಹೆಚ್ಚುವರಿ ಲಿಗಂಡ್ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ ಸೈನೈಡ್ ಸಂಕೀರ್ಣದ ಸಂಶ್ಲೇಷಣೆಯನ್ನು ನಡೆಸಿದರೆ, 5 ರ ಸಮನ್ವಯ ಸಂಖ್ಯೆಯನ್ನು ಅರಿತುಕೊಳ್ಳಬಹುದು: 
ಅಚಲವಾದ ಕಾಂತೀಯಪೆಂಟಾಸಿಯಾನೊನಿಕೊಲೇಟ್ (II) -ಐಯಾನ್ 3- ಸಂಕೀರ್ಣವು ಚೌಕಾಕಾರದ ಪಿರಮಿಡ್ನ ಆಕಾರವನ್ನು ಹೊಂದಿದೆ: 
ಆಕ್ಟಾಹೆಡ್ರಲ್ ನಿಕಲ್(II) 2+ ಸಂಕೀರ್ಣ, ಆದರೂ ಪರಕಾಂತೀಯ, ಆದರೆ ಸಾಕಷ್ಟು ಸ್ಥಿರವಾಗಿದೆ. ಅವರ ವಿದ್ಯಾಭ್ಯಾಸ ಬಾಕಿಯಿದೆ sp 3 ಡಿ 2-ನಿಕಲ್ ಪರಮಾಣು ಕಕ್ಷೆಗಳ ಹೈಬ್ರಿಡೈಸೇಶನ್: 
ಹೊರಗಿನ ಪರಮಾಣು ಕಕ್ಷೆಗಳು ಡಿ-ಉಪಮಟ್ಟದ, ಸಂಕೀರ್ಣ, ನಿಯಮದಂತೆ, ದೊಡ್ಡ ಪ್ರಮಾಣದಲ್ಲಿ ಪರಕಾಂತೀಯಮತ್ತು ಕರೆಯಲಾಗುತ್ತದೆ ಹೊರ-ಕಕ್ಷೆಯಅಥವಾ ಹೆಚ್ಚಿನ ಸ್ಪಿನ್. ಅಂತಹ ಸಂಕೀರ್ಣಗಳ ರಚನೆಯು ಹೈಬ್ರಿಡೈಸೇಶನ್ ಪ್ರಕಾರಕ್ಕೆ ಅನುಗುಣವಾಗಿರಬಹುದು, ಉದಾಹರಣೆಗೆ, sp 3 ಡಿ 2 .
ಅಂತಹ ಸಂಕೀರ್ಣಗಳು, ರಚನೆಯ ಸಮಯದಲ್ಲಿ ಹೊರಭಾಗದ ಪರಮಾಣು ಕಕ್ಷೆಗಳ ಭಾಗವಹಿಸುವಿಕೆಯೊಂದಿಗೆ ಹೈಬ್ರಿಡೈಸೇಶನ್ ನಡೆಯುತ್ತದೆ ಡಿ-ಉಪಮಟ್ಟಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ಒಳ-ಕಕ್ಷೆಯಅಥವಾ ಕಡಿಮೆ ಸ್ಪಿನ್ಮತ್ತು ನಿಯಮದಂತೆ, ಕಾಂತೀಯಅಥವಾ ದುರ್ಬಲವಾಗಿ ಪ್ಯಾರಾಮ್ಯಾಗ್ನೆಟಿಕ್(ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಎಲ್ಲಾ ಅಥವಾ ಬಹುತೇಕ ಎಲ್ಲಾ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಜೋಡಿಯಾಗಿವೆ ಮತ್ತು ಹೈಬ್ರಿಡೈಸೇಶನ್ ಪ್ರಕಾರ, ಉದಾ. ಡಿ 2 sp 3 ಅಥವಾ ಡಿಎಸ್ಪಿ 2).
ಕಬ್ಬಿಣದ (II) ಸಂಕೀರ್ಣಗಳನ್ನು ಪರೀಕ್ಷಿಸುವಾಗ, ಬಾಹ್ಯ ಕಕ್ಷೀಯ ಮತ್ತು ಇಂಟ್ರಾಆರ್ಬಿಟಲ್ ಸಂಕೀರ್ಣಗಳು ಕಂಡುಬರುತ್ತವೆ.


ಕೆಳಗಿನ ರೇಖಾಚಿತ್ರವು ಅವು ಹೇಗೆ ರೂಪುಗೊಳ್ಳುತ್ತವೆ ಎಂಬುದನ್ನು ತೋರಿಸುತ್ತದೆ ಪ್ಯಾರಾಮ್ಯಾಗ್ನೆಟಿಕ್ ಹೈ-ಸ್ಪಿನ್ಹೆಕ್ಸಾಫ್ಲೋರೋಫೆರೇಟ್(II)-ಐಯಾನ್ 4- ಮತ್ತು ಡಯಾಮ್ಯಾಗ್ನೆಟಿಕ್ ಕಡಿಮೆ ಸ್ಪಿನ್ hexacyanoferrate(II) ಅಯಾನ್ 4-.
ಪ್ರತಿ ನಿರ್ದಿಷ್ಟ ಪ್ರಕರಣದಲ್ಲಿ ಯಾವ ರೀತಿಯ ಸಂಕೀರ್ಣವು ರೂಪುಗೊಳ್ಳುತ್ತದೆ ಎಂಬ ಪ್ರಶ್ನೆಗೆ ವೇಲೆನ್ಸ್ ಬಾಂಡ್ಗಳ ಸಿದ್ಧಾಂತವು ಉತ್ತರಿಸುವುದಿಲ್ಲ, ಏಕೆಂದರೆ ಈ ವಿಧಾನವು ಲಿಗಂಡ್ನ ಸ್ವಭಾವದ ಪ್ರಭಾವವನ್ನು ಗಣನೆಗೆ ತೆಗೆದುಕೊಳ್ಳುವುದಿಲ್ಲ. ಆದ್ದರಿಂದ, ವೇಲೆನ್ಸ್ ಬಾಂಡ್ ವಿಧಾನವು ಸಂಕೀರ್ಣದ ಕಾಂತೀಯ ಗುಣಲಕ್ಷಣಗಳ ಡೇಟಾ ಅಥವಾ ರೂಪುಗೊಂಡ ಸಂಕೀರ್ಣದ ಸ್ವರೂಪದ ಮೇಲೆ ಲಿಗಂಡ್ನ ಪ್ರಭಾವದ ಮಾಹಿತಿಯೊಂದಿಗೆ ಅಗತ್ಯವಾಗಿ ಪೂರಕವಾಗಿರಬೇಕು.
.ಕ್ರಿಸ್ಟಲ್ ಫೀಲ್ಡ್ ಸಿದ್ಧಾಂತ 20 ನೇ ಶತಮಾನದ 40 ರ ದಶಕದಲ್ಲಿ ವೇಲೆನ್ಸಿ ಬಾಂಡ್ಗಳ ಸಿದ್ಧಾಂತವನ್ನು ಬದಲಾಯಿಸಿತು. ಅದರ ಶುದ್ಧ ರೂಪದಲ್ಲಿ, ಇದನ್ನು ಪ್ರಸ್ತುತ ಬಳಸಲಾಗುವುದಿಲ್ಲ, ಏಕೆಂದರೆ ಇದು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಕೋವೆಲನ್ಸಿಯ ಬಂಧಗಳ ರಚನೆಯನ್ನು ವಿವರಿಸಲು ಸಾಧ್ಯವಿಲ್ಲ ಮತ್ತು ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಸಂದರ್ಭದಲ್ಲಿ ಸಹ ಲಿಗಂಡ್ಗಳ ನಿಜವಾದ ಸ್ಥಿತಿಯನ್ನು (ಉದಾಹರಣೆಗೆ, ಅವುಗಳ ನಿಜವಾದ ಗಾತ್ರಗಳು) ಗಣನೆಗೆ ತೆಗೆದುಕೊಳ್ಳುವುದಿಲ್ಲ. ಸಂಪೂರ್ಣವಾಗಿ ಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ ಗೆ.
ಈಗಾಗಲೇ 50 ರ ದಶಕದ ಮಧ್ಯಭಾಗದಲ್ಲಿ, ಸರಳೀಕೃತ ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದ ಸಿದ್ಧಾಂತವನ್ನು ಸುಧಾರಿತವಾಗಿ ಬದಲಾಯಿಸಲಾಯಿತು. ಲಿಗಂಡ್ ಕ್ಷೇತ್ರ ಸಿದ್ಧಾಂತ, ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಮತ್ತು ಲಿಗಂಡ್ ನಡುವಿನ ರಾಸಾಯನಿಕ ಬಂಧಗಳ ಕೋವೆಲನ್ಸಿಯ ಸ್ವಭಾವವನ್ನು ಗಣನೆಗೆ ತೆಗೆದುಕೊಳ್ಳುವುದು.
ಆದಾಗ್ಯೂ, ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳ ರಚನೆಯನ್ನು ವಿವರಿಸುವ ಸಾಮಾನ್ಯ ವಿಧಾನವನ್ನು ನೀಡಲಾಗಿದೆ ಆಣ್ವಿಕ ಕಕ್ಷೀಯ ಸಿದ್ಧಾಂತ(MO), ಇದು ಪ್ರಸ್ತುತ ಎಲ್ಲಕ್ಕಿಂತ ಮೇಲುಗೈ ಸಾಧಿಸುತ್ತದೆ. ಆಣ್ವಿಕ ಕಕ್ಷೀಯ ವಿಧಾನವು ಅತಿಕ್ರಮಿಸುವ ಪರಮಾಣು ಕಕ್ಷೆಗಳ ಅನುಪಸ್ಥಿತಿಯಲ್ಲಿ ಸಂಪೂರ್ಣವಾಗಿ ಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ ಪರಸ್ಪರ ಕ್ರಿಯೆಯನ್ನು ಒದಗಿಸುತ್ತದೆ, ಮತ್ತು ಅತಿಕ್ರಮಣದ ಮಧ್ಯಂತರ ಡಿಗ್ರಿಗಳ ಸಂಪೂರ್ಣ ಸೆಟ್.
ಮೂಲ ಪರಿಕಲ್ಪನೆಗಳನ್ನು ನೋಡೋಣ ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದ ಸಿದ್ಧಾಂತ, ವೇಲೆನ್ಸಿ ಬಾಂಡ್ಗಳ ಸಿದ್ಧಾಂತದಂತೆ, ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳಲ್ಲಿನ ರಾಸಾಯನಿಕ ಬಂಧಗಳ ಗುಣಾತ್ಮಕ ವಿವರಣೆಗಾಗಿ ಅದರ ಮಹತ್ವವನ್ನು ಅದರ ಸರಳತೆ ಮತ್ತು ಸ್ಪಷ್ಟತೆಯಿಂದಾಗಿ ಇನ್ನೂ ಉಳಿಸಿಕೊಂಡಿದೆ.
ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರ ಸಿದ್ಧಾಂತದಲ್ಲಿ, ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಮತ್ತು ಲಿಗಂಡ್ ನಡುವಿನ ರಾಸಾಯನಿಕ ಬಂಧವನ್ನು ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ ಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ. ಈ ಸಿದ್ಧಾಂತದ ಪ್ರಕಾರ, ಲಿಗಂಡ್ಗಳು ಸಾಮಾನ್ಯ ಪಾಲಿಹೆಡ್ರಾದ ಶೃಂಗಗಳಲ್ಲಿ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಸುತ್ತಲೂ ನೆಲೆಗೊಂಡಿವೆ ( ಬಹುಮುಖಿ) ನಂತೆ ಪಾಯಿಂಟ್ ಶುಲ್ಕಗಳು. ಸಿದ್ಧಾಂತವು ಲಿಗಂಡ್ನ ನಿಜವಾದ ಪರಿಮಾಣವನ್ನು ಗಣನೆಗೆ ತೆಗೆದುಕೊಳ್ಳುವುದಿಲ್ಲ.
ಲಿಗಂಡ್ಗಳು, ಪಾಯಿಂಟ್ ಚಾರ್ಜ್ಗಳಂತೆ, ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಸುತ್ತಲೂ ರಚಿಸುತ್ತವೆ ಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ ಕ್ಷೇತ್ರ("ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರ", ನಾವು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತದ ಸ್ಫಟಿಕವನ್ನು ಪರಿಗಣಿಸಿದರೆ, ಅಥವಾ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರ), ಇದರಲ್ಲಿ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಶಕ್ತಿಯ ಮಟ್ಟಗಳು ಮತ್ತು, ಎಲ್ಲಕ್ಕಿಂತ ಹೆಚ್ಚಾಗಿ, ಡಿ-ಉಪಮಟ್ಟಗಳು ವಿಭಜನೆಯಾಗುತ್ತಿವೆ, ಮತ್ತು ಅವರ ಶಕ್ತಿಯ ಬದಲಾವಣೆಗಳು. ವಿಭಜನೆಯ ಸ್ವರೂಪ, ಹೊಸ ಶಕ್ತಿಯ ಮಟ್ಟಗಳ ಶಕ್ತಿ ಅವಲಂಬಿಸಿರುತ್ತದೆ ಸಮ್ಮಿತಿಲಿಗಂಡ್ಗಳ ವ್ಯವಸ್ಥೆ (ಆಕ್ಟಾಹೆಡ್ರಲ್, ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಅಥವಾ ಇತರ ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರ). H 2 O, NH 3, CO ಮತ್ತು ಇತರ ಅಣುಗಳನ್ನು ಲಿಗಂಡ್ಗಳಾಗಿ ಸಂಯೋಜಿಸಿದಾಗ, ಅವುಗಳನ್ನು ಹೀಗೆ ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ ದ್ವಿಧ್ರುವಿಗಳು, ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಕಡೆಗೆ ಋಣಾತ್ಮಕ ಚಾರ್ಜ್ನೊಂದಿಗೆ ಆಧಾರಿತವಾಗಿದೆ.
ಲಿಗಂಡ್ಗಳ ಆಕ್ಟಾಹೆಡ್ರಲ್ ಜೋಡಣೆಯ ಪ್ರಕರಣವನ್ನು ನಾವು ಪರಿಗಣಿಸೋಣ (ಉದಾಹರಣೆಗೆ, 3- ಅಥವಾ 3+). ಆಕ್ಟಾಹೆಡ್ರಾನ್ನ ಮಧ್ಯದಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳೊಂದಿಗೆ ಸಂಕೀರ್ಣವಾದ ಪರಮಾಣು M(+n) ಇದೆ ಡಿಪರಮಾಣು ಕಕ್ಷೆಗಳು, ಮತ್ತು ಅದರ ಶೃಂಗಗಳಲ್ಲಿ ಪಾಯಿಂಟ್ ಋಣಾತ್ಮಕ ಶುಲ್ಕಗಳ ರೂಪದಲ್ಲಿ ಲಿಗಂಡ್ಗಳಿವೆ (ಉದಾಹರಣೆಗೆ, F - ಅಯಾನುಗಳು ಅಥವಾ NH 3 ನಂತಹ ಧ್ರುವ ಅಣುಗಳು). ಸಾಂಪ್ರದಾಯಿಕ ಅಯಾನು M(+n) ಲಿಗಂಡ್ಗಳೊಂದಿಗೆ ಸಂಬಂಧ ಹೊಂದಿಲ್ಲ, ಎಲ್ಲಾ ಐದರ ಶಕ್ತಿಗಳು ಡಿ-AO ಒಂದೇ (ಅಂದರೆ ಪರಮಾಣು ಕಕ್ಷೆಗಳು ಅವನತಿ ಹೊಂದುತ್ತವೆ).
ಆದಾಗ್ಯೂ, ಲಿಗಂಡ್ಗಳ ಅಷ್ಟಹೆಡ್ರಲ್ ಕ್ಷೇತ್ರದಲ್ಲಿ ಡಿಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ AO ಗಳು ಸೇರುತ್ತವೆ ಅಸಮಾನಸ್ಥಾನ. ಪರಮಾಣು ಕಕ್ಷೆಗಳು ಡಿ(z 2) ಮತ್ತು ಡಿ(X 2 -
ವೈ 2), ನಿರ್ದೇಶಾಂಕ ಅಕ್ಷಗಳ ಉದ್ದಕ್ಕೂ ಉದ್ದವಾಗಿದ್ದು, ಲಿಗಂಡ್ಗಳಿಗೆ ಹತ್ತಿರಕ್ಕೆ ಬರುತ್ತವೆ. ಈ ಕಕ್ಷೆಗಳು ಮತ್ತು ಆಕ್ಟಾಹೆಡ್ರನ್ನ ಶೃಂಗಗಳಲ್ಲಿರುವ ಲಿಗಂಡ್ಗಳ ನಡುವೆ ಗಮನಾರ್ಹ ವ್ಯತ್ಯಾಸಗಳು ಉದ್ಭವಿಸುತ್ತವೆ. ವಿಕರ್ಷಣ ಶಕ್ತಿಗಳು, ಕಕ್ಷೀಯ ಶಕ್ತಿಯ ಹೆಚ್ಚಳಕ್ಕೆ ಕಾರಣವಾಗುತ್ತದೆ. ಬೇರೆ ರೀತಿಯಲ್ಲಿ ಹೇಳುವುದಾದರೆ, ಈ ಪರಮಾಣು ಕಕ್ಷೆಗಳು ಒಳಪಟ್ಟಿರುತ್ತವೆ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರಕ್ಕೆ ಗರಿಷ್ಠ ಮಾನ್ಯತೆ. ಬಲವಾಗಿ ಸಂಕುಚಿತ ವಸಂತವು ಅಂತಹ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಭೌತಿಕ ಮಾದರಿಯಾಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸುತ್ತದೆ. 

ಇತರೆ ಮೂರು ಡಿ-AO - ಡಿ(xy), ಡಿ(xz) ಮತ್ತು ಡಿ(yz), ನಿರ್ದೇಶಾಂಕ ಅಕ್ಷಗಳ ನಡುವೆ ಮತ್ತು ಲಿಗಂಡ್ಗಳ ನಡುವೆ ಇದೆ, ಅವುಗಳಿಂದ ಹೆಚ್ಚಿನ ದೂರದಲ್ಲಿವೆ. ಅಂತಹವರ ಪರಸ್ಪರ ಕ್ರಿಯೆ ಡಿಲಿಗಂಡ್ಗಳೊಂದಿಗಿನ AO ಕಡಿಮೆ ಮತ್ತು ಆದ್ದರಿಂದ ಶಕ್ತಿ ಡಿ(xy), ಡಿ(xz) ಮತ್ತು ಡಿ(yz)-AO ಮೂಲಕ್ಕೆ ಹೋಲಿಸಿದರೆ ಕಡಿಮೆಯಾಗುತ್ತದೆ. 

ಹೀಗಾಗಿ, ಐದು ಪಟ್ಟು ಅವನತಿ ಡಿ-AO ಸಂಕೀರ್ಣ ಏಜೆಂಟ್, ಒಳಗೆ ಬರುವುದು ಆಕ್ಟಾಹೆಡ್ರಲ್ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರ, ಬಹಿರಂಗ ವಿಭಜನೆಹೊಸ ಕಕ್ಷೆಗಳ ಎರಡು ಗುಂಪುಗಳಾಗಿ - ಮೂರು ಬಾರಿ ಕ್ಷೀಣಿಸುವ ಕಕ್ಷೆಗಳುಕಡಿಮೆ ಶಕ್ತಿಯೊಂದಿಗೆ, ಡಿ(xy), ಡಿ(xz) ಮತ್ತು ಡಿ(yz), ಮತ್ತು ದ್ವಿಗುಣವಾಗಿ ಕ್ಷೀಣಿಸುವ ಕಕ್ಷೆಗಳುಹೆಚ್ಚಿನ ಶಕ್ತಿಯೊಂದಿಗೆ ಡಿ(z 2) ಮತ್ತು ಡಿ(X 2 -
ವೈ 2) ಈ ಹೊಸ ಗುಂಪುಗಳು ಡಿ- ಜೊತೆ ಕಕ್ಷೆಗಳು ಕಡಿಮೆಮತ್ತು ಹೆಚ್ಚಿನ ಶಕ್ತಿಸೂಚಿಸುತ್ತವೆ ಡಿಇ ಮತ್ತು ಡಿ g: 
ಶಕ್ತಿ ವ್ಯತ್ಯಾಸಎರಡು ಹೊಸ ಉಪಹಂತಗಳು ಡಿಇ ಮತ್ತು ಡಿ g ಎಂಬ ಹೆಸರನ್ನು ಪಡೆದುಕೊಂಡಿದೆ ವಿಭಜಿಸುವ ನಿಯತಾಂಕ D0:
ಇ 2 – ಇ 1 = D0
ಎರಡು ಹೊಸ ಸ್ಥಳ ಶಕ್ತಿಯ ಉಪಮಟ್ಟಗಳು ಡಿಇ ಮತ್ತು ಡಿಮೂಲಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ g ( ಡಿ-AO) ಶಕ್ತಿಯ ರೇಖಾಚಿತ್ರದಲ್ಲಿ ಅಸಮವಾದ:
(ಇ 2 – ಇ 0) > (ಇ 0 – ಇ 1).
ಕ್ವಾಂಟಮ್ ಯಾಂತ್ರಿಕ ಸಿದ್ಧಾಂತಅದು ಅಗತ್ಯವಿದೆ ಹೊಸ ಶಕ್ತಿಯ ಮಟ್ಟಗಳು ಸಂಪೂರ್ಣವಾಗಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ತುಂಬಿದಾಗ, ಒಟ್ಟು ಶಕ್ತಿಯು ಬದಲಾಗದೆ ಉಳಿಯುತ್ತದೆ, ಅಂದರೆ ಅವಳು ಉಳಿಯಬೇಕು ಸಮಾನವಾಗಿರುತ್ತದೆ ಇ 0 .
ಬೇರೆ ರೀತಿಯಲ್ಲಿ ಹೇಳುವುದಾದರೆ, ಸಮಾನತೆಯನ್ನು ತೃಪ್ತಿಪಡಿಸಬೇಕು
4(ಇ 2 – ಇ 0) = 6(ಇ 0 – ಇ 1),
ಅಲ್ಲಿ 4 ಮತ್ತು 6 - ಗರಿಷ್ಠಪ್ರತಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆ ಡಿ g - ಮತ್ತು ಡಿಇ-ಎಒ ಈ ಸಮಾನತೆಯಿಂದ ಅದು ಅನುಸರಿಸುತ್ತದೆ
(ಇ 2 – ಇ 0) / (ಇ 0 – ಇ 1) = 3/2 ಮತ್ತು
(ಇ 2 – ಇ 1) / (ಇ 0 – ಇ 1 >) = 5/2, ಅಥವಾ
D0/( ಇ 0 – ಇ 1) = 5/2, ಎಲ್ಲಿಂದ ( ಇ 0 – ಇ 1) = 2/5 ´ D 0 >. ಸಾಧ್ಯವಿರುವ ಗರಿಷ್ಠ ಆರು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಪ್ರತಿ ಎಲೆಕ್ಟ್ರಾನ್ನಲ್ಲಿ ಇರಿಸುವುದು ಡಿಇ-ಆರ್ಬಿಟಲ್ಸ್ ಕಾರಣಗಳು ಇಳಿಕೆ (ಗೆಲುವುಗಳು) ಶಕ್ತಿ 2/5 D 0 ಮೂಲಕ. ಇದಕ್ಕೆ ತದ್ವಿರುದ್ಧವಾಗಿ, ಪ್ರತಿ ಎಲೆಕ್ಟ್ರಾನ್ನ ಸ್ಥಾನವನ್ನು ನಾಲ್ಕರಲ್ಲಿ ಸಾಧ್ಯ ಡಿ g ಕಕ್ಷೆಗಳು ಕಾರಣವಾಗುತ್ತವೆ ಹೆಚ್ಚಳ (ವೆಚ್ಚ) ಶಕ್ತಿ 3/5 D 0 ಮೂಲಕ. ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ತುಂಬಿದ್ದರೆ ಡಿಇ - ಮತ್ತು ಡಿ g -ಕಕ್ಷೆಗಳು ಸಂಪೂರ್ಣವಾಗಿ, ನಂತರ ಇಲ್ಲ ವಿಜೇತಶಕ್ತಿ ಇಲ್ಲ(ಹಾಗೆಯೇ ಆಗುವುದಿಲ್ಲ ಹೆಚ್ಚುವರಿ ಶಕ್ತಿಯ ಬಳಕೆ): 4 ´ 3/5 ´ D 0 - 6 ´ 2/5 ´ D 0 = 0. ಆದರೆ ಮೂಲ ವೇಳೆ ಡಿ-AO ಮಾತ್ರ ಜನಸಂಖ್ಯೆ ಹೊಂದಿದೆ ಭಾಗಶಃಮತ್ತು 1 ರಿಂದ 6 ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ ಮತ್ತು ಈ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಮಾತ್ರ ಇರಿಸಲಾಗುತ್ತದೆ ಡಿ e-AO, ನಂತರ ನಾವು ಪಡೆಯುತ್ತೇವೆ ಗಮನಾರ್ಹ ಶಕ್ತಿಯ ಲಾಭ. ಪ್ರತಿ ಲಿಗಂಡ್ನ ನಿರ್ದಿಷ್ಟತೆಯು ಈ ಲಿಗಂಡ್ ರಚಿಸುವ ಕ್ಷೇತ್ರದ ಮೇಲೆ ಪರಿಣಾಮ ಬೀರುತ್ತದೆ - ಬಲವಾದಅಥವಾ ದುರ್ಬಲ. ಹೇಗೆ ಬಲವಾದ ಕ್ಷೇತ್ರಲಿಗಂಡ್ಗಳಿಗಿಂತ ಹೆಚ್ಚುಅರ್ಥ ವಿಭಜಿಸುವ ನಿಯತಾಂಕ D0. ವಿಭಜಿಸುವ ನಿಯತಾಂಕದ ಅಧ್ಯಯನವು ಸಾಮಾನ್ಯವಾಗಿ ಆಧರಿಸಿದೆ ಸ್ಪೆಕ್ಟ್ರೋಸ್ಕೋಪಿಕ್ಸಂಶೋಧನೆ. ತರಂಗಾಂತರಗಳು ಹೀರಿಕೊಳ್ಳುವ ಬ್ಯಾಂಡ್ಗಳುಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಪರಿವರ್ತನೆಯಿಂದಾಗಿ ಸ್ಫಟಿಕದ ಸ್ಥಿತಿಯಲ್ಲಿ ಅಥವಾ ದ್ರಾವಣದಲ್ಲಿ ಸಂಕೀರ್ಣಗಳು l ಡಿಇ - ಆನ್ ಡಿ g-AO, ಸಂಬಂಧಿಸಿದೆ ವಿಭಜಿಸುವ ನಿಯತಾಂಕ D 0 ಕೆಳಗಿನಂತೆ: n = 1/l; ಡಿ ಪ್ಲ್ಯಾಂಕ್ನ ಸ್ಥಿರತೆ ಎಲ್ಲಿದೆ ಗಂ 6.626 ´ 10 - 34 J. s ಗೆ ಸಮಾನವಾಗಿರುತ್ತದೆ; ವಿಭಜಿಸುವ ನಿಯತಾಂಕ, ಲಿಗಂಡ್ ಪ್ರಕಾರದ ಜೊತೆಗೆ, ಅವಲಂಬಿಸಿರುತ್ತದೆ ಆಕ್ಸಿಡೀಕರಣದ ಮಟ್ಟದಲ್ಲಿಮತ್ತು ಪ್ರಕೃತಿಸಂಕೀರ್ಣ ಏಜೆಂಟ್. ನಲ್ಲಿ ಹೆಚ್ಚುತ್ತಿರುವ ಪರಮಾಣು ಚಾರ್ಜ್ಸಂಕೀರ್ಣ-ರೂಪಿಸುವ ಪರಮಾಣುವಿನ D 0 ಸಹ ಹೆಚ್ಚಾಗುತ್ತದೆ. ಹೆಕ್ಸಾಮಿನಿರಿಡಿಯಮ್(III) 3+, ಹೆಕ್ಸಾಮಿನಿರಿಡಿಯಮ್(III) 3+, ಮತ್ತು ಹೆಕ್ಸಾಮಿನಿರಿಡಿಯಮ್(III) 3+ ಕ್ಯಾಟಯಾನ್ಗಳು ( Z= 27, 45 ಮತ್ತು 77) 22900, 34100 ಮತ್ತು 41000 cm -1 ಗೆ ಸಮಾನವಾದ ವಿಭಜಿಸುವ ನಿಯತಾಂಕಗಳಿಂದ ನಿರೂಪಿಸಲಾಗಿದೆ. ಲಿಗಂಡ್ಗಳ ಸ್ವರೂಪದ ಮೇಲೆ D0 ಅವಲಂಬನೆಯು ಹೆಚ್ಚು ವೈವಿಧ್ಯಮಯವಾಗಿದೆ. ಹಲವಾರು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳ ಅಧ್ಯಯನದ ಪರಿಣಾಮವಾಗಿ, ಅವುಗಳ ಸಾಮಾನ್ಯ ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿಯಲ್ಲಿರುವ ಸಂಕೀರ್ಣ ಲೋಹಗಳ ಸೀಳುವಿಕೆಯ ನಿಯತಾಂಕವನ್ನು ಹೆಚ್ಚಿಸುವ ಸಾಮರ್ಥ್ಯದ ದೃಷ್ಟಿಯಿಂದ, ಸಾಮಾನ್ಯ ಲಿಗಂಡ್ಗಳನ್ನು ಈ ಕೆಳಗಿನಂತೆ ಜೋಡಿಸಬಹುದು ಎಂದು ಕಂಡುಬಂದಿದೆ. ಸ್ಪೆಕ್ಟ್ರೋಕೆಮಿಕಲ್ ಸರಣಿ, ಇದರೊಂದಿಗೆ D 0 ನ ಮೌಲ್ಯವು ಏಕತಾನತೆಯಿಂದ ಹೆಚ್ಚಾಗುತ್ತದೆ: ಹೀಗಾಗಿ, ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಸುತ್ತಲೂ ಪ್ರಬಲವಾದ ಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ ಕ್ಷೇತ್ರ ಮತ್ತು ಪ್ರಬಲವಾದ ಸೀಳು ಡಿ-AO NO 2 - ಲಿಗಂಡ್ಗಳಿಂದ ಉಂಟಾಗುತ್ತದೆ, ಸಿಎನ್ -
ಮತ್ತು CO. ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿತರಣೆಯನ್ನು ನಾವು ಪರಿಗಣಿಸೋಣ ಡಿಇ - ಮತ್ತು ಡಿಲಿಗಂಡ್ಗಳ ಅಷ್ಟಮುಖ ಕ್ಷೇತ್ರದಲ್ಲಿ g-ಕಕ್ಷೆಗಳು. ಚೆಕ್-ಇನ್ ಡಿಇ - ಮತ್ತು ಡಿ g-ಆರ್ಬಿಟಲ್ಸ್ ಪೂರ್ಣ ಅನುಸಾರವಾಗಿ ಸಂಭವಿಸುತ್ತದೆ ಹುಂಡ್ ನಿಯಮಮತ್ತು ಪೌಲಿ ತತ್ವ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ವಿಭಜಿಸುವ ನಿಯತಾಂಕದ ಮೌಲ್ಯವನ್ನು ಲೆಕ್ಕಿಸದೆ, ಮೊದಲ ಮೂರು ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಕ್ವಾಂಟಮ್ ಕೋಶಗಳಿಂದ ಆಕ್ರಮಿಸಲ್ಪಡುತ್ತವೆ ಡಿಇ-ಉಪಮಟ್ಟದ: ಒಂದು ವೇಳೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆ ಶೇ ಡಿ- ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಮೂರು ಉಪ-ಹಂತಗಳಿವೆ; ಅವುಗಳನ್ನು ವಿಭಜಿತ ಉಪ ಹಂತಗಳಲ್ಲಿ ಇರಿಸಲು ಎರಡು ಸಾಧ್ಯತೆಗಳಿವೆ. ವಿಭಜಿಸುವ ನಿಯತಾಂಕದ ಕಡಿಮೆ ಮೌಲ್ಯದಲ್ಲಿ (ಲಿಗಂಡ್ಗಳ ದುರ್ಬಲ ಕ್ಷೇತ್ರ), ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಬೇರ್ಪಡಿಸುವ ಶಕ್ತಿಯ ತಡೆಗೋಡೆಯನ್ನು ಜಯಿಸುತ್ತವೆ ಡಿಇ - ಮತ್ತು ಡಿಜಿ-ಕಕ್ಷೆಗಳು; ನಾಲ್ಕನೇ ಮತ್ತು ನಂತರ ಐದನೇ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಕ್ವಾಂಟಮ್ ಕೋಶಗಳನ್ನು ಜನಪ್ರಿಯಗೊಳಿಸುತ್ತವೆ ಡಿಜಿ-ಉಪಮಟ್ಟದ. ಬಲವಾದ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರ ಮತ್ತು ಹೆಚ್ಚಿನ D0 ಮೌಲ್ಯದೊಂದಿಗೆ, ಜನಸಂಖ್ಯೆಯು ನಾಲ್ಕನೇ ಮತ್ತು ಐದನೇ ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ಜನಸಂಖ್ಯೆಯನ್ನು ಹೊಂದಿದೆ. ಡಿಜಿ-ಸಬ್ಲೆವೆಲ್ ಹೊರಗಿಡಲಾಗಿದೆ; ಭರ್ತಿ ಪ್ರಗತಿಯಲ್ಲಿದೆ ಡಿಇ-ಕಕ್ಷೆಗಳು. ನಲ್ಲಿ ದುರ್ಬಲ ಕ್ಷೇತ್ರ ಲಿಗಂಡ್ಗಳು 4 ಅಥವಾ 5 ಎಲೆಕ್ಟ್ರಾನ್ಗಳೊಂದಿಗೆ ಕ್ವಾಂಟಮ್ ಕೋಶಗಳನ್ನು ಜನಪ್ರಿಯಗೊಳಿಸುವುದು ಸಮಾನಾಂತರ ಸ್ಪಿನ್ಗಳು, ಆದ್ದರಿಂದ ಪರಿಣಾಮವಾಗಿ ಸಂಕೀರ್ಣವು ಬಲವಾಗಿ ಹೊರಹೊಮ್ಮುತ್ತದೆ ಪರಕಾಂತೀಯ. ಬಲವಾದ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರದಲ್ಲಿಒಂದು ಮತ್ತು ನಂತರ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ ಡಿಇ-ಉಪಮಟ್ಟದ, ಆದ್ದರಿಂದ ಪರಕಾಂತತ್ವಸಂಕೀರ್ಣವು ಹೆಚ್ಚು ದುರ್ಬಲವಾಗಿರುತ್ತದೆ. ದುರ್ಬಲ ಕ್ಷೇತ್ರದ ಸಂದರ್ಭದಲ್ಲಿ ಆರನೇ, ಏಳನೇ ಮತ್ತು ಎಂಟನೇ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಮತ್ತೆ ಆನ್ ಆಗುತ್ತವೆ ಡಿಇ-ಸಬ್ಲೆವೆಲ್, ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳಿಗೆ ಸಂರಚನೆಗಳನ್ನು ಪೂರೈಸುತ್ತದೆ (ಪ್ರಕರಣದಲ್ಲಿ ಒಂದು ಡಿ 6, ಎರಡು - ಡಿ 7 ಮತ್ತು ಮೂರು - ಡಿ 8): ಬಲವಾದ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರದ ಸಂದರ್ಭದಲ್ಲಿ, ಆರನೇ ಎಲೆಕ್ಟ್ರಾನ್ ಜನಪ್ರಿಯವಾಗುತ್ತದೆ ಡಿಇ-ಎಒ, ಕಾರಣವಾಗುತ್ತದೆ ಕಾಂತೀಯತೆಸಂಕೀರ್ಣ, ಅದರ ನಂತರ ಏಳನೇ ಮತ್ತು ಎಂಟನೇ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಹೋಗುತ್ತವೆ ಡಿಜಿ-ಉಪಮಟ್ಟದ: ನಿಸ್ಸಂಶಯವಾಗಿ, ಎಂಟು-ಎಲೆಕ್ಟ್ರಾನ್ ಸಂರಚನೆಯೊಂದಿಗೆ ರಚನೆಯಲ್ಲಿ ವ್ಯತ್ಯಾಸಗಳುಲಿಗಂಡ್ಗಳೊಂದಿಗೆ ಸಂಕೀರ್ಣಗಳ ನಡುವೆ ದುರ್ಬಲಮತ್ತು ಬಲವಾದ ಕ್ಷೇತ್ರಗಳು ಕಣ್ಮರೆಯಾಗುತ್ತವೆ. ಒಂಬತ್ತನೇ ಮತ್ತು ಹತ್ತನೇ ಎಲೆಕ್ಟ್ರಾನ್ನಿಂದ ಕಕ್ಷೆಗಳ ಉದ್ಯೋಗವು ಎರಡೂ ಪ್ರಕಾರಗಳ ಸಂಕೀರ್ಣಗಳಿಗೆ ಭಿನ್ನವಾಗಿರುವುದಿಲ್ಲ: ಆಕ್ಟಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣ ಅಯಾನುಗಳು 3+ ಮತ್ತು 3- ವಿದ್ಯುನ್ಮಾನ ರಚನೆಯ ಪರಿಗಣನೆಗೆ ನಾವು ಹಿಂತಿರುಗೋಣ. ನಲ್ಲಿರುವ ಸ್ಥಳದ ಪ್ರಕಾರ ಸ್ಪೆಕ್ಟ್ರೋಕೆಮಿಕಲ್ ಸರಣಿ, ಅಮೋನಿಯ NH 3 ಲಿಗಂಡ್ಗಳಲ್ಲಿ ಒಂದಾಗಿದೆ ಬಲವಾದ ಕ್ಷೇತ್ರ
, ಮತ್ತು ಫ್ಲೋರೈಡ್ ಅಯಾನ್ ಎಫ್ -- ದುರ್ಬಲ ಕ್ಷೇತ್ರ
. ಪರಿಣಾಮವಾಗಿ, ಈ ಸಂಕೀರ್ಣಗಳಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ಪರಮಾಣು ಕಕ್ಷೆಗಳ ಉದ್ಯೋಗವು ಈ ಕೆಳಗಿನ ಯೋಜನೆಯ ಪ್ರಕಾರ ಸಂಭವಿಸುತ್ತದೆ: 3- ಅಯಾನ್ನಲ್ಲಿ, ಎಫ್ - ಲಿಗಂಡ್ಗಳು ದುರ್ಬಲ ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರವನ್ನು (D 0 = 13000 cm - 1) ರಚಿಸುತ್ತವೆ, ಮತ್ತು ಮೂಲ 3 ರ ಎಲ್ಲಾ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಡಿ 6 -JSC ನಲ್ಲಿ ಇದೆ ಡಿಇ - ಮತ್ತು ಡಿಯಾವುದೇ ಜೋಡಣೆಯಿಲ್ಲದೆ g ಕಕ್ಷೆಗಳು. ಒಂದು ಸಂಕೀರ್ಣ ಅಯಾನು ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ಮತ್ತು ನಾಲ್ಕು ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ, ಆದ್ದರಿಂದ ಇದು ಪರಕಾಂತೀಯ. 3+ ಅಯಾನ್ನಲ್ಲಿ, NH 3 ಲಿಗಂಡ್ಗಳು ಬಲವಾದ ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರವನ್ನು ರಚಿಸುತ್ತವೆ (D 0 = 22900 cm - 1), ಎಲ್ಲಾ 3 ಡಿ 6-ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೆಚ್ಚು ಶಕ್ತಿಯುತವಾಗಿ ಅನುಕೂಲಕರವಾದ ಮೇಲೆ ಇರಿಸಲಾಗುತ್ತದೆ ಡಿಇ-ಕಕ್ಷೆಗಳು. ನಿಂದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವರ್ಗಾವಣೆ ಡಿಇ - ಆನ್ ಡಿ g-ಕಕ್ಷೆಗಳು ಅಸಾಧ್ಯಏಕೆಂದರೆ ತುಂಬಾ ಹೆಚ್ಚಿನ ಶಕ್ತಿಯ ತಡೆಗೋಡೆ. ಆದ್ದರಿಂದ, ಈ ಸಂಕೀರ್ಣ ಕ್ಯಾಷನ್ ಆಗಿದೆ ಕಡಿಮೆ ಸ್ಪಿನ್, ಇದು ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವುದಿಲ್ಲ ಮತ್ತು ಕಾಂತೀಯ. ಇದೇ ರೀತಿಯಾಗಿ, 2+ ಮತ್ತು 4- ಅಯಾನುಗಳಿಗೆ ಆಕ್ಟಾಹೆಡ್ರಲ್ ಕ್ಷೇತ್ರದಲ್ಲಿ ಕಕ್ಷೆಗಳ ಮೇಲೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿತರಣೆಯ ಯೋಜನೆಗಳನ್ನು ಪ್ರಸ್ತುತಪಡಿಸಬಹುದು: H 2 O ಲಿಗಂಡ್ಗಳು ದುರ್ಬಲ ಕ್ಷೇತ್ರವನ್ನು ರಚಿಸುತ್ತವೆ; ನಡುವೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿನಿಮಯ ಡಿಇ - ಮತ್ತು ಡಿ g-ಆರ್ಬಿಟಲ್ಗಳು ಯಾವುದೇ ತೊಂದರೆಗಳನ್ನು ಉಂಟುಮಾಡುವುದಿಲ್ಲ ಮತ್ತು ಆದ್ದರಿಂದ ಸಂಕೀರ್ಣ ಅಯಾನುಗಳಲ್ಲಿ ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯು ಸಾಂಪ್ರದಾಯಿಕ Fe + II ಅಯಾನುಗಳಂತೆಯೇ ಇರುತ್ತದೆ. ಪರಿಣಾಮವಾಗಿ ಆಕ್ವಾ ಕಾಂಪ್ಲೆಕ್ಸ್ ಆಗಿದೆ ಹೆಚ್ಚಿನ ಸ್ಪಿನ್, ಪ್ಯಾರಾಮ್ಯಾಗ್ನೆಟಿಕ್. ಸ್ಫಟಿಕದಂತಹ ಸ್ಥಿತಿಯಲ್ಲಿರುವ ಅನೇಕ ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳು ಮತ್ತು ಜಲೀಯ ದ್ರಾವಣವು ಗಾಢವಾದ ಬಣ್ಣವನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಹೀಗಾಗಿ, 2+ ಕ್ಯಾಟಯಾನುಗಳನ್ನು ಹೊಂದಿರುವ ಜಲೀಯ ದ್ರಾವಣವು ಗಾಢವಾದ ನೀಲಿ ಬಣ್ಣವನ್ನು ಹೊಂದಿರುತ್ತದೆ, 3+ ಕ್ಯಾಟಯಾನುಗಳು ದ್ರಾವಣಕ್ಕೆ ನೇರಳೆ ಬಣ್ಣವನ್ನು ನೀಡುತ್ತದೆ ಮತ್ತು 2+ ಕ್ಯಾಟಯಾನುಗಳು ಕೆಂಪು ಬಣ್ಣವನ್ನು ನೀಡುತ್ತವೆ. ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದ ಸಿದ್ಧಾಂತವು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಒಂದು ಬಣ್ಣ ಅಥವಾ ಇನ್ನೊಂದು ನೋಟವನ್ನು ವಿವರಿಸಲು ಸಾಧ್ಯವಾಗಿಸುತ್ತದೆ. ಒಂದು ವಸ್ತುವಿನ ದ್ರಾವಣ ಅಥವಾ ಸ್ಫಟಿಕದ ಮಾದರಿಯ ಮೂಲಕ ಬೆಳಕನ್ನು ಹಾದು ಹೋದರೆ ವರ್ಣಪಟಲದ ಗೋಚರ ಭಾಗ, ನಂತರ, ತಾತ್ವಿಕವಾಗಿ, ಮಾದರಿಯ ದೈಹಿಕ ನಡವಳಿಕೆಗೆ ಮೂರು ಆಯ್ಕೆಗಳು ಸಾಧ್ಯ: ಬೆಳಕಿನ ಹೀರಿಕೊಳ್ಳುವಿಕೆ ಇಲ್ಲಯಾವುದೇ ತರಂಗಾಂತರ (ವಸ್ತು ಮಾದರಿ ಬಣ್ಣರಹಿತ, ಇದು ವರ್ಣಪಟಲದ ನೇರಳಾತೀತ ಪ್ರದೇಶದಲ್ಲಿ ಹೀರಿಕೊಳ್ಳುವ ಬ್ಯಾಂಡ್ಗಳನ್ನು ಹೊಂದಿರಬಹುದು); ಸಂಪೂರ್ಣ ಬೆಳಕಿನ ಹೀರಿಕೊಳ್ಳುವಿಕೆಸಂಪೂರ್ಣ ತರಂಗಾಂತರ ವ್ಯಾಪ್ತಿಯಲ್ಲಿ (ಮಾದರಿಯು ಕಾಣಿಸುತ್ತದೆ ಕಪ್ಪು); ಅಂತಿಮವಾಗಿ, ಬೆಳಕಿನ ಹೀರಿಕೊಳ್ಳುವಿಕೆಮಾತ್ರ ನಿರ್ದಿಷ್ಟ ತರಂಗಾಂತರ(ನಂತರ ಮಾದರಿಯು ಹೊಂದಿರುತ್ತದೆ ಹೀರಿಕೊಳ್ಳಲು ಪೂರಕವಾದ ಬಣ್ಣವರ್ಣಪಟಲದ ಕಿರಿದಾದ ಭಾಗ). ಹೀಗಾಗಿ, ದ್ರಾವಣ ಅಥವಾ ಸ್ಫಟಿಕಗಳ ಬಣ್ಣವನ್ನು ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ ಹೀರಿಕೊಳ್ಳುವ ಬ್ಯಾಂಡ್ಗಳ ಆವರ್ತನಗೋಚರ ಬೆಳಕು: ಸಂಕೀರ್ಣಗಳ ಮೂಲಕ ಬೆಳಕಿನ ಕ್ವಾಂಟಾವನ್ನು ಹೀರಿಕೊಳ್ಳುವುದು (ಉದಾಹರಣೆಗೆ, ಆಕ್ಟಾಹೆಡ್ರಲ್ ರಚನೆಯನ್ನು ಹೊಂದಿರುವವರು) ಎಲೆಕ್ಟ್ರಾನ್ಗಳೊಂದಿಗೆ ಬೆಳಕಿನ ಪರಸ್ಪರ ಕ್ರಿಯೆಯಿಂದ ವಿವರಿಸಲಾಗಿದೆ ಡಿ e-sublevel, ಖಾಲಿ ಕಕ್ಷೆಗಳಿಗೆ ಅವುಗಳ ಪರಿವರ್ತನೆಯೊಂದಿಗೆ ಡಿಜಿ-ಉಪಮಟ್ಟದ. ಉದಾಹರಣೆಗೆ, ಹೆಕ್ಸಾಕ್ವಾಟಿಟಾನಿಯಂ(III) 3+ ಕ್ಯಾಟಯಾನುಗಳನ್ನು ಹೊಂದಿರುವ ಜಲೀಯ ದ್ರಾವಣದ ಮೂಲಕ ಬೆಳಕನ್ನು ಹಾದುಹೋಗುವಾಗ, ವರ್ಣಪಟಲದ ಹಳದಿ-ಹಸಿರು ಪ್ರದೇಶದಲ್ಲಿ (20300 cm - 1, l »500 nm) ಬೆಳಕಿನ ಹೀರಿಕೊಳ್ಳುವ ಬ್ಯಾಂಡ್ ಪತ್ತೆಯಾಗುತ್ತದೆ. ಇದು ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಏಕ ಎಲೆಕ್ಟ್ರಾನ್ನ ಪರಿವರ್ತನೆಯ ಕಾರಣದಿಂದಾಗಿರುತ್ತದೆ ಡಿಇ-ಎಒ ಆನ್ ಡಿಜಿ-ಉಪಮಟ್ಟದ: ಆದ್ದರಿಂದ, 3+ ಹೊಂದಿರುವ ಪರಿಹಾರವು ನೇರಳೆ ಬಣ್ಣವನ್ನು ಪಡೆಯುತ್ತದೆ (ಹೀರಿಕೊಂಡ ಹಳದಿ-ಹಸಿರು ಜೊತೆಗೆ). ವೆನಾಡಿಯಮ್ ಉಪ್ಪು Cl 3 ರ ಪರಿಹಾರವು ಹಸಿರು ಬಣ್ಣದ್ದಾಗಿದೆ. ಇದು ಬೆಳಕಿನ ಕಿರಣದ ಶಕ್ತಿಯ ಭಾಗವನ್ನು ಹೀರಿಕೊಳ್ಳುವಾಗ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಅನುಗುಣವಾದ ಪರಿವರ್ತನೆಗಳ ಕಾರಣದಿಂದಾಗಿರುತ್ತದೆ. ನೆಲದ ಸ್ಥಿತಿಯಲ್ಲಿ, ವನಾಡಿಯಮ್ (III) 3 ರ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸಂರಚನೆಯೊಂದಿಗೆ ಡಿ 2, ಎರಡು ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಆಕ್ರಮಿಸಿಕೊಂಡಿವೆ ಡಿಇ-ಉಪಮಟ್ಟದ: ಮಾತ್ರ ಇದೆ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಪರಿವರ್ತನೆಗೆ ಎರಡು ಆಯ್ಕೆಗಳುಮೇಲೆ ಡಿ g -ಉಪಮಟ್ಟದ: ಒಂದೋ ಎರಡೂಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಆಕ್ರಮಿಸಿಕೊಂಡಿವೆ ಡಿ g -AO, ಅಥವಾ ಮಾತ್ರ ಒಂದುಅವರಲ್ಲಿ. ಒಟ್ಟು ಸ್ಪಿನ್ನಲ್ಲಿನ ಇಳಿಕೆಗೆ ಸಂಬಂಧಿಸಿದ ಯಾವುದೇ ಇತರ ಎಲೆಕ್ಟ್ರಾನ್ ಪರಿವರ್ತನೆಗಳನ್ನು ನಿಷೇಧಿಸಲಾಗಿದೆ. ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಕಾನ್ಫಿಗರೇಶನ್ ಹೊಂದಿದ್ದರೆ ಡಿ 0 ಅಥವಾ ಡಿನಂತರ 10 ಎಲೆಕ್ಟ್ರಾನ್ ಪರಿವರ್ತನೆಗಳುಜೊತೆಗೆ ಡಿಇ - ಆನ್ ಡಿ g -ಸಬ್ಲೆವೆಲ್ ಅಥವಾ ಪ್ರತಿಕ್ರಮದಲ್ಲಿ ಅಸಾಧ್ಯಒಂದೋ ಏಕೆಂದರೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಅನುಪಸ್ಥಿತಿ, ಒಂದೋ ಏಕೆಂದರೆ ಖಾಲಿ ಕಕ್ಷೆಗಳ ಅನುಪಸ್ಥಿತಿ. ಆದ್ದರಿಂದ, Sc(III), Cu(I), Zn(II), Cd(II) ಮುಂತಾದ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ಗಳೊಂದಿಗಿನ ಸಂಕೀರ್ಣಗಳ ಪರಿಹಾರಗಳು ಸ್ಪೆಕ್ಟ್ರಮ್ನ ಗೋಚರ ಭಾಗದಲ್ಲಿ ಶಕ್ತಿಯನ್ನು ಹೀರಿಕೊಳ್ಳುವುದಿಲ್ಲ ಮತ್ತು ಕಾಣಿಸಿಕೊಳ್ಳುತ್ತವೆ. ಬಣ್ಣರಹಿತ: ಬೆಳಕಿನ ಹೀರಿಕೊಳ್ಳುವಿಕೆಯ ಆಯ್ಕೆಯು ಕೇವಲ ಅವಲಂಬಿಸಿರುತ್ತದೆ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ಮತ್ತು ಅದರ ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿ, ಆದರೆ ಸಹ ಲಿಗಂಡ್ಗಳ ವಿಧ. ಸ್ಪೆಕ್ಟ್ರೋಕೆಮಿಕಲ್ ಸರಣಿಯ ಎಡಭಾಗದಲ್ಲಿರುವ ಲಿಗಂಡ್ಗಳನ್ನು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತದಲ್ಲಿ ರಚಿಸುವ ಲಿಗಂಡ್ಗಳೊಂದಿಗೆ ಬದಲಾಯಿಸುವಾಗ ಬಲವಾದಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ ಕ್ಷೇತ್ರವನ್ನು ಗಮನಿಸಲಾಗಿದೆ ಹೆಚ್ಚಳಹರಡುವ ಬೆಳಕಿನಿಂದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ಹೀರಿಕೊಳ್ಳಲ್ಪಟ್ಟ ಶಕ್ತಿಯ ಭಾಗ ಮತ್ತು ಪರಿಣಾಮವಾಗಿ, ಇಳಿಕೆಅನುಗುಣವಾದ ಹೀರಿಕೊಳ್ಳುವ ಬ್ಯಾಂಡ್ನ ತರಂಗಾಂತರ. ಹೀಗಾಗಿ, ಟೆಟ್ರಾಕ್ವಾಕಾಪರ್ (II) 2+ ಕ್ಯಾಟಯಾನ್ಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ಜಲೀಯ ದ್ರಾವಣವು ನೀಲಿ ಬಣ್ಣದ್ದಾಗಿದೆ ಮತ್ತು ಟೆಟ್ರಾಅಮಿನೆಕಾಪರ್ (II) 2+ ಸಲ್ಫೇಟ್ನ ದ್ರಾವಣವು ಗಾಢವಾದ ನೀಲಿ ಬಣ್ಣದ್ದಾಗಿದೆ. ________________________ ಪುನರಾವರ್ತಿಸಿ: >>> ಅರ್ಜಿಗಳನ್ನು
ಕಾರಣ ಶಕ್ತಿಯ ಲಾಭ ಆದ್ಯತೆಯ ವಸಾಹತುಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಡಿಇ-ಪರಮಾಣು ಕಕ್ಷೆಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರದಿಂದ ಸಂಕೀರ್ಣದ ಸ್ಥಿರೀಕರಣದ ಶಕ್ತಿ.
ಬೆಳಕಿನ ವೇಗ ಜೊತೆಗೆ
= 3 ´ 10 10 cm/s.
ಘಟಕ D 0 ತರಂಗ ಸಂಖ್ಯೆ n ನಂತೆಯೇ ಇರುತ್ತದೆ: cm - 1, ಇದು ಸರಿಸುಮಾರು 12 J/mol ಗೆ ಅನುರೂಪವಾಗಿದೆ.
ಅದೇ ಅವಧಿಯ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಮತ್ತು ಅದೇ ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿಯಲ್ಲಿ, ಅದೇ ಲಿಗಂಡ್ಗಳೊಂದಿಗೆ, ಸೀಳುವಿಕೆಯ ನಿಯತಾಂಕವು ಸರಿಸುಮಾರು ಒಂದೇ ಆಗಿರುತ್ತದೆ. ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಆಕ್ಸಿಡೀಕರಣದ ಹೆಚ್ಚುತ್ತಿರುವ ಮಟ್ಟದೊಂದಿಗೆ, D 0 ನ ಮೌಲ್ಯ ಹೆಚ್ಚಾಗುತ್ತದೆ. ಹೀಗಾಗಿ, ಆಕ್ವಾ ಸಂಕೀರ್ಣಗಳು 2+ ಮತ್ತು 2+ ಗಾಗಿ, ವಿಭಜಿಸುವ ನಿಯತಾಂಕದ ಮೌಲ್ಯವು 7800 ಮತ್ತು 10400 cm - 1, ಮತ್ತು 3+ ಮತ್ತು 3+ - 13700 ಮತ್ತು 21000 cm - 1, ಕ್ರಮವಾಗಿ.
I-Br - Cl - » NCS - ಸಂಖ್ಯೆ 3 - ಎಫ್ -ಓಹ್ - H2O »ಎಚ್ - ಎನ್ಎಚ್ 3 ಸಂಖ್ಯೆ 2 -ಸಿಎನ್ - "ಇಲ್ಲ" CO. 









ಇದಕ್ಕೆ ವಿರುದ್ಧವಾಗಿ, CN - ಲಿಗಂಡ್ಗಳು ಗಮನಾರ್ಹವಾದ ಸೀಳನ್ನು ಉಂಟುಮಾಡುತ್ತವೆ ಡಿ-AO, ಮೊತ್ತವು 33000 ಸೆಂ - 1. ಇದರರ್ಥ ಬಲವಿದೆ ಎಲ್ಲಾ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ನಿಯೋಜಿಸುವ ಪ್ರವೃತ್ತಿಮೇಲೆ ಡಿಇ-ಕಕ್ಷೆಗಳು. ಶಕ್ತಿ ಗಳಿಕೆ, ಇಂತಹ ಕಕ್ಷೆಗಳ ಜನಸಂಖ್ಯೆಯೊಂದಿಗೆ ಪಡೆಯಲಾಗಿದೆ, ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಣೆಯ ಕಾರಣ ಶಕ್ತಿಯ ವೆಚ್ಚಕ್ಕಿಂತ ಹೆಚ್ಚು.


ಹೆಚ್ಚುವರಿ ಶಕ್ತಿಯನ್ನು ಪಡೆದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸೂಚಿಸಲಾದ ಪರಿವರ್ತನೆಗಳು ಅನುರೂಪವಾಗಿದೆ ಹೀರಿಕೊಳ್ಳುವ ಬ್ಯಾಂಡ್ಹೆಕ್ಸಾಕ್ವಾವನಾಡಿಯಮ್ (III) ಕ್ಲೋರೈಡ್ನ ದ್ರಾವಣದ ಹೀರಿಕೊಳ್ಳುವ ವರ್ಣಪಟಲದಲ್ಲಿ ಸುಮಾರು 400 nm. ವರ್ಣಪಟಲದ ನೇರಳೆ-ನೇರಳೆ ಪ್ರದೇಶದ ಹೀರಿಕೊಳ್ಳುವಿಕೆಯು ಪರಿಹಾರಕ್ಕೆ ಹೆಚ್ಚುವರಿ ಬಣ್ಣವನ್ನು ನೀಡುತ್ತದೆ - ಪ್ರಕಾಶಮಾನವಾದ ಹಸಿರು.

ಮತ್ತು ಜಾನ್ ವ್ಯಾನ್ ವ್ಲೆಕ್ ಲಿಗಂಡ್ಗಳಿಂದ ಸುತ್ತುವರೆದಿರುವ ಪರಿವರ್ತನೆಯ ಲೋಹದ ಕ್ಯಾಟಯಾನುಗಳ ಕೆಳಗಿನ ಸ್ಥಿತಿಗಳನ್ನು ವಿವರಿಸಲು - ಅಯಾನುಗಳು ಮತ್ತು ತಟಸ್ಥ ಅಣುಗಳು. ಕ್ರಿಸ್ಟಲ್ ಫೀಲ್ಡ್ ಸಿದ್ಧಾಂತವನ್ನು (ಡಿಲೊಕಲೈಸ್ಡ್) ಆಣ್ವಿಕ ಕಕ್ಷೀಯ ಸಿದ್ಧಾಂತದೊಂದಿಗೆ ಮತ್ತಷ್ಟು ಸಂಯೋಜಿಸಲಾಯಿತು [ಮತ್ತು ಪರಿಷ್ಕರಿಸಲಾಗಿದೆ] ಸಮನ್ವಯ ಸಂಯುಕ್ತಗಳಲ್ಲಿನ ಲೋಹ-ಲಿಗಂಡ್ ಬಂಧದ ಭಾಗಶಃ ಕೋವೆಲೆನ್ಸಿಯನ್ನು ಗಣನೆಗೆ ತೆಗೆದುಕೊಳ್ಳುವ ಸಾಮಾನ್ಯ ಸಿದ್ಧಾಂತವಾಗಿದೆ.
ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರ ಸಿದ್ಧಾಂತವು ಸ್ಫಟಿಕಗಳು ಮತ್ತು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳ ಆಪ್ಟಿಕಲ್ ಹೀರಿಕೊಳ್ಳುವ ವರ್ಣಪಟಲ ಮತ್ತು ಎಲೆಕ್ಟ್ರಾನ್ ಪ್ಯಾರಾಮ್ಯಾಗ್ನೆಟಿಕ್ ರೆಸೋನೆನ್ಸ್ ಸ್ಪೆಕ್ಟ್ರಾವನ್ನು ಊಹಿಸಲು ಅಥವಾ ಅರ್ಥೈಸಲು ಅನುವು ಮಾಡಿಕೊಡುತ್ತದೆ, ಹಾಗೆಯೇ ಪರಿವರ್ತನೆಯ ಲೋಹದ ಸಂಕೀರ್ಣಗಳ ಪರಿಹಾರಗಳಲ್ಲಿ ಜಲಸಂಚಯನ ಮತ್ತು ಸ್ಥಿರತೆಯ ಎಂಥಾಲ್ಪಿಗಳು.
ಕ್ರಿಸ್ಟಲ್ ಫೀಲ್ಡ್ ಸಿದ್ಧಾಂತದ ವಿಮರ್ಶೆ[ | ]
TCP ಯ ಪ್ರಕಾರ, ಸಂಕ್ರಮಣ ಲೋಹ ಮತ್ತು ಲಿಗಂಡ್ಗಳ ನಡುವಿನ ಪರಸ್ಪರ ಕ್ರಿಯೆಯು ಧನಾತ್ಮಕ ಆವೇಶದ ಲೋಹದ ಕ್ಯಾಷನ್ ಮತ್ತು ಲಿಗಂಡ್ನ ನಾನ್ಬಾಂಡಿಂಗ್ ಆರ್ಬಿಟಲ್ಗಳಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಋಣಾತ್ಮಕ ಆವೇಶದ ನಡುವಿನ ಆಕರ್ಷಣೆಯಿಂದ ಉದ್ಭವಿಸುತ್ತದೆ. ಸಿದ್ಧಾಂತವು ಐದು ಶಕ್ತಿಯ ಬದಲಾವಣೆಯನ್ನು ಕ್ಷೀಣಿಸುತ್ತದೆ ಎಂದು ಪರಿಗಣಿಸುತ್ತದೆ ಡಿ-ಕಕ್ಷೆಗಳು ಲಿಗಂಡ್ಗಳ ಪಾಯಿಂಟ್ ಚಾರ್ಜ್ಗಳಿಂದ ಸುತ್ತುವರಿದಿವೆ. ಲಿಗಂಡ್ ಲೋಹದ ಅಯಾನನ್ನು ಸಮೀಪಿಸುತ್ತಿದ್ದಂತೆ, ಲಿಗಂಡ್ನ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಕೆಲವರಿಗೆ ಹತ್ತಿರವಾಗುತ್ತವೆ ಡಿಇತರರಿಗಿಂತ ಕಕ್ಷೆಗಳು, ಅವನತಿಯ ನಷ್ಟವನ್ನು ಉಂಟುಮಾಡುತ್ತವೆ. ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಡಿ-ಕಕ್ಷೆಗಳು ಮತ್ತು ಲಿಗಂಡ್ಗಳು ಒಂದೇ ಚಿಹ್ನೆಯೊಂದಿಗೆ ಚಾರ್ಜ್ಗಳಾಗಿ ಪರಸ್ಪರ ಹಿಮ್ಮೆಟ್ಟಿಸುತ್ತವೆ. ಹೀಗಾಗಿ, ಅವರ ಶಕ್ತಿ ಡಿಲಿಗಂಡ್ಗಳಿಗೆ ಹತ್ತಿರವಿರುವ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಹೆಚ್ಚು ದೂರದಲ್ಲಿರುವವುಗಳಿಗಿಂತ ಹೆಚ್ಚಾಗಿರುತ್ತದೆ, ಇದು ಶಕ್ತಿಯ ಮಟ್ಟಗಳ ವಿಭಜನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ ಡಿ- ಕಕ್ಷೆಗಳು.
ಕೆಳಗಿನ ಅಂಶಗಳು ವಿಭಜನೆಯ ಮೇಲೆ ಪ್ರಭಾವ ಬೀರುತ್ತವೆ:
- ಲೋಹದ ಅಯಾನಿನ ಸ್ವರೂಪ.
- ಲೋಹದ ಆಕ್ಸಿಡೀಕರಣದ ಮಟ್ಟ. ಹೆಚ್ಚಿನ ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿ, ಹೆಚ್ಚಿನ ಸೀಳುವ ಶಕ್ತಿ.
- ಲೋಹದ ಅಯಾನಿನ ಸುತ್ತ ಲಿಗಂಡ್ಗಳ ಜೋಡಣೆ.
- ಲೋಹದ ಅಯಾನನ್ನು ಸುತ್ತುವರೆದಿರುವ ಲಿಗಂಡ್ಗಳ ಸ್ವರೂಪ. ಲಿಗಂಡ್ಗಳ ಪರಿಣಾಮವು ಬಲವಾಗಿರುತ್ತದೆ, ಹೆಚ್ಚಿನ ಮತ್ತು ಕಡಿಮೆ ಶಕ್ತಿಯ ಮಟ್ಟಗಳ ನಡುವಿನ ವ್ಯತ್ಯಾಸವು ಹೆಚ್ಚಾಗುತ್ತದೆ.
ಲಿಗಂಡ್ ಸಮನ್ವಯದ ಅತ್ಯಂತ ಸಾಮಾನ್ಯ ವಿಧವಾಗಿದೆ ಅಷ್ಟಮುಖಿ, ಇದರಲ್ಲಿ ಆರು ಲಿಗಂಡ್ಗಳು ಲೋಹದ ಅಯಾನಿನ ಸುತ್ತ ಆಕ್ಟಾಹೆಡ್ರಲ್ ಸಮ್ಮಿತಿಯ ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರವನ್ನು ರಚಿಸುತ್ತವೆ. ಹೊರಗಿನ ಶೆಲ್ನಲ್ಲಿ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ನೊಂದಿಗೆ ಲೋಹದ ಅಯಾನಿನ ಅಷ್ಟಮುಖ ಪರಿಸರದಲ್ಲಿ, ಡಿ-ಆರ್ಬಿಟಲ್ಗಳನ್ನು ಶಕ್ತಿಯ ಮಟ್ಟಗಳಲ್ಲಿ ವ್ಯತ್ಯಾಸದೊಂದಿಗೆ ಎರಡು ಗುಂಪುಗಳಾಗಿ ವಿಂಗಡಿಸಲಾಗಿದೆ Δ oct ( ವಿದಳನ ಶಕ್ತಿ), ಆದರೆ ಕಕ್ಷೆಗಳ ಶಕ್ತಿ dxy, dxzಮತ್ತು d yzಗಿಂತ ಕಡಿಮೆ ಇರುತ್ತದೆ ಡಿ z 2 ಮತ್ತು ಡಿ X 2 -ವೈ 2, ಮೊದಲ ಗುಂಪಿನ ಕಕ್ಷೆಗಳು ಲಿಗಂಡ್ಗಳಿಂದ ಮುಂದೆ ನೆಲೆಗೊಂಡಿರುವುದರಿಂದ ಮತ್ತು ಕಡಿಮೆ ವಿಕರ್ಷಣೆಯನ್ನು ಅನುಭವಿಸುತ್ತವೆ. ಮೂರು ಕಡಿಮೆ ಶಕ್ತಿಯ ಕಕ್ಷೆಗಳನ್ನು ಹೀಗೆ ಗೊತ್ತುಪಡಿಸಲಾಗಿದೆ ಟಿ 2 ಗ್ರಾಂ, ಮತ್ತು ಎರಡು ಹೆಚ್ಚಿನ ರೀತಿಯೊಂದಿಗೆ ಇ ಜಿ.
ಮುಂದಿನವು ಸಾಮಾನ್ಯವಾಗಿದೆ ಟೆಟ್ರಾಹೆಡ್ರಲ್ನಾಲ್ಕು ಲಿಗಂಡ್ಗಳು ಲೋಹದ ಅಯಾನಿನ ಸುತ್ತಲೂ ಟೆಟ್ರಾಹೆಡ್ರಾನ್ ಅನ್ನು ರೂಪಿಸುವ ಸಂಕೀರ್ಣಗಳು. ಈ ವಿಷಯದಲ್ಲಿ ಡಿ-ಕಕ್ಷೆಗಳನ್ನು ಸಹ ಎರಡು ಗುಂಪುಗಳಾಗಿ ವಿಂಗಡಿಸಲಾಗಿದೆ ಮತ್ತು ಶಕ್ತಿಯ ಮಟ್ಟಗಳಲ್ಲಿ ವ್ಯತ್ಯಾಸವಿದೆ Δ tetr. ಆಕ್ಟಾಹೆಡ್ರಲ್ ಸಮನ್ವಯಕ್ಕಿಂತ ಭಿನ್ನವಾಗಿ, ಕಕ್ಷೆಗಳು ಕಡಿಮೆ ಶಕ್ತಿಯನ್ನು ಹೊಂದಿರುತ್ತವೆ ಡಿ z 2 ಮತ್ತು ಡಿ X 2 -ವೈ 2, ಮತ್ತು ಹೆಚ್ಚು - ಡಿ xy , ಡಿ xzಮತ್ತು ಡಿ yz. ಜೊತೆಗೆ, ಲಿಗಂಡ್ಗಳ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ನೇರವಾಗಿ ದಿಕ್ಕಿನಲ್ಲಿಲ್ಲದ ಕಾರಣ ಡಿ-ಕಕ್ಷೆಗಳು, ವಿಭಜಿಸುವ ಶಕ್ತಿಯು ಆಕ್ಟಾಹೆಡ್ರಲ್ ಸಮನ್ವಯಕ್ಕಿಂತ ಕಡಿಮೆ ಇರುತ್ತದೆ. TCP ಬಳಸಿಕೊಂಡು ನೀವು ವಿವರಿಸಬಹುದು ಪ್ಲಾನೋ-ಚದರಮತ್ತು ಸಂಕೀರ್ಣಗಳ ಇತರ ಜ್ಯಾಮಿತಿಗಳು.
ಕಕ್ಷೆಗಳ ಎರಡು ಅಥವಾ ಹೆಚ್ಚಿನ ಗುಂಪುಗಳ ನಡುವಿನ ಶಕ್ತಿಯ ಮಟ್ಟಗಳಲ್ಲಿನ ವ್ಯತ್ಯಾಸ Δ ಸಹ ಲಿಗಂಡ್ಗಳ ಸ್ವರೂಪವನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ. ಕೆಲವು ಲಿಗಂಡ್ಗಳು ಇತರರಿಗಿಂತ ಕಡಿಮೆ ಸೀಳನ್ನು ಉಂಟುಮಾಡುತ್ತವೆ, ಅದರ ಕಾರಣಗಳನ್ನು ವಿವರಿಸಲಾಗಿದೆ. ಸ್ಪೆಕ್ಟ್ರೋಕೆಮಿಕಲ್ ಸರಣಿ- ಪ್ರಾಯೋಗಿಕವಾಗಿ ಪಡೆದ ಲಿಗಂಡ್ಗಳ ಪಟ್ಟಿ, ಆರೋಹಣ ಕ್ರಮದಲ್ಲಿ Δ:
ಲೋಹದ ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿಯು Δ ಮೇಲೆ ಪರಿಣಾಮ ಬೀರುತ್ತದೆ. ಹೆಚ್ಚಿನ ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿಯನ್ನು ಹೊಂದಿರುವ ಲೋಹವು ದೊಡ್ಡ ಚಾರ್ಜ್ ವ್ಯತ್ಯಾಸದಿಂದಾಗಿ ಲಿಗಂಡ್ಗಳನ್ನು ಹತ್ತಿರಕ್ಕೆ ಆಕರ್ಷಿಸುತ್ತದೆ. ಲೋಹದ ಅಯಾನಿಗೆ ಹತ್ತಿರವಿರುವ ಲಿಗಂಡ್ಗಳು ಹೆಚ್ಚು ಸೀಳನ್ನು ಉಂಟುಮಾಡುತ್ತವೆ.
ಕಡಿಮೆ ಮತ್ತು ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳು[ | ]
ಪ್ರಮುಖ ಸೀಳನ್ನು ಉಂಟುಮಾಡುವ ಲಿಗಂಡ್ಗಳು ಡಿ CN− ಮತ್ತು CO ನಂತಹ -ಮಟ್ಟಗಳನ್ನು ಲಿಗಾಂಡ್ಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ ಬಲವಾದ ಕ್ಷೇತ್ರ. ಅಂತಹ ಲಿಗಂಡ್ಗಳೊಂದಿಗಿನ ಸಂಕೀರ್ಣಗಳಲ್ಲಿ, ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಹೆಚ್ಚಿನ ಶಕ್ತಿಯ ಕಕ್ಷೆಗಳನ್ನು ಆಕ್ರಮಿಸಿಕೊಳ್ಳುವುದು ಪ್ರತಿಕೂಲವಾಗಿದೆ. ಪರಿಣಾಮವಾಗಿ, ಹೆಚ್ಚಿನ ಶಕ್ತಿಯ ಕಕ್ಷೆಗಳು ತುಂಬಲು ಪ್ರಾರಂಭವಾಗುವ ಮೊದಲು ಕಡಿಮೆ ಶಕ್ತಿಯ ಕಕ್ಷೆಗಳು ಸಂಪೂರ್ಣವಾಗಿ ತುಂಬಿರುತ್ತವೆ. ಅಂತಹ ಸಂಕೀರ್ಣಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ಕಡಿಮೆ ಸ್ಪಿನ್. ಉದಾಹರಣೆಗೆ, NO 2 - ಒಂದು ಉನ್ನತ-ಕ್ಷೇತ್ರದ ಲಿಗಂಡ್ ಆಗಿದ್ದು ಅದು ದೊಡ್ಡ ವಿಭಜನೆಯನ್ನು ಉಂಟುಮಾಡುತ್ತದೆ. ಎಲ್ಲಾ 5 ಡಿ-ಆಕ್ಟಾಹೆಡ್ರಲ್ ಅಯಾನು 3- ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಕೆಳಮಟ್ಟದಲ್ಲಿರುತ್ತವೆ ಟಿ 2ಜಿ .
ಇದಕ್ಕೆ ವ್ಯತಿರಿಕ್ತವಾಗಿ, I− ಮತ್ತು Br− ನಂತಹ ಕಡಿಮೆ ಸೀಳನ್ನು ಉಂಟುಮಾಡುವ ಲಿಗಂಡ್ಗಳನ್ನು ಲಿಗಂಡ್ಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ದುರ್ಬಲ ಕ್ಷೇತ್ರ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಒಂದೇ ಕಡಿಮೆ ಶಕ್ತಿಯ ಕಕ್ಷೆಯಲ್ಲಿ ಇರಿಸುವುದಕ್ಕಿಂತ ಹೆಚ್ಚಿನ ಶಕ್ತಿಯ ಕಕ್ಷೆಗಳಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಇಡುವುದು ಸುಲಭ, ಏಕೆಂದರೆ ಒಂದೇ ಕಕ್ಷೆಯಲ್ಲಿರುವ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಪರಸ್ಪರ ಹಿಮ್ಮೆಟ್ಟಿಸುತ್ತದೆ ಮತ್ತು ಎರಡನೇ ಎಲೆಕ್ಟ್ರಾನ್ ಅನ್ನು ಕಕ್ಷೆಯಲ್ಲಿ ಇರಿಸುವ ಶಕ್ತಿಯ ವೆಚ್ಚವು Δ ಗಿಂತ ಹೆಚ್ಚು. ಹೀಗೆ, ಜೋಡಿಯಾಗಿರುವ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಕಾಣಿಸಿಕೊಳ್ಳುವ ಮೊದಲು, ಪ್ರತಿ ಐದರಲ್ಲಿ ಡಿ-ಕಕ್ಷೆಗಳನ್ನು ಹಂಡ್ ನಿಯಮಕ್ಕೆ ಅನುಗುಣವಾಗಿ ಒಂದು ಬಾರಿಗೆ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ಇರಿಸಬೇಕು. ಅಂತಹ ಸಂಕೀರ್ಣಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ಹೆಚ್ಚಿನ ಸ್ಪಿನ್. ಉದಾಹರಣೆಗೆ, Br− ಒಂದು ದುರ್ಬಲ-ಕ್ಷೇತ್ರದ ಲಿಗಂಡ್ ಆಗಿದ್ದು ಅದು ಸ್ವಲ್ಪ ವಿಭಜನೆಯನ್ನು ಉಂಟುಮಾಡುತ್ತದೆ. ಎಲ್ಲಾ 5 ಡಿ 5 ಅನ್ನು ಹೊಂದಿರುವ 3− ಅಯಾನಿನ ಕಕ್ಷೆಗಳು ಡಿ- ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ನಿಂದ ಆಕ್ರಮಿಸಲ್ಪಡುತ್ತವೆ.
ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳಿಗೆ ವಿಭಜಿಸುವ ಶಕ್ತಿಯು Δ tetr ಸರಿಸುಮಾರು 4/9Δ oct (ಅದೇ ಲೋಹ ಮತ್ತು ಲಿಗಂಡ್ಗಳಿಗೆ) ಸಮಾನವಾಗಿರುತ್ತದೆ. ಪರಿಣಾಮವಾಗಿ, ಶಕ್ತಿಯ ಮಟ್ಟದಲ್ಲಿ ವ್ಯತ್ಯಾಸ ಡಿ-ಕಕ್ಷೆಗಳು ಸಾಮಾನ್ಯವಾಗಿ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಸುವ ಶಕ್ತಿಗಿಂತ ಕೆಳಗಿರುತ್ತವೆ ಮತ್ತು ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣಗಳು ಸಾಮಾನ್ಯವಾಗಿ ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ ಆಗಿರುತ್ತವೆ.
ವಿತರಣಾ ರೇಖಾಚಿತ್ರಗಳು ಡಿ- ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಸಮನ್ವಯ ಸಂಯುಕ್ತಗಳ ಕಾಂತೀಯ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಊಹಿಸಲು ಸಾಧ್ಯವಾಗಿಸುತ್ತದೆ. ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳೊಂದಿಗಿನ ಸಂಕೀರ್ಣಗಳು ಪ್ಯಾರಾಮ್ಯಾಗ್ನೆಟಿಕ್ ಮತ್ತು ಕಾಂತೀಯ ಕ್ಷೇತ್ರದಿಂದ ಆಕರ್ಷಿತವಾಗುತ್ತವೆ, ಆದರೆ ಇಲ್ಲದ ಸಂಕೀರ್ಣಗಳು ಡಯಾಮ್ಯಾಗ್ನೆಟಿಕ್ ಮತ್ತು ದುರ್ಬಲವಾಗಿ ಹಿಮ್ಮೆಟ್ಟಿಸುತ್ತದೆ.
ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದ ಸ್ಥಿರೀಕರಣ ಶಕ್ತಿ[ | ]
ಕ್ರಿಸ್ಟಲ್ ಫೀಲ್ಡ್ ಸ್ಟೆಬಿಲೈಸೇಶನ್ ಎನರ್ಜಿ (CFE) ಕಕ್ಷೆಗಳ ಸರಾಸರಿ ಶಕ್ತಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಪರಿವರ್ತನೆಯ ಲೋಹದ ಅಯಾನಿನ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸಂರಚನೆಯ ಶಕ್ತಿಯಾಗಿದೆ. ಲಿಗಾಂಡ್ ಕ್ಷೇತ್ರದಲ್ಲಿ ಕೆಲವು ಕಕ್ಷೆಗಳ ಶಕ್ತಿಯ ಮಟ್ಟವು ಕಾಲ್ಪನಿಕ ಗೋಳಾಕಾರದ ಕ್ಷೇತ್ರಕ್ಕಿಂತ ಕಡಿಮೆಯಿರುವುದರಿಂದ ಸ್ಥಿರೀಕರಣವು ಸಂಭವಿಸುತ್ತದೆ, ಇದರಲ್ಲಿ ಎಲ್ಲಾ ಐದು ಡಿ-ಕಕ್ಷೆಗಳು ಒಂದೇ ವಿಕರ್ಷಣ ಬಲವನ್ನು ಹೊಂದಿವೆ, ಮತ್ತು ಎಲ್ಲಾ ಡಿ-ಕಕ್ಷೆಗಳು ಕ್ಷೀಣಗೊಳ್ಳುತ್ತವೆ. ಉದಾಹರಣೆಗೆ, ಆಕ್ಟಾಹೆಡ್ರಲ್ ಸಂದರ್ಭದಲ್ಲಿ ಮಟ್ಟ ಟಿ 2 ಗ್ರಾಂಗೋಳಾಕಾರದ ಕ್ಷೇತ್ರದಲ್ಲಿ ಸರಾಸರಿ ಮಟ್ಟಕ್ಕಿಂತ ಕಡಿಮೆ. ಪರಿಣಾಮವಾಗಿ, ಈ ಕಕ್ಷೆಗಳು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿದ್ದರೆ, ಲೋಹದ ಅಯಾನು ಗೋಳಾಕಾರದ ಕ್ಷೇತ್ರಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರದಲ್ಲಿ ಹೆಚ್ಚು ಸ್ಥಿರವಾಗಿರುತ್ತದೆ. ಇದಕ್ಕೆ ವಿರುದ್ಧವಾಗಿ, ಕಕ್ಷೆಗಳ ಶಕ್ತಿಯ ಮಟ್ಟ ಇ ಜಿಸರಾಸರಿಗಿಂತ ಹೆಚ್ಚು, ಮತ್ತು ಅವುಗಳಲ್ಲಿ ಒಳಗೊಂಡಿರುವ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಸ್ಥಿರೀಕರಣವನ್ನು ಕಡಿಮೆ ಮಾಡುತ್ತದೆ.
ಆಕ್ಟಾಹೆಡ್ರಲ್ ಕ್ಷೇತ್ರದಿಂದ ಸ್ಥಿರೀಕರಣದ ಶಕ್ತಿ
ಅಷ್ಟಮುಖ ಕ್ಷೇತ್ರದಲ್ಲಿ ಮೂರು ಕಕ್ಷೆಗಳಿವೆ ಟಿ 2 ಗ್ರಾಂ 2/5 Δ ಆಕ್ಟೇವ್ ಮತ್ತು ಎರಡು ಕಕ್ಷೆಗಳಿಂದ ಸರಾಸರಿ ಶಕ್ತಿಯ ಮಟ್ಟಕ್ಕೆ ಹೋಲಿಸಿದರೆ ಸ್ಥಿರವಾಗಿದೆ ಇ ಜಿ 3/5 Δ ಅಕ್ಟೋಬರ್ನಿಂದ ಅಸ್ಥಿರಗೊಳಿಸಲಾಗಿದೆ. ಮೇಲೆ ಎರಡು ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಕಾನ್ಫಿಗರೇಶನ್ಗಳ ಉದಾಹರಣೆಗಳಿವೆ ಡಿ 5 . ಮೊದಲ ಉದಾಹರಣೆಯಲ್ಲಿ, ಐದು ಎಲೆಕ್ಟ್ರಾನ್ಗಳೊಂದಿಗೆ ಕಡಿಮೆ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣ 3− ಇದೆ ಟಿ 2 ಗ್ರಾಂ. ಇದರ ESP 5 × 2 / 5 Δ oct = 2Δ oct. ಎರಡನೆಯ ಉದಾಹರಣೆಯಲ್ಲಿ, ESKP (3 × 2 / 5 Δ oct) - (2 × 3 / 5 Δ oct) = 0 ನೊಂದಿಗೆ ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ ಸಂಕೀರ್ಣ 3- ಈ ಸಂದರ್ಭದಲ್ಲಿ, ಕಡಿಮೆ ಮಟ್ಟದ ಕಕ್ಷೆಗಳಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸ್ಥಿರಗೊಳಿಸುವ ಪರಿಣಾಮ ಉನ್ನತ ಮಟ್ಟದ ಕಕ್ಷೆಗಳಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಅಸ್ಥಿರಗೊಳಿಸುವ ಪರಿಣಾಮದಿಂದ ತಟಸ್ಥಗೊಂಡಿದೆ.
ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದಿಂದ ಡಿ-ಲೆವೆಲ್ ವಿಭಜನೆಯ ರೇಖಾಚಿತ್ರಗಳು[ | ]
| ಅಷ್ಟಮುಖಿ | ಪೆಂಟಗೋನಲ್-ಬೈಪಿರಮಿಡ್ | ಚದರ-ಆಂಟಿಪ್ರಿಸ್ಮ್ಯಾಟಿಕ್ |
|---|---|---|
ಕ್ರಿಸ್ಟಲ್ ಫೀಲ್ಡ್ ಸಿದ್ಧಾಂತ 20 ನೇ ಶತಮಾನದ 40 ರ ದಶಕದಲ್ಲಿ ವೇಲೆನ್ಸಿ ಬಾಂಡ್ಗಳ ಸಿದ್ಧಾಂತವನ್ನು ಬದಲಾಯಿಸಿತು. ಅದರ ಶುದ್ಧ ರೂಪದಲ್ಲಿ, ಇದನ್ನು ಪ್ರಸ್ತುತ ಬಳಸಲಾಗುವುದಿಲ್ಲ, ಏಕೆಂದರೆ ಇದು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಕೋವೆಲನ್ಸಿಯ ಬಂಧಗಳ ರಚನೆಯನ್ನು ವಿವರಿಸಲು ಸಾಧ್ಯವಿಲ್ಲ ಮತ್ತು ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಸಂದರ್ಭದಲ್ಲಿ ಸಹ ಲಿಗಂಡ್ಗಳ ನಿಜವಾದ ಸ್ಥಿತಿಯನ್ನು (ಉದಾಹರಣೆಗೆ, ಅವುಗಳ ನಿಜವಾದ ಗಾತ್ರಗಳು) ಗಣನೆಗೆ ತೆಗೆದುಕೊಳ್ಳುವುದಿಲ್ಲ. ಸಂಪೂರ್ಣವಾಗಿ ಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ ಗೆ.
ಈಗಾಗಲೇ 50 ರ ದಶಕದ ಮಧ್ಯಭಾಗದಲ್ಲಿ, ಸರಳೀಕೃತ ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದ ಸಿದ್ಧಾಂತವನ್ನು ಸುಧಾರಿತವಾಗಿ ಬದಲಾಯಿಸಲಾಯಿತು. ಲಿಗಂಡ್ ಕ್ಷೇತ್ರ ಸಿದ್ಧಾಂತ, ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಮತ್ತು ಲಿಗಂಡ್ ನಡುವಿನ ರಾಸಾಯನಿಕ ಬಂಧಗಳ ಕೋವೆಲನ್ಸಿಯ ಸ್ವಭಾವವನ್ನು ಗಣನೆಗೆ ತೆಗೆದುಕೊಳ್ಳುವುದು.
ಆದಾಗ್ಯೂ, ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳ ರಚನೆಯನ್ನು ವಿವರಿಸುವ ಸಾಮಾನ್ಯ ವಿಧಾನವನ್ನು ನೀಡಲಾಗಿದೆ ಆಣ್ವಿಕ ಕಕ್ಷೀಯ ಸಿದ್ಧಾಂತ(MO), ಇದು ಪ್ರಸ್ತುತ ಎಲ್ಲಕ್ಕಿಂತ ಮೇಲುಗೈ ಸಾಧಿಸುತ್ತದೆ. ಆಣ್ವಿಕ ಕಕ್ಷೀಯ ವಿಧಾನವು ಅತಿಕ್ರಮಿಸುವ ಪರಮಾಣು ಕಕ್ಷೆಗಳ ಅನುಪಸ್ಥಿತಿಯಲ್ಲಿ ಸಂಪೂರ್ಣವಾಗಿ ಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ ಪರಸ್ಪರ ಕ್ರಿಯೆಯನ್ನು ಒದಗಿಸುತ್ತದೆ, ಮತ್ತು ಅತಿಕ್ರಮಣದ ಮಧ್ಯಂತರ ಡಿಗ್ರಿಗಳ ಸಂಪೂರ್ಣ ಸೆಟ್.
ಮೂಲ ಪರಿಕಲ್ಪನೆಗಳನ್ನು ನೋಡೋಣ ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದ ಸಿದ್ಧಾಂತ, ವೇಲೆನ್ಸಿ ಬಾಂಡ್ಗಳ ಸಿದ್ಧಾಂತದಂತೆ, ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳಲ್ಲಿನ ರಾಸಾಯನಿಕ ಬಂಧಗಳ ಗುಣಾತ್ಮಕ ವಿವರಣೆಗಾಗಿ ಅದರ ಮಹತ್ವವನ್ನು ಅದರ ಸರಳತೆ ಮತ್ತು ಸ್ಪಷ್ಟತೆಯಿಂದಾಗಿ ಇನ್ನೂ ಉಳಿಸಿಕೊಂಡಿದೆ.
ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರ ಸಿದ್ಧಾಂತದಲ್ಲಿ, ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಮತ್ತು ಲಿಗಂಡ್ ನಡುವಿನ ರಾಸಾಯನಿಕ ಬಂಧವನ್ನು ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ ಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ. ಈ ಸಿದ್ಧಾಂತದ ಪ್ರಕಾರ, ಲಿಗಂಡ್ಗಳು ಸಾಮಾನ್ಯ ಪಾಲಿಹೆಡ್ರಾದ ಶೃಂಗಗಳಲ್ಲಿ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಸುತ್ತಲೂ ನೆಲೆಗೊಂಡಿವೆ ( ಬಹುಮುಖಿ) ನಂತೆ ಪಾಯಿಂಟ್ ಶುಲ್ಕಗಳು. ಸಿದ್ಧಾಂತವು ಲಿಗಂಡ್ನ ನಿಜವಾದ ಪರಿಮಾಣವನ್ನು ಗಣನೆಗೆ ತೆಗೆದುಕೊಳ್ಳುವುದಿಲ್ಲ.
ಲಿಗಂಡ್ಗಳು, ಪಾಯಿಂಟ್ ಚಾರ್ಜ್ಗಳಂತೆ, ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಸುತ್ತಲೂ ರಚಿಸುತ್ತವೆ ಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ ಕ್ಷೇತ್ರ("ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರ", ನಾವು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತದ ಸ್ಫಟಿಕವನ್ನು ಪರಿಗಣಿಸಿದರೆ, ಅಥವಾ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರ), ಇದರಲ್ಲಿ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಶಕ್ತಿಯ ಮಟ್ಟಗಳು ಮತ್ತು, ಎಲ್ಲಕ್ಕಿಂತ ಹೆಚ್ಚಾಗಿ, ಡಿ-ಉಪಮಟ್ಟಗಳು ವಿಭಜನೆಯಾಗುತ್ತಿವೆ, ಮತ್ತು ಅವರ ಶಕ್ತಿಯ ಬದಲಾವಣೆಗಳು. ವಿಭಜನೆಯ ಸ್ವರೂಪ, ಹೊಸ ಶಕ್ತಿಯ ಮಟ್ಟಗಳ ಶಕ್ತಿ ಅವಲಂಬಿಸಿರುತ್ತದೆ ಸಮ್ಮಿತಿಲಿಗಂಡ್ಗಳ ವ್ಯವಸ್ಥೆ (ಆಕ್ಟಾಹೆಡ್ರಲ್, ಟೆಟ್ರಾಹೆಡ್ರಲ್ ಅಥವಾ ಇತರ ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರ). H 2 O, NH 3, CO ಮತ್ತು ಇತರ ಅಣುಗಳನ್ನು ಲಿಗಂಡ್ಗಳಾಗಿ ಸಂಯೋಜಿಸಿದಾಗ, ಅವುಗಳನ್ನು ಹೀಗೆ ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ ದ್ವಿಧ್ರುವಿಗಳು, ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಕಡೆಗೆ ಋಣಾತ್ಮಕ ಚಾರ್ಜ್ನೊಂದಿಗೆ ಆಧಾರಿತವಾಗಿದೆ.
ಲಿಗಂಡ್ಗಳ ಆಕ್ಟಾಹೆಡ್ರಲ್ ಜೋಡಣೆಯ ಪ್ರಕರಣವನ್ನು ಪರಿಗಣಿಸಿ (ಉದಾಹರಣೆಗೆ, -3 ಅಥವಾ 3+). ಆಕ್ಟಾಹೆಡ್ರಾನ್ನ ಮಧ್ಯದಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳೊಂದಿಗೆ ಸಂಕೀರ್ಣ ಅಯಾನು M(+ n) ಇದೆ ಡಿಪರಮಾಣು ಕಕ್ಷೆಗಳು, ಮತ್ತು ಅದರ ಶೃಂಗಗಳಲ್ಲಿ ಪಾಯಿಂಟ್ ಋಣಾತ್ಮಕ ಶುಲ್ಕಗಳ ರೂಪದಲ್ಲಿ ಲಿಗಂಡ್ಗಳಿವೆ (ಉದಾಹರಣೆಗೆ, F - ಅಯಾನುಗಳು ಅಥವಾ NH 3 ನಂತಹ ಧ್ರುವ ಅಣುಗಳು). ಸಾಂಪ್ರದಾಯಿಕ ಅಯಾನು M(+ n), ಲಿಗಂಡ್ಗಳೊಂದಿಗೆ ಸಂಬಂಧ ಹೊಂದಿಲ್ಲ, ಎಲ್ಲಾ ಐದರ ಶಕ್ತಿಗಳು ಡಿ-AO ಒಂದೇ (ಅಂದರೆ ಪರಮಾಣು ಕಕ್ಷೆಗಳು ಅವನತಿ ಹೊಂದುತ್ತವೆ).
ಆದಾಗ್ಯೂ, ಲಿಗಂಡ್ಗಳ ಅಷ್ಟಹೆಡ್ರಲ್ ಕ್ಷೇತ್ರದಲ್ಲಿ ಡಿಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ AO ಗಳು ಸೇರುತ್ತವೆ ಅಸಮಾನಸ್ಥಾನ. ಪರಮಾಣು ಕಕ್ಷೆಗಳು ಡಿ(z 2) ಮತ್ತು d(x 2 -y 2), ನಿರ್ದೇಶಾಂಕ ಅಕ್ಷಗಳ ಉದ್ದಕ್ಕೂ ಉದ್ದವಾಗಿದ್ದು, ಲಿಗಂಡ್ಗಳಿಗೆ ಹತ್ತಿರಕ್ಕೆ ಬರುತ್ತವೆ. ಈ ಕಕ್ಷೆಗಳು ಮತ್ತು ಆಕ್ಟಾಹೆಡ್ರನ್ನ ಶೃಂಗಗಳಲ್ಲಿರುವ ಲಿಗಂಡ್ಗಳ ನಡುವೆ ಗಮನಾರ್ಹ ವ್ಯತ್ಯಾಸಗಳು ಉದ್ಭವಿಸುತ್ತವೆ. ವಿಕರ್ಷಣ ಶಕ್ತಿಗಳು, ಕಕ್ಷೀಯ ಶಕ್ತಿಯ ಹೆಚ್ಚಳಕ್ಕೆ ಕಾರಣವಾಗುತ್ತದೆ. ಬೇರೆ ರೀತಿಯಲ್ಲಿ ಹೇಳುವುದಾದರೆ, ಈ ಪರಮಾಣು ಕಕ್ಷೆಗಳು ಒಳಪಟ್ಟಿರುತ್ತವೆ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರಕ್ಕೆ ಗರಿಷ್ಠ ಮಾನ್ಯತೆ. ಬಲವಾಗಿ ಸಂಕುಚಿತ ವಸಂತವು ಅಂತಹ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಭೌತಿಕ ಮಾದರಿಯಾಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸುತ್ತದೆ.
ಇತರೆ ಮೂರು ಡಿ-AO - ಡಿ(xy), ಡಿ(xz) ಮತ್ತು ಡಿ(yz), ನಿರ್ದೇಶಾಂಕ ಅಕ್ಷಗಳ ನಡುವೆ ಮತ್ತು ಲಿಗಂಡ್ಗಳ ನಡುವೆ ಇದೆ, ಅವುಗಳಿಂದ ಹೆಚ್ಚಿನ ದೂರದಲ್ಲಿವೆ. ಅಂತಹವರ ಪರಸ್ಪರ ಕ್ರಿಯೆ ಡಿಲಿಗಂಡ್ಗಳೊಂದಿಗಿನ AO ಕಡಿಮೆ ಮತ್ತು ಆದ್ದರಿಂದ ಶಕ್ತಿ ಡಿ(xy), ಡಿ(xz) ಮತ್ತು ಡಿ(yz)-AO ಮೂಲಕ್ಕೆ ಹೋಲಿಸಿದರೆ ಕಡಿಮೆಯಾಗುತ್ತದೆ.
ಹೀಗಾಗಿ, ಐದು ಪಟ್ಟು ಅವನತಿ ಡಿ-AO ಸಂಕೀರ್ಣ ಏಜೆಂಟ್, ಒಳಗೆ ಬರುವುದು ಆಕ್ಟಾಹೆಡ್ರಲ್ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರ, ಬಹಿರಂಗ ವಿಭಜನೆಹೊಸ ಕಕ್ಷೆಗಳ ಎರಡು ಗುಂಪುಗಳಾಗಿ - ಮೂರು ಬಾರಿ ಕ್ಷೀಣಿಸುವ ಕಕ್ಷೆಗಳುಕಡಿಮೆ ಶಕ್ತಿಯೊಂದಿಗೆ, ಡಿ(xy), ಡಿ(xz) ಮತ್ತು ಡಿ(yz), ಮತ್ತು ದ್ವಿಗುಣವಾಗಿ ಕ್ಷೀಣಿಸುವ ಕಕ್ಷೆಗಳುಹೆಚ್ಚಿನ ಶಕ್ತಿಯೊಂದಿಗೆ ಡಿ(z 2) ಮತ್ತು d(x 2 -y 2). ಈ ಹೊಸ ಗುಂಪುಗಳು ಡಿ- ಜೊತೆ ಕಕ್ಷೆಗಳು ಕಡಿಮೆಮತ್ತು ಹೆಚ್ಚಿನ ಶಕ್ತಿಸೂಚಿಸುತ್ತವೆ ಡಿε ಮತ್ತು ಡಿγ:
ಡಿ(z 2) ಮತ್ತು d(x 2 -y 2)
ಡಿ(xy), ಡಿ(xz),ಡಿ(yz)
ಶಕ್ತಿ ವ್ಯತ್ಯಾಸಎರಡು ಹೊಸ ಉಪಹಂತಗಳು ಡಿε ಮತ್ತು ಡಿγ ಎಂದು ಹೆಸರಿಸಲಾಯಿತು ವಿಭಜಿಸುವ ನಿಯತಾಂಕ Δ 0:
ಇ 2 – ಇ 1 = Δ 0 ≈ 0
ಎರಡು ಹೊಸ ಸ್ಥಳ ಶಕ್ತಿಯ ಉಪಮಟ್ಟಗಳು ಡಿε ಮತ್ತು ಡಿγ ಮೂಲಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ ( ಡಿ-AO) ಶಕ್ತಿಯ ರೇಖಾಚಿತ್ರದಲ್ಲಿ ಅಸಮವಾದ:
(ಇ 2 – ಇ 0) > (ಇ 0 – ಇ 1).
ಕ್ವಾಂಟಮ್ ಯಾಂತ್ರಿಕ ಸಿದ್ಧಾಂತಅದು ಅಗತ್ಯವಿದೆ ಹೊಸ ಶಕ್ತಿಯ ಮಟ್ಟಗಳು ಸಂಪೂರ್ಣವಾಗಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ತುಂಬಿದಾಗ, ಒಟ್ಟು ಶಕ್ತಿಯು ಬದಲಾಗದೆ ಉಳಿಯುತ್ತದೆ, ಅಂದರೆ ಅವಳು ಉಳಿಯಬೇಕು ಸಮಾನವಾಗಿರುತ್ತದೆ ಇ 0 .
ಬೇರೆ ರೀತಿಯಲ್ಲಿ ಹೇಳುವುದಾದರೆ, ಸಮಾನತೆಯನ್ನು ತೃಪ್ತಿಪಡಿಸಬೇಕು
4(ಇ 2 – ಇ 0) = 6(ಇ 0 – ಇ 1),
ಅಲ್ಲಿ 4 ಮತ್ತು 6 - ಗರಿಷ್ಠಪ್ರತಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆ ಡಿγ- ಮತ್ತು ಡಿε-AO. ಈ ಸಮಾನತೆಯಿಂದ ಅದು ಅನುಸರಿಸುತ್ತದೆ
(ಇ 2 – ಇ 0) / (ಇ 0 – ಇ 1) = 3/2 ಮತ್ತು
(ಇ 2 – ಇ 1) / (ಇ 0 – ಇ 1) = 5/2, ಅಥವಾ
Δ 0 / ( ಇ 0 – ಇ 1) = 5/2, ಎಲ್ಲಿಂದ ( ಇ 0 – ಇ 1) = 2/5Δ 0 .
ಸಾಧ್ಯವಿರುವ ಗರಿಷ್ಠ ಆರು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಪ್ರತಿ ಎಲೆಕ್ಟ್ರಾನ್ನಲ್ಲಿ ಇರಿಸುವುದು ಡಿε ಕಕ್ಷೆಗಳು ಕಾರಣವಾಗುತ್ತವೆ ಇಳಿಕೆ (ಗೆಲುವುಗಳು) ಶಕ್ತಿ 2/5 Δ 0 ಮೂಲಕ.
ಇದಕ್ಕೆ ತದ್ವಿರುದ್ಧವಾಗಿ, ಪ್ರತಿ ಎಲೆಕ್ಟ್ರಾನ್ನ ಸ್ಥಾನವನ್ನು ನಾಲ್ಕರಲ್ಲಿ ಸಾಧ್ಯ ಡಿγ ಕಕ್ಷೆಗಳು ಕಾರಣವಾಗುತ್ತವೆ ಹೆಚ್ಚಳ (ವೆಚ್ಚ) ಶಕ್ತಿ 3/5 Δ 0 ಮೂಲಕ.
ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ತುಂಬಿದ್ದರೆ ಡಿε- ಮತ್ತು ಡಿγ-ಕಕ್ಷೆಗಳು ಸಂಪೂರ್ಣವಾಗಿ, ನಂತರ ಇಲ್ಲ ವಿಜೇತಶಕ್ತಿ ಇಲ್ಲ(ಹಾಗೆಯೇ ಆಗುವುದಿಲ್ಲ ಹೆಚ್ಚುವರಿ ಶಕ್ತಿಯ ಬಳಕೆ).
ಆದರೆ ಮೂಲ ವೇಳೆ ಡಿ-AO ಮಾತ್ರ ಜನಸಂಖ್ಯೆ ಹೊಂದಿದೆ ಭಾಗಶಃಮತ್ತು 1 ರಿಂದ 6 ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ ಮತ್ತು ಈ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಮಾತ್ರ ಇರಿಸಲಾಗುತ್ತದೆ ಡಿε-AO, ನಂತರ ನಾವು ಪಡೆಯುತ್ತೇವೆ ಗಮನಾರ್ಹ ಶಕ್ತಿಯ ಲಾಭ.
ಕಾರಣ ಶಕ್ತಿಯ ಲಾಭ ಆದ್ಯತೆಯ ವಸಾಹತುಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಡಿε- ಪರಮಾಣು ಕಕ್ಷೆಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರದಿಂದ ಸಂಕೀರ್ಣದ ಸ್ಥಿರೀಕರಣದ ಶಕ್ತಿ.
ಪ್ರತಿ ಲಿಗಂಡ್ನ ನಿರ್ದಿಷ್ಟತೆಯು ಈ ಲಿಗಂಡ್ ರಚಿಸುವ ಕ್ಷೇತ್ರದ ಮೇಲೆ ಪರಿಣಾಮ ಬೀರುತ್ತದೆ - ಬಲವಾದಅಥವಾ ದುರ್ಬಲ. ಹೇಗೆ ಬಲವಾದ ಕ್ಷೇತ್ರಲಿಗಂಡ್ಗಳಿಗಿಂತ ಹೆಚ್ಚುಅರ್ಥ ವಿಭಜಿಸುವ ನಿಯತಾಂಕ Δ 0 .
ವಿಭಜಿಸುವ ನಿಯತಾಂಕದ ಅಧ್ಯಯನವು ಸಾಮಾನ್ಯವಾಗಿ ಆಧರಿಸಿದೆ ಸ್ಪೆಕ್ಟ್ರೋಸ್ಕೋಪಿಕ್ಸಂಶೋಧನೆ. ತರಂಗಾಂತರಗಳು ಹೀರಿಕೊಳ್ಳುವ ಬ್ಯಾಂಡ್ಗಳುಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವರ್ಗಾವಣೆಯಿಂದಾಗಿ ಸ್ಫಟಿಕದಂತಹ ಸ್ಥಿತಿಯಲ್ಲಿ ಅಥವಾ ದ್ರಾವಣದಲ್ಲಿ ಸಂಕೀರ್ಣಗಳು ಡಿε- ರಂದು ಡಿγ-AO, ಸಂಬಂಧಿಸಿದೆ ವಿಭಜಿಸುವ ನಿಯತಾಂಕΔ 0 ಕೆಳಗಿನಂತೆ:
λ = ಸಿ / ν; Δ 0 = ಇ 2 – ಇ 1 = ಗಂ ν = ಗಂ · ( ಸಿ / λ),
ಪ್ಲ್ಯಾಂಕ್ನ ಸ್ಥಿರತೆ ಎಲ್ಲಿದೆ ಗಂಸಮಾನ 6.6260693 ∙ 10 -34 J s;
ಬೆಳಕಿನ ವೇಗ ಜೊತೆಗೆ
= 3 · 10 10 cm/s.
ಘಟಕΔ 0 ತರಂಗ ಸಂಖ್ಯೆಯಂತೆಯೇ ಇರುತ್ತದೆ: cm -1, ಇದು ಸರಿಸುಮಾರು 12 J/mol ಗೆ ಅನುರೂಪವಾಗಿದೆ. ವಿಭಜಿಸುವ ನಿಯತಾಂಕ, ಲಿಗಂಡ್ ಪ್ರಕಾರದ ಜೊತೆಗೆ, ಅವಲಂಬಿಸಿರುತ್ತದೆ ಆಕ್ಸಿಡೀಕರಣದ ಮಟ್ಟದಲ್ಲಿಮತ್ತು ಪ್ರಕೃತಿಸಂಕೀರ್ಣ ಏಜೆಂಟ್.
ಅದೇ ಅವಧಿಯ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಮತ್ತು ಅದೇ ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿಯಲ್ಲಿ, ಅದೇ ಲಿಗಂಡ್ಗಳೊಂದಿಗೆ, ಸೀಳುವಿಕೆಯ ನಿಯತಾಂಕವು ಸರಿಸುಮಾರು ಒಂದೇ ಆಗಿರುತ್ತದೆ. ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಆಕ್ಸಿಡೀಕರಣದ ಹೆಚ್ಚುತ್ತಿರುವ ಮಟ್ಟದೊಂದಿಗೆ, ಮೌಲ್ಯ Δ 0 ಹೆಚ್ಚಾಗುತ್ತದೆ. ಹೀಗಾಗಿ, ಆಕ್ವಾ ಸಂಕೀರ್ಣಗಳು 2+ ಮತ್ತು 2+ ಗೆ ವಿಭಜಿಸುವ ನಿಯತಾಂಕದ ಮೌಲ್ಯವು 7800 ಮತ್ತು 10400 cm -1, ಮತ್ತು 3+ ಮತ್ತು +3 13700 ಮತ್ತು 21000 cm -1, ಕ್ರಮವಾಗಿ. ನಲ್ಲಿ ಹೆಚ್ಚುತ್ತಿರುವ ಪರಮಾಣು ಚಾರ್ಜ್ಸಂಕೀರ್ಣ-ರೂಪಿಸುವ ಪರಮಾಣುವಿನ Δ 0 ಸಹ ಹೆಚ್ಚಾಗುತ್ತದೆ. ಹೆಕ್ಸಾಮಿನಿರಿಡಿಯಮ್(III) 3+, ಹೆಕ್ಸಾಮಿನಿರಿಡಿಯಮ್(III) 3+, ಮತ್ತು ಹೆಕ್ಸಾಮಿನಿರಿಡಿಯಮ್(III) 3+ ಕ್ಯಾಟಯಾನ್ಗಳು ( Z= 27, 45 ಮತ್ತು 77) 22900, 34100 ಮತ್ತು 41000 cm -1 ಗೆ ಸಮಾನವಾದ ವಿಭಜಿಸುವ ನಿಯತಾಂಕಗಳಿಂದ ನಿರೂಪಿಸಲಾಗಿದೆ.
ಲಿಗಂಡ್ಗಳ ಸ್ವಭಾವದ ಮೇಲೆ Δ 0 ಅವಲಂಬನೆಯು ಹೆಚ್ಚು ವೈವಿಧ್ಯಮಯವಾಗಿದೆ. ಹಲವಾರು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳ ಅಧ್ಯಯನದ ಪರಿಣಾಮವಾಗಿ, ಅವುಗಳ ಸಾಮಾನ್ಯ ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿಯಲ್ಲಿರುವ ಸಂಕೀರ್ಣ ಲೋಹಗಳ ಸೀಳುವಿಕೆಯ ನಿಯತಾಂಕವನ್ನು ಹೆಚ್ಚಿಸುವ ಸಾಮರ್ಥ್ಯದ ದೃಷ್ಟಿಯಿಂದ, ಸಾಮಾನ್ಯ ಲಿಗಂಡ್ಗಳನ್ನು ಈ ಕೆಳಗಿನಂತೆ ಜೋಡಿಸಬಹುದು ಎಂದು ಕಂಡುಬಂದಿದೆ. ಸ್ಪೆಕ್ಟ್ರೋಕೆಮಿಕಲ್ ಸರಣಿ, ಇದರೊಂದಿಗೆ ಮೌಲ್ಯ Δ 0 ಏಕತಾನತೆಯಿಂದ ಹೆಚ್ಚಾಗುತ್ತದೆ:
I > Br > Cl > NCS - ≈ NO 3 - > F - > OH - > H 2 O > H - > NH 3 > NO 2 - > CN - > NO > CO.
ಹೀಗಾಗಿ, ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಸುತ್ತಲೂ ಪ್ರಬಲವಾದ ಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ ಕ್ಷೇತ್ರ ಮತ್ತು ಪ್ರಬಲವಾದ ಸೀಳು ಡಿ-AO ಲಿಗಂಡ್ಗಳು CN-, NO ಮತ್ತು CO ನಿಂದ ಉಂಟಾಗುತ್ತದೆ. ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿತರಣೆಯನ್ನು ನಾವು ಪರಿಗಣಿಸೋಣ ಡಿε- ಮತ್ತು ಡಿಲಿಗಂಡ್ಗಳ ಅಷ್ಟಮುಖ ಕ್ಷೇತ್ರದಲ್ಲಿ γ-ಕಕ್ಷೆಗಳು. ಚೆಕ್-ಇನ್ ಡಿε- ಮತ್ತು ಡಿγ-ಕಕ್ಷೆಗಳು ಪೂರ್ಣ ಅನುಸಾರವಾಗಿ ಸಂಭವಿಸುತ್ತವೆ ಹುಂಡ್ ನಿಯಮಮತ್ತು ಪೌಲಿ ತತ್ವ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ವಿಭಜಿಸುವ ನಿಯತಾಂಕದ ಮೌಲ್ಯವನ್ನು ಲೆಕ್ಕಿಸದೆ, ಮೊದಲ ಮೂರು ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಕ್ವಾಂಟಮ್ ಕೋಶಗಳಿಂದ ಆಕ್ರಮಿಸಲ್ಪಡುತ್ತವೆ ಡಿε-ಉಪಮಟ್ಟದ:
![]() dε
dε
ಒಂದು ವೇಳೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆ ಶೇ ಡಿ- ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಮೂರು ಉಪ-ಹಂತಗಳಿವೆ; ಅವುಗಳನ್ನು ವಿಭಜಿತ ಉಪ ಹಂತಗಳಲ್ಲಿ ಇರಿಸಲು ಎರಡು ಸಾಧ್ಯತೆಗಳಿವೆ. ವಿಭಜಿಸುವ ನಿಯತಾಂಕದ ಕಡಿಮೆ ಮೌಲ್ಯದಲ್ಲಿ (ಲಿಗಂಡ್ಗಳ ದುರ್ಬಲ ಕ್ಷೇತ್ರ), ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಬೇರ್ಪಡಿಸುವ ಶಕ್ತಿಯ ತಡೆಗೋಡೆಯನ್ನು ಜಯಿಸುತ್ತವೆ ಡಿε- ಮತ್ತು ಡಿγ-ಕಕ್ಷೆಗಳು; ನಾಲ್ಕನೇ ಮತ್ತು ನಂತರ ಐದನೇ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಕ್ವಾಂಟಮ್ ಕೋಶಗಳನ್ನು ಜನಪ್ರಿಯಗೊಳಿಸುತ್ತವೆ ಡಿγ-ಉಪಮಟ್ಟದ.
![]() dε
dε
ಬಲವಾದ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರ ಮತ್ತು Δ 0 ನ ಹೆಚ್ಚಿನ ಮೌಲ್ಯದೊಂದಿಗೆ, ನಾಲ್ಕನೇ ಮತ್ತು ಐದನೇ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಜನಸಂಖ್ಯೆ ಡಿγ-ಉಪಮಟ್ಟವನ್ನು ಹೊರಗಿಡಲಾಗಿದೆ; ಭರ್ತಿ ಪ್ರಗತಿಯಲ್ಲಿದೆ ಡಿε-ಕಕ್ಷೆಗಳು.
![]() dε
dε
ನಲ್ಲಿ ದುರ್ಬಲ ಕ್ಷೇತ್ರ ಲಿಗಂಡ್ಗಳು 4 ಅಥವಾ 5 ಎಲೆಕ್ಟ್ರಾನ್ಗಳೊಂದಿಗೆ ಕ್ವಾಂಟಮ್ ಕೋಶಗಳನ್ನು ಜನಪ್ರಿಯಗೊಳಿಸುವುದು ಸಮಾನಾಂತರ ಸ್ಪಿನ್ಗಳು, ಆದ್ದರಿಂದ ಪರಿಣಾಮವಾಗಿ ಸಂಕೀರ್ಣವು ಬಲವಾಗಿ ಹೊರಹೊಮ್ಮುತ್ತದೆ ಪರಕಾಂತೀಯ. ಬಲವಾದ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರದಲ್ಲಿಒಂದು ಮತ್ತು ನಂತರ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ ಡಿε-ಉಪಮಟ್ಟದ, ಆದ್ದರಿಂದ ಪರಕಾಂತತ್ವಸಂಕೀರ್ಣವು ಹೆಚ್ಚು ದುರ್ಬಲವಾಗಿರುತ್ತದೆ. ದುರ್ಬಲ ಕ್ಷೇತ್ರದ ಸಂದರ್ಭದಲ್ಲಿ ಆರನೇ, ಏಳನೇ ಮತ್ತು ಎಂಟನೇ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಮತ್ತೆ ಆನ್ ಆಗುತ್ತವೆ ಡಿγ-ಉಪಮಟ್ಟದ, ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳಿಗೆ ಸಂರಚನೆಗಳನ್ನು ಪೂರೈಸುತ್ತದೆ (ಪ್ರಕರಣದಲ್ಲಿ ಒಂದು ಡಿ 6, ಎರಡು - ಡಿ 7 ಮತ್ತು ಮೂರು - ಡಿ 8):
![]() dε
dε
ಬಲವಾದ ಲಿಗಂಡ್ ಕ್ಷೇತ್ರದ ಸಂದರ್ಭದಲ್ಲಿ, ಆರನೇ ಎಲೆಕ್ಟ್ರಾನ್ ಜನಪ್ರಿಯವಾಗುತ್ತದೆ dε-ಎಒ, ಕಾರಣವಾಗುತ್ತದೆ ಕಾಂತೀಯತೆಸಂಕೀರ್ಣ, ಅದರ ನಂತರ ಏಳನೇ ಮತ್ತು ಎಂಟನೇ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಹೋಗುತ್ತವೆ ಡಿγ-ಉಪಮಟ್ಟದ:
![]() dε
dε
ನಿಸ್ಸಂಶಯವಾಗಿ, ಎಂಟು-ಎಲೆಕ್ಟ್ರಾನ್ ಸಂರಚನೆಯೊಂದಿಗೆ ರಚನೆಯಲ್ಲಿ ವ್ಯತ್ಯಾಸಗಳುಲಿಗಂಡ್ಗಳೊಂದಿಗೆ ಸಂಕೀರ್ಣಗಳ ನಡುವೆ ದುರ್ಬಲಮತ್ತು ಬಲವಾದ ಕ್ಷೇತ್ರಗಳು ಕಣ್ಮರೆಯಾಗುತ್ತವೆ. ಒಂಬತ್ತನೇ ಮತ್ತು ಹತ್ತನೇ ಎಲೆಕ್ಟ್ರಾನ್ನಿಂದ ಕಕ್ಷೆಗಳ ಉದ್ಯೋಗವು ಎರಡೂ ಪ್ರಕಾರಗಳ ಸಂಕೀರ್ಣಗಳಿಗೆ ಭಿನ್ನವಾಗಿರುವುದಿಲ್ಲ:
![]() dε
dε
ಆಕ್ಟಾಹೆಡ್ರಲ್ ಸಂಕೀರ್ಣ ಅಯಾನುಗಳು 3+ ಮತ್ತು -3 ರ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಚನೆಯ ಪರಿಗಣನೆಗೆ ನಾವು ಹಿಂತಿರುಗೋಣ. ನಲ್ಲಿರುವ ಸ್ಥಳದ ಪ್ರಕಾರ ಸ್ಪೆಕ್ಟ್ರೋಕೆಮಿಕಲ್ ಸರಣಿ, ಅಮೋನಿಯ NH 3 ಲಿಗಂಡ್ಗಳಲ್ಲಿ ಒಂದಾಗಿದೆ ಬಲವಾದ ಕ್ಷೇತ್ರ, ಮತ್ತು ಫ್ಲೋರೈಡ್ ಅಯಾನ್ ಎಫ್ -- ದುರ್ಬಲ ಕ್ಷೇತ್ರ. -3 ಅಯಾನ್ನಲ್ಲಿ, ಎಫ್ - ಲಿಗಂಡ್ಗಳು ದುರ್ಬಲ ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರವನ್ನು (Δ 0 = 13000 cm -1) ರಚಿಸುತ್ತವೆ, ಮತ್ತು ಮೂಲ 3 ರ ಎಲ್ಲಾ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಡಿ 6 -JSC ನಲ್ಲಿ ಇದೆ ಡಿε- ಮತ್ತು ಡಿಯಾವುದೇ ಜೋಡಣೆಯಿಲ್ಲದೆ γ ಕಕ್ಷೆಗಳು. ಒಂದು ಸಂಕೀರ್ಣ ಅಯಾನು ಹೆಚ್ಚಿನ ಸ್ಪಿನ್ಮತ್ತು ನಾಲ್ಕು ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ, ಆದ್ದರಿಂದ ಇದು ಪರಕಾಂತೀಯ:

3+ ಅಯಾನುಗಳಲ್ಲಿ, NH 3 ಲಿಗಂಡ್ಗಳು ಬಲವಾದ ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರವನ್ನು ರಚಿಸುತ್ತವೆ (Δ 0 = 22900 cm -1), ಎಲ್ಲಾ 3 ಡಿ 6-ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೆಚ್ಚು ಶಕ್ತಿಯುತವಾಗಿ ಅನುಕೂಲಕರವಾದ ಮೇಲೆ ಇರಿಸಲಾಗುತ್ತದೆ ಡಿε-ಕಕ್ಷೆಗಳು. ನಿಂದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವರ್ಗಾವಣೆ ಡಿε- ರಂದು ಡಿγ ಕಕ್ಷೆಗಳು ಅಸಾಧ್ಯಏಕೆಂದರೆ ತುಂಬಾ ಹೆಚ್ಚಿನ ಶಕ್ತಿಯ ತಡೆಗೋಡೆ. ಆದ್ದರಿಂದ, ಈ ಸಂಕೀರ್ಣ ಕ್ಯಾಷನ್ ಆಗಿದೆ ಕಡಿಮೆ ಸ್ಪಿನ್, ಇದು ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವುದಿಲ್ಲ ಮತ್ತು ಕಾಂತೀಯ:

ಇದೇ ರೀತಿಯಾಗಿ, 2+ ಮತ್ತು -4 ಅಯಾನುಗಳಿಗೆ ಆಕ್ಟಾಹೆಡ್ರಲ್ ಕ್ಷೇತ್ರದಲ್ಲಿ ಕಕ್ಷೆಗಳ ಮೇಲೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿತರಣೆಯ ಯೋಜನೆಗಳನ್ನು ಪ್ರಸ್ತುತಪಡಿಸಬಹುದು:


H 2 O ಲಿಗಂಡ್ಗಳು ದುರ್ಬಲ ಕ್ಷೇತ್ರವನ್ನು ರಚಿಸುತ್ತವೆ; ನಡುವೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿನಿಮಯ ಡಿε- ಮತ್ತು ಡಿγ-ಕಕ್ಷೆಗಳು ಯಾವುದೇ ತೊಂದರೆಗಳನ್ನು ಉಂಟುಮಾಡುವುದಿಲ್ಲ ಮತ್ತು ಆದ್ದರಿಂದ ಸಂಕೀರ್ಣ ಅಯಾನುಗಳಲ್ಲಿ ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯು ಸಾಂಪ್ರದಾಯಿಕ ಅಯಾನು Fe + II ನಲ್ಲಿರುವಂತೆಯೇ ಇರುತ್ತದೆ. ಪರಿಣಾಮವಾಗಿ ಆಕ್ವಾ ಕಾಂಪ್ಲೆಕ್ಸ್ ಆಗಿದೆ ಹೆಚ್ಚಿನ ಸ್ಪಿನ್, ಪ್ಯಾರಾಮ್ಯಾಗ್ನೆಟಿಕ್.
ಇದಕ್ಕೆ ವಿರುದ್ಧವಾಗಿ, CN - ಲಿಗಂಡ್ಗಳು ಗಮನಾರ್ಹವಾದ ಸೀಳನ್ನು ಉಂಟುಮಾಡುತ್ತವೆ ಡಿ-AO, 33000 cm -1 ಮೊತ್ತ. ಇದರರ್ಥ ಬಲವಿದೆ ಎಲ್ಲಾ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ನಿಯೋಜಿಸುವ ಪ್ರವೃತ್ತಿಮೇಲೆ ಡಿε-ಕಕ್ಷೆಗಳು. ಶಕ್ತಿ ಗಳಿಕೆ, ಇಂತಹ ಕಕ್ಷೆಗಳ ಜನಸಂಖ್ಯೆಯೊಂದಿಗೆ ಪಡೆಯಲಾಗಿದೆ, ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಣೆಯ ಕಾರಣ ಶಕ್ತಿಯ ವೆಚ್ಚಕ್ಕಿಂತ ಹೆಚ್ಚು.
ವೇಲೆನ್ಸಿ ಬಾಂಡ್ ವಿಧಾನದ ದೃಷ್ಟಿಕೋನದಿಂದ, ಆಕ್ವಾ ಸಂಕೀರ್ಣದಲ್ಲಿ ಬಂಧವನ್ನು ರೂಪಿಸುವ ವೇಲೆನ್ಸಿ ಆರ್ಬಿಟಲ್ಗಳ ಹೈಬ್ರಿಡೈಸೇಶನ್ ಒಳಗೊಂಡಿರುತ್ತದೆ ಡಿ-AO ಬಾಹ್ಯ ಉಪಮಟ್ಟದ (4 sp 3 ಡಿ 2), ಮತ್ತು ಕಡಿಮೆ ಸ್ಪಿನ್ನಲ್ಲಿ - ಡಿ-ಜೆಎಸ್ಸಿ ಆಂತರಿಕ ಉಪಹಂತ (3 ಡಿ 2 4sp 3).
ಹೀಗಾಗಿ, ದುರ್ಬಲ-ಕ್ಷೇತ್ರದ ಲಿಗಂಡ್ಗಳೊಂದಿಗೆ ಹೈ-ಸ್ಪಿನ್ ಸಂಕೀರ್ಣಗಳಲ್ಲಿ, ಭಾಗವಹಿಸುವಿಕೆಯೊಂದಿಗೆ ಹೈಬ್ರಿಡೈಸೇಶನ್ ಸಂಭವಿಸುತ್ತದೆ ಡಿಬಾಹ್ಯ ಉಪಮಟ್ಟದ AO, ಮತ್ತು ಹೈ-ಫೀಲ್ಡ್ ಲಿಗಂಡ್ಗಳೊಂದಿಗೆ ಕಡಿಮೆ-ಸ್ಪಿನ್ - ಡಿ- ಆಂತರಿಕ ಉಪಮಟ್ಟದ JSC. ಸಂಕೀರ್ಣದಲ್ಲಿನ ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯನ್ನು ಎಲೆಕ್ಟ್ರಾನ್ ಪ್ಯಾರಾಮ್ಯಾಗ್ನೆಟಿಕ್ ರೆಸೋನೆನ್ಸ್ (ಇಪಿಆರ್) ಮೂಲಕ ನಿರ್ಧರಿಸಬಹುದು. EPR ಸ್ಪೆಕ್ಟ್ರೋಮೀಟರ್ಗಳು ಎಂದು ಕರೆಯಲ್ಪಡುವ ಈ ವಿಧಾನದ ಉಪಕರಣಗಳನ್ನು ಬಳಸಿ, ಪ್ಯಾರಾಮ್ಯಾಗ್ನೆಟಿಕ್ ಪದಾರ್ಥಗಳನ್ನು ಅಧ್ಯಯನ ಮಾಡಲಾಗುತ್ತದೆ.
ಸ್ಫಟಿಕ ಕ್ಷೇತ್ರದ ಸಿದ್ಧಾಂತವು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಒಂದು ಬಣ್ಣ ಅಥವಾ ಇನ್ನೊಂದು ನೋಟವನ್ನು ವಿವರಿಸಲು ಸಾಧ್ಯವಾಗಿಸುತ್ತದೆ. ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳಲ್ಲಿ, ಸ್ಫಟಿಕದ ಸ್ಥಿತಿ ಮತ್ತು ಜಲೀಯ ದ್ರಾವಣದಲ್ಲಿ ಗಮನಾರ್ಹ ಸಂಖ್ಯೆಯು ಅವುಗಳ ಪ್ರಕಾಶಮಾನವಾದ ಬಣ್ಣದಿಂದ ಪ್ರತ್ಯೇಕಿಸಲ್ಪಟ್ಟಿದೆ. ಹೀಗಾಗಿ, 2+ ಕ್ಯಾಟಯಾನುಗಳನ್ನು ಹೊಂದಿರುವ ಜಲೀಯ ದ್ರಾವಣವು ಗಾಢವಾದ ನೀಲಿ ಬಣ್ಣವನ್ನು ಹೊಂದಿರುತ್ತದೆ, 3+ ಕ್ಯಾಟಯಾನುಗಳು ದ್ರಾವಣಕ್ಕೆ ನೇರಳೆ ಬಣ್ಣವನ್ನು ನೀಡುತ್ತದೆ ಮತ್ತು 2+ ಕ್ಯಾಟಯಾನುಗಳು ಕೆಂಪು ಬಣ್ಣವನ್ನು ನೀಡುತ್ತವೆ. ಒಂದು ವಸ್ತುವಿನ ದ್ರಾವಣ ಅಥವಾ ಸ್ಫಟಿಕದ ಮಾದರಿಯ ಮೂಲಕ ಬೆಳಕನ್ನು ಹಾದು ಹೋದರೆ ವರ್ಣಪಟಲದ ಗೋಚರ ಭಾಗ, ನಂತರ, ತಾತ್ವಿಕವಾಗಿ, ಮಾದರಿಯ ದೈಹಿಕ ನಡವಳಿಕೆಗೆ ಮೂರು ಆಯ್ಕೆಗಳು ಸಾಧ್ಯ: ಬೆಳಕಿನ ಹೀರಿಕೊಳ್ಳುವಿಕೆ ಇಲ್ಲಯಾವುದೇ ತರಂಗಾಂತರ (ವಸ್ತು ಮಾದರಿ ಬಣ್ಣರಹಿತ, ಇದು ವರ್ಣಪಟಲದ ನೇರಳಾತೀತ ಪ್ರದೇಶದಲ್ಲಿ ಹೀರಿಕೊಳ್ಳುವ ಬ್ಯಾಂಡ್ಗಳನ್ನು ಹೊಂದಿರಬಹುದು); ಸಂಪೂರ್ಣ ಬೆಳಕಿನ ಹೀರಿಕೊಳ್ಳುವಿಕೆಸಂಪೂರ್ಣ ತರಂಗಾಂತರ ವ್ಯಾಪ್ತಿಯಲ್ಲಿ (ಮಾದರಿಯು ಕಾಣಿಸುತ್ತದೆ ಕಪ್ಪು); ಅಂತಿಮವಾಗಿ, ಬೆಳಕಿನ ಹೀರಿಕೊಳ್ಳುವಿಕೆಮಾತ್ರ ನಿರ್ದಿಷ್ಟ ತರಂಗಾಂತರ(ನಂತರ ಮಾದರಿಯು ಹೊಂದಿರುತ್ತದೆ ಹೀರಿಕೊಳ್ಳಲು ಪೂರಕವಾದ ಬಣ್ಣವರ್ಣಪಟಲದ ಕಿರಿದಾದ ಭಾಗ).

ಹೀಗಾಗಿ, ದ್ರಾವಣ ಅಥವಾ ಸ್ಫಟಿಕಗಳ ಬಣ್ಣವನ್ನು ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ ಹೀರಿಕೊಳ್ಳುವ ಬ್ಯಾಂಡ್ಗಳ ಆವರ್ತನಗೋಚರ ಬೆಳಕು. ಸಂಕೀರ್ಣಗಳ ಮೂಲಕ ಬೆಳಕಿನ ಕ್ವಾಂಟಾವನ್ನು ಹೀರಿಕೊಳ್ಳುವುದು (ಉದಾಹರಣೆಗೆ, ಆಕ್ಟಾಹೆಡ್ರಲ್ ರಚನೆಯನ್ನು ಹೊಂದಿರುವವರು) ಎಲೆಕ್ಟ್ರಾನ್ಗಳೊಂದಿಗೆ ಬೆಳಕಿನ ಪರಸ್ಪರ ಕ್ರಿಯೆಯಿಂದ ವಿವರಿಸಲಾಗಿದೆ ಡಿε-ಉಪಮಟ್ಟದ, ಖಾಲಿ ಕಕ್ಷೆಗಳಿಗೆ ಅವುಗಳ ಪರಿವರ್ತನೆಯೊಂದಿಗೆ ಡಿγ-ಉಪಮಟ್ಟದ. ಉದಾಹರಣೆಗೆ, ಹೆಕ್ಸಾಕ್ವಾಟಿಟಾನಿಯಮ್(III) 3+ ಕ್ಯಾಟಯಾನುಗಳನ್ನು ಹೊಂದಿರುವ ಜಲೀಯ ದ್ರಾವಣದ ಮೂಲಕ ಬೆಳಕನ್ನು ಹಾದುಹೋದಾಗ, ವರ್ಣಪಟಲದ ಹಳದಿ-ಹಸಿರು ಪ್ರದೇಶದಲ್ಲಿ (20300 cm -1, λ=500 nm) ಬೆಳಕಿನ ಹೀರಿಕೊಳ್ಳುವ ಬ್ಯಾಂಡ್ ಪತ್ತೆಯಾಗುತ್ತದೆ. ಇದು ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ನ ಏಕ ಎಲೆಕ್ಟ್ರಾನ್ನ ಪರಿವರ್ತನೆಯ ಕಾರಣದಿಂದಾಗಿರುತ್ತದೆ ಡಿε-AO ಆನ್ ಡಿγ-ಉಪಮಟ್ಟದ:

ಆದ್ದರಿಂದ, 3+ ಹೊಂದಿರುವ ಪರಿಹಾರವು ನೇರಳೆ ಬಣ್ಣವನ್ನು ಪಡೆಯುತ್ತದೆ (ಹೀರಿಕೊಂಡ ಹಳದಿ-ಹಸಿರು ಜೊತೆಗೆ). ವೆನಾಡಿಯಮ್ ಉಪ್ಪು Cl 3 ರ ಪರಿಹಾರವು ಹಸಿರು ಬಣ್ಣದ್ದಾಗಿದೆ. ಇದು ಬೆಳಕಿನ ಕಿರಣದ ಶಕ್ತಿಯ ಭಾಗವನ್ನು ಹೀರಿಕೊಳ್ಳುವಾಗ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಅನುಗುಣವಾದ ಪರಿವರ್ತನೆಗಳ ಕಾರಣದಿಂದಾಗಿರುತ್ತದೆ. ನೆಲದ ಸ್ಥಿತಿಯಲ್ಲಿ, ವನಾಡಿಯಮ್ (III) 3 ರ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸಂರಚನೆಯೊಂದಿಗೆ ಡಿ 2, ಎರಡು ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಆಕ್ರಮಿಸಿಕೊಂಡಿವೆ ಡಿε-ಉಪಮಟ್ಟದ:

ಮಾತ್ರ ಇದೆ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಪರಿವರ್ತನೆಗೆ ಎರಡು ಆಯ್ಕೆಗಳುಮೇಲೆ ಡಿγ-ಉಪಮಟ್ಟದ: ಒಂದೋ ಎರಡೂಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಆಕ್ರಮಿಸಿಕೊಂಡಿವೆ ಡಿγ-AO, ಅಥವಾ ಮಾತ್ರ ಒಂದುಅವರಲ್ಲಿ. ಒಟ್ಟು ಸ್ಪಿನ್ನಲ್ಲಿನ ಇಳಿಕೆಗೆ ಸಂಬಂಧಿಸಿದ ಯಾವುದೇ ಇತರ ಎಲೆಕ್ಟ್ರಾನ್ ಪರಿವರ್ತನೆಗಳನ್ನು ನಿಷೇಧಿಸಲಾಗಿದೆ.
ಹೆಚ್ಚುವರಿ ಶಕ್ತಿಯನ್ನು ಪಡೆದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸೂಚಿಸಲಾದ ಪರಿವರ್ತನೆಗಳು ಅನುರೂಪವಾಗಿದೆ ಹೀರಿಕೊಳ್ಳುವ ಬ್ಯಾಂಡ್ಹೆಕ್ಸಾಕ್ವಾವನಾಡಿಯಮ್ (III) ಕ್ಲೋರೈಡ್ನ ದ್ರಾವಣದ ಹೀರಿಕೊಳ್ಳುವ ವರ್ಣಪಟಲದಲ್ಲಿ ಸುಮಾರು 400 nm. ವರ್ಣಪಟಲದ ನೇರಳೆ-ನೇರಳೆ ಪ್ರದೇಶದ ಹೀರಿಕೊಳ್ಳುವಿಕೆಯು ಪರಿಹಾರಕ್ಕೆ ಹೆಚ್ಚುವರಿ ಬಣ್ಣವನ್ನು ನೀಡುತ್ತದೆ - ಪ್ರಕಾಶಮಾನವಾದ ಹಸಿರು. ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಕಾನ್ಫಿಗರೇಶನ್ ಹೊಂದಿದ್ದರೆ ಡಿ 0 ಅಥವಾ ಡಿನಂತರ 10 ಎಲೆಕ್ಟ್ರಾನ್ ಪರಿವರ್ತನೆಗಳುಜೊತೆಗೆ ಡಿε- ರಂದು ಡಿγ-ಉಪಮಟ್ಟದ ಅಥವಾ ಪ್ರತಿಯಾಗಿ ಅಸಾಧ್ಯಒಂದೋ ಏಕೆಂದರೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಅನುಪಸ್ಥಿತಿ, ಒಂದೋ ಏಕೆಂದರೆ ಖಾಲಿ ಕಕ್ಷೆಗಳ ಅನುಪಸ್ಥಿತಿ. ಆದ್ದರಿಂದ, Sc (III) ನಂತಹ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ಗಳೊಂದಿಗೆ ಸಂಕೀರ್ಣಗಳ ಪರಿಹಾರಗಳು (3 ಡಿ 0), Cu(I) (3 ಡಿ 10), Zn(II) (3 ಡಿ 10), ಸಿಡಿ(II) (4 ಡಿ 10), ಇತ್ಯಾದಿ, ವರ್ಣಪಟಲದ ಗೋಚರ ಭಾಗದಲ್ಲಿ ಶಕ್ತಿಯನ್ನು ಹೀರಿಕೊಳ್ಳುವುದಿಲ್ಲ ಮತ್ತು ಕಾಣಿಸಿಕೊಳ್ಳುತ್ತದೆ ಬಣ್ಣರಹಿತ. ಬೆಳಕಿನ ಹೀರಿಕೊಳ್ಳುವಿಕೆಯ ಆಯ್ಕೆಯು ಕೇವಲ ಅವಲಂಬಿಸಿರುತ್ತದೆ ಸಂಕೀರ್ಣ ಏಜೆಂಟ್ಮತ್ತು ಅದರ ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿ, ಆದರೆ ಸಹ ಲಿಗಂಡ್ಗಳ ವಿಧ. ಸ್ಪೆಕ್ಟ್ರೋಕೆಮಿಕಲ್ ಸರಣಿಯ ಎಡಭಾಗದಲ್ಲಿರುವ ಲಿಗಂಡ್ಗಳನ್ನು ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತದಲ್ಲಿ ರಚಿಸುವ ಲಿಗಂಡ್ಗಳೊಂದಿಗೆ ಬದಲಾಯಿಸುವಾಗ ಬಲವಾದಸ್ಥಾಯೀವಿದ್ಯುತ್ತಿನ ಕ್ಷೇತ್ರವನ್ನು ಗಮನಿಸಲಾಗಿದೆ ಹೆಚ್ಚಳಹರಡುವ ಬೆಳಕಿನಿಂದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ಹೀರಿಕೊಳ್ಳಲ್ಪಟ್ಟ ಶಕ್ತಿಯ ಭಾಗ ಮತ್ತು ಪರಿಣಾಮವಾಗಿ, ಇಳಿಕೆಅನುಗುಣವಾದ ಹೀರಿಕೊಳ್ಳುವ ಬ್ಯಾಂಡ್ನ ತರಂಗಾಂತರ. ಹೀಗಾಗಿ, ಟೆಟ್ರಾಕ್ವಾಕಾಪರ್ (II) 2+ ಕ್ಯಾಟಯಾನ್ಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ಜಲೀಯ ದ್ರಾವಣವು ನೀಲಿ ಬಣ್ಣದ್ದಾಗಿದೆ ಮತ್ತು ಟೆಟ್ರಾಅಮಿನೆಕಾಪರ್ (II) 2+ ಸಲ್ಫೇಟ್ನ ದ್ರಾವಣವು ಗಾಢವಾದ ನೀಲಿ ಬಣ್ಣದ್ದಾಗಿದೆ.
ಸಂಬಂಧಿಸಿದ ಮಾಹಿತಿ.