Државна фармакопеја xiii. Одредување на главните групи на биолошки активни супстанции. Автентикација на цели лисја
Лековите се специфичен производствен производ, чиј квалитет потрошувачот не може самостојно да го оцени. Гарантирањето на квалитетот на двата лека произведени во Русија и увезени од странство е една од главните задачи на државата во областа на заштитата на јавното здравје. Најважните задачи вклучуваат не само заситување на домашниот фармацевтски пазар со овие лекови, туку и влез на меѓународниот фармацевтски пазар, што може да се постигне со обезбедување дека домашните лекови се усогласени со барањата на светските стандарди, истакна министерката Вероника Скворцова во воведното обраќање до публикацијата.
Новото издание на Државната фармакопеја, XIII издание, ги решава овие стратешки проблеми.
Првата фармакопеја, објавена во 1765 година, беше на латински и имаше за цел да го обезбеди квалитетот на лековите што ги користат хирурзите во воените болници. Во следните години, децении и векови, домашната фармакопеја постојано беше реобјавувана, ажурирајќи ја нејзината содржина во согласност со состојбата и степенот на развој на фармацевтската индустрија и системот за контрола и лиценцирање како кај нас така и во странство, рече директорот на Секторот. на Државното регулирање на прометот на лекови во неговиот вовед.средства Арсалан Циндимеев.
Државната фармакопеја од XIII издание вклучуваше 229 општа фармакопеја и 179 статии од фармакопеја.
За прв пат, во Државната фармакопеја од XIII издание се воведени 99 општи фармакопеја, вклучувајќи 30 за методи на анализа, 5 за дозирани форми и 12 за методи за определување на фармацевтски и технолошки параметри на дозираните форми. Покрај тоа, 2 општи фармакопејални статии - за лековити растителни суровини и 3 - за методите на нејзина анализа, 7 - за групи на имунобиолошки лекови и 31 - за методите на нивно тестирање, 3 - за групи на лекови од крв и крвна плазма на луѓе и животни, 9 - на методи за анализа на медицински производи добиени од крв и крвна плазма на луѓе и животни.
Главната цел што ја следи Државната фармакопеја на Руската Федерација е стандардизирање на квалитетот на лековите во оптек на домашниот фармацевтски пазар, забележува Елена Саканјан, директор на Центарот за фармакопеја и меѓународна соработка на Федералната државна буџетска институција „NTsESMP“.
Навременото објавување на Државната фармакопеја на Руската Федерација, која во согласност со Федералниот закон „За циркулација на лекови“ треба да се спроведува со фреквенција не поголема од 1 пат во 5 години, ќе биде клучот за решавање на проблемот со обезбедување на висококвалитетна медицинска нега на населението во нашата земја.
Наредбата на Министерството за здравство на Руската Федерација од 29 октомври 2015 година бр. 771 предвидува воведување на сила на општите фармакопеја монографии и фармакопеја монографии вклучени во Државната фармакопеја од XIII издание од 1 јануари 2016 година.
Утврдено е дека општите фармакопејски монографии и фармакопејските монографии одобрени со оваа наредба, општите фармакопески монографии и фармакопејските монографии одобрени по наредба на Министерството за здравство на Руската Федерација од 21 ноември 2014 година бр. 768 „За одобрување на општи фармакопејски монографии и фармакопеја монографии“ ги сочинуваат публикациите на Државната фармакопеја XIII
Утврди дека:
регулаторна документација за регистрирани лекови за медицинска употреба, како и за лекови за медицинска употреба, чии барања за државна регистрација се поднесуваат до Министерството за здравство на Руската Федерација пред влегувањето во сила на фармакопејските монографии одобрени со оваа наредба , ќе бидат усогласени со овие фармакопејски монографии пред 1 јануари 2018 година;
регулаторна документација за регистрирани лекови за медицинска употреба, како и за лекови за медицинска употреба, чии барања за државна регистрација се доставуваат до Министерството за здравство на Руската Федерација пред влегувањето во сила на општите фармакопејски монографии одобрени со овој ред, ќе се усогласат со овие општи фармакопејски монографски статии до 1 јануари 2019 година.
Новата Државна фармакопеја може да се најде на следната е-адреса:
Општи фармакопеја монографии и фармакопеја монографии на Државната фармакопеја на Руската Федерација
XIII издание
В.А. Меркулов, Е.И. Сакањан, Т.Б. Шемерјанкина, О.А. Мочикина, Н.Д. Буњатјан
Федерална државна буџетска институција „Научен центар за експертиза на медицински производи“ на Министерството за здравство на Руската Федерација, 127051, Москва, Русија
Резиме: Државната фармакопеја на Руската Федерација е збир на општа фармакопеја и статии од фармакопеја и е предмет на повторно издавање најмалку еднаш на секои 5 години. Следното издание на Државната фармакопеја на Руската Федерација, планирано за објавување во 2015 година, ќе вклучува и општи фармакопеја монографии и фармакопеја монографии кои први биле развиени во практиката на домашната, а во некои случаи и глобалната фармакопеја анализа, како и статии кои се ажурирани и ревидирани верзии општи фармакопејски монографии и фармакопејски монографии. Воведувањето на општи фармакопеја монографии и фармакопеја монографии на ова издание на Државната фармакопеја на Руската Федерација значително ќе го зголеми нивото на домашната фармакопеја анализа и ќе обезбеди нејзино усогласување со барањата на светските стандарди.
Клучни зборови: државна фармакопеја; општа фармакопеја монографија; фармакопеја монографија; квалитет на лекови; фармакопеја анализа.
Библиографски опис: Меркулов В.А., Сакањан ЕИ, Шемерјанкина ТБ, Мочикина ОА, Буњатјан НД. Општи фармакопеја написи и написи од фармакопеја на Државната фармакопеја на Руската Федерација XIII издание. Гласник на Научен центар за вештачење на медицински производи 2015 година; (2): 54-58.
ОПШТИ МОНОГРАФИ И ФАРМАКОПЕЈСКИ МОНОГРАФИ НА ДРЖАВНАТА ФАРМАКОПЕИЈА НА РУСКАТА Федерација, xIII издание v.A. Меркулов, Е.И. Сакањан, Т.Б. Шемерјанкина, О.А. Мочикина, Н.Д. Буњатјан
Федерална државна буџетска институција „Научен центар за стручна евалуација на медицински производи“ на Министерството за здравство на Руската Федерација, 127051, Москва, Русија
Апстракт: Државната фармакопеја на Руската Федерација е збирка на општи монографии и фармакопеја монографии. Треба да се реиздава најмалку еднаш во 5 години. Следното закажано издание на Државната фармакопеја на Руската Федерација е планирано за објавување во 2015 година. Тоа ќе вклучува и прво развиени во национални и, во некои случаи, глобална фармакопеја анализа општи и фармакопеја монографии, како и ажурирани ревидирани општи и фармакопески монографии. Спроведувањето на општите и фармакопејските монографии на споменатото издание на Државната фармакопеја на Руската Федерација значително ќе го зголеми нивото на националната фармакопеја анализа и ќе обезбеди нејзино усогласување со меѓународните стандарди.
Клучни зборови: Државна фармакопеја; општа монографија; фармакопеја монографија; квалитет на лекот; фармакопеја анализа.
Библиографски опис: Меркулов В.А., Сакањан ЕИ, Шемерјанкина ТБ, Мочикина ОА, Буњатјан НД. Општи монографии и фармакопеја монографии на Државната фармакопеја на Руската Федерација, XIII издание. Научен центар за стручна евалуација на лекови Билтен 2015 година; (2): 54-58.
Главната цел што ја следи Државната фармакопеја на Руската Федерација (SF RF) е стандардизирање на квалитетот на лековите во оптек на домашниот фармацевтски пазар.
Во моментов функционираат Државниот фонд на X издание (1968), Државниот фонд на XI издание (дел 1 - 1987, дел 2 - 1989), како и Државниот фонд од XII издание (дел 1 - 2007 г.) територијата на Руската Федерација. Наведените датуми на објавување на овие публикации на Глобалниот фонд укажуваат дека тие не се во согласност со барањата на актуелниот Федерален закон од 12 април 2010 година „За циркулација на лекови“ бр. 61-ФЗ во врска со времето на повторно издавање на Државна фармакопеја.
И покрај ова, општите фармакопеја монографии (GPM) и фармакопеја монографии (PS) вклучени во изданијата на Државната фармакопеја X-X11 не се откажани. Некои од нив имаат потреба од ревизија, некои од написите веќе ја изгубија својата важност поради недостаток на побарувачка. Тие вклучуваат такви GPM како „Биолошки метод за одредување на активноста на 0,1% раствор на адреналин хидрохлорид“, „Биолошко тестирање
ција на новарсенол и миарсенол“, „Одредување на степенот на белина на лековите во прав“ и други. Потребно е и укинување на ФС за лекови повлечени од промет. Покрај тоа, фармацевтските супстанции одобрени во периодот помеѓу издавањето на фармакопеите, според кои поединечни претпријатија произведуваат лекови и го следат нивниот квалитет, треба да се ревидираат, бидејќи методите на фармакопеја анализа постојано се подобруваат.
Во моментов, 229 OFS и 179 FS се подготвени за вклучување во следното XIII издание на Државниот фонд на Руската Федерација. Тие можат да се поделат на соодветни делови.
Делот „Општи написи за фармакопеја“ содржи: статии за општи методи, Општи фармакопејски монографии за методите на анализа, реагенси, дозирани форми и методи на нивна анализа; лековити растителни суровини и методи за проценка на нивниот квалитет; групи на имунобиолошки лекови и методи на нивна анализа; медицински производи од човечка и животинска крв и крвна плазма и аналитички методи кои се користат при проценка на нивниот квалитет; радиофармацевтски производи.
Фармакопејалните монографии се претставени во деловите „Фармацевтски супстанции“ и „Лекови“. Делот „Фармацевтски супстанции“ е претставен преку фармакопејски артикли за фармацевтски супстанции од синтетичко или минерално потекло, кои се користат како активни и/или ексципиенси. Дополнително, фармакопејските монографии за лековити растителни суровини што се користат во фармацевтското производство, вклучително и лековити хербални препарати, се претставени како посебен поддел. Делот „Лекови“ се состои од два подсекции: имунобиолошки лекови и лекови добиени од човечка крв и плазма.
Додатоците на Државниот фонд на Руската Федерација, XIII издание, се претставени со референтни табели: табела со атомски маси, алкохол-холометриски табели, табела со изотонични еквиваленти на лековити супстанции за натриум хлорид, табела со бројот на капки во 1 g и 1 ml и маса од 1 капка течни лекови на температура од 20 ° C со помош на стандарден мерач на капки, цртежи на IR спектри на стандардни примероци на фармацевтски супстанции.
Од овој број, за прв пат за Државната фармакопеја на Руската Федерација, XIII издание, беа развиени и препорачани за одобрување 102 монографии на Општа фармакопеја, вклучувајќи 30 монографии на Општа фармакопеја за методи на анализа, 5 монографии на Општа фармакопеја за дозирани форми, и 12 Монографии на Општа фармакопеја за методи за определување фармацевтски и технолошки параметри на дозирани форми, 2 монографии на Општа фармакопеја за лековити растителни суровини и 3 Монографија на Општа фармакопеја за методи на нејзина анализа, 7 Општа фармакопеја Монографски имунобиолошки групи и3 мем. Монографија за општа фармакопеја за нивните методи на испитување, 3 Монографија за општа фармакопеја за групи на лекови од крв и плазма од човечка и животинска, 9 Монографија за општа фармакопеја за методи на анализа на лекови добиени од крв и плазма крв на луѓе и животни.
Покрај тоа, за вклучување во Државната фармакопеја на Руската Федерација од XIII издание, за прв пат беа подготвени 17 фармакопејални статии, вклучувајќи 4 FS за фармацевтски супстанции, 4 FS за лековити растителни суровини, 5 FS за имунобиолошки медицински производи и 4 FS за медицински производи од човечка крв и крвна плазма.
Голем број општи фармацевтски супстанции претходно претставени во Државната фармакопеја на СССР во изданијата X и XI (издание X и Државна фармакопеја на СССР, издание на Државната фармакопеја XI на СССР) се исклучени од практиката на модерна фармакопеја анализа како непотврдени. Другите тековни OFS и FS Државна фармакопеја на СССР X издание, Државната фармакопеја на XI издание на СССР (издание 1, 2) и Државната фармакопеја на Руската Федерација XII издание (издание SF RF XII) се ревидирани и дополнети со материјали кои земаат во предвид современите барања, научни и практични достигнувања во областа на фармакопеја анализа.
Монографијата на Општата фармакопеја „Правила за употреба на фармакопеја монографии“ е дополнета со деловите „Влажност“ и „Складирање“. Дополнително, дадени се соодветни појаснувања во деловите „Опис“, „Маса“, „Волумен“, „Температура“, „Точно мерење“, „Растворувачи“, „Индикатори“, „Граници на содржина“, „Филтрација“.
„Земење примероци“ на OFS вклучува дефиниции за термини, општи одредби, а додаден е и делот „Правила за земање примероци“. Воведени се и нови делови: „Земење примероци од наливни лекови и материјали
риболов“, „Земење примероци на лекови во амбалажа за широка потрошувачка“, „Пакување, етикетирање, складирање на избрани примероци“, „Барања за простории, опрема и персонал за земање мостри“.
OFS „Sieve Analysis“ беше развиен за да го замени OFS GF XI изданието „Определување на мелење прашоци и сита“ и ја означува целта на анализата на ситото, условите и методите за нејзино спроведување, класификација на типични големини на сита во согласност со барањата на светот стандарди.
Новото издание на Монографијата на Општата фармакопеја „Стерилизација“ содржи современи актуелни методи и услови за стерилизација на фармацевтски супстанци, лекови, ексципиенси и сл., критериум за степенот на стерилизација и опис на биолошките показатели за стерилизација.
Во согласност со дополнителните податоци за токсичност, дадени се појаснувања на Монографијата на Општата фармакопеја „Резидуални органски растворувачи“ и додадени се информации за растворувачи со недоволно потврдена токсичност.
Во Монографијата на Општата фармакопеја „Радиофармацевтски препарати“ е проширен делот „Список на индикатори за квалитет што мора да ги исполнуваат радиофармацевтските препарати од индустриско производство и експонатното производство“, а делот „Полуживот“ е дополнет со равенка за полуживот кривина.
Монографијата на Општата фармакопеја „Фармацевтски супстанции“ направи значајни дополнувања на делот што ги карактеризира барањата за квалитетот на фармацевтските супстанции (на пример, „Преостанати органски растворувачи“, „Бактериски ендотоксини или пирогеност“ итн.). Обезбедена е уредена дефиниција за поимот „фармацевтска супстанција“. Монографијата на Општата фармакопеја е дополнета со делови за методите на биолошка анализа: „Абнормална токсичност“ и „Хистамин и/или депресорни супстанции“. Вклучува табели како што се „Граници за контрола, идентификација и квалификација на поврзаните нечистотии за фармацевтски супстанции“, „Граници за контрола, идентификација и квалификација на сродните нечистотии во пептиди добиени по синтетички пат“ и „Критериуми за стандардизирање на дозволената содржина на тешки метали“.
Монографијата на Општата фармакопеја „Рок на траење на лековите“ е дополнета со делот „Тестови за стабилност со методот на „забрзано стареење“.
Во Монографијата на Општата фармакопеја „Општи реакции на автентичноста“ дополнително е воведен делот „Алуминиум“, а во Монографијата на Општата фармакопеја „Начин на согорување во колба со кислород“ е додаден дел „Селен“.
Продолжува описот на тестовите за чистота и дозволените граници на нечистотии во лековите. Така, за прв пат се претставени методи за одредување нечистотии на алуминиум, фосфати, жива и селен. Методите за одредување нечистотии на амониум, калциум, арсен, сулфати, хлориди и цинк и регулаторните барања за нивната содржина се усогласени со барањата на светските стандарди. Монографијата на Општата фармакопеја „Тешки метали“ дополнително ги специфицира методите за квантитативно определување на поединечни јони, а Монографијата на Општата фармакопеја „Железо“ содржи појаснувања во врска со концентрацијата на реагенсите.
Одредувањето на флуорот во лековите се препорачува да се врши со три методи: титриметриски, спектрофотометриски и јонометриски.
Покрај определувањето на бројот на сапонификација, киселинските, етерските и јодните броеви, XIII издание на Државната фармакопеја на Руската Федерација вклучува општи фармаколошки монографии посветени на определувањето на броевите на пероксид, хидроксил и анизидин. За разлика од вредноста на пероксидот, бројот на анизидин ја карактеризира содржината на секундарните оксидациони производи (алдехиди, кетони) во испитуваната фармацевтска супстанција и/или медикаментозниот производ и на тој начин дава целосна слика за квалитетот на лекот што се анализира.
Монографијата на Општата фармакопеја „Определување на протеини“ е значително ревидирана: структурата на написот е променета, појаснето е во врска со определувањето на супстанците кои интерферираат, описот на спектрофотометриските и колориметриските методи за определување на протеинот е проширен и Воведена е флуориметриска метода за определување на протеин со употреба на о-фталдехид. Исклучен е метод како што е определување на протеин со Неслеров реагенс - овој метод е вклучен во посебна монографија на Општа фармакопеја „Одредување на протеински азот со Неслеров реагенс со прелиминарно таложење на протеински материјал во имунобиолошки медицински производи“.
За да се карактеризира главниот индикатор за квалитетот на антацидните лекови, 13-тото издание на Државната фармакопеја на Руската Федерација за прв пат ја вклучи Монографијата на Општата фармакопеја „Определување на способност за неутрализирање на киселината“.
Современите спектроскопски методи за проучување на структурата и квалитетот на лековите се Раман спектрометрија, спектрометрија на флуоресценција на Х-зраци, блиско-инфрацрвена спектрометрија, инфрацрвена спектрометрија, ултравиолетова и видлива спектрофотометрија, спектрометрија на атомски емисии, флуориметрија, нуклеарна магнетна респектометриска спектрометрија, итн. Земајќи ги предвид современите можности на спектроскопските методи, првпат беа развиени OFS како „Раман спектрометрија“, „спектрометрија на флуоресценција на Х-зраци“, „Масна спектрометрија“ и „Спектрометрија на блиско инфрацрвена боја“.
Потребата за воведување на OFS „Полиморфизам“ и „Кристалиност“ се должи на релевантноста на проценката на полиморфизмот и степенот на кристалинчност или содржината на аморфната фракција во фармацевтските супстанции, што последователно го одредува терапевтскиот ефект на лековите и значително влијае на параметрите. на нивната биорасположивост.
Монографијата на Општата фармакопеја „Атомска емисиона спектрометрија и спектрометрија на атомска апсорпција“ од XII издание на Државната фармакопеја (Дел 1) е поделена на две монографии за општа фармакопеја: „Атомска емисиона спектрометрија“ и „Атомска апсорпциона спектрометрија“. Следното издание на Државниот фонд на Руската Федерација ќе ја претстави ревидираната и проширена верзија на Монографијата на Општата фармакопеја „Атомска емисиона спектрометрија“.
Во новото издание на Монографијата на Општата фармакопеја „Флуориметрија“, формулацијата на дефиницијата на методот е променета кон поголема краткост и разноврсност, дадени се фармацевтски супстанции за кои е достапен овој метод на определување, се опишани извори на возбудливо зрачење, концептот на Stokes shift е даден со кратко оправдување на причината за оваа појава, групи на соединенија со флуоресцентни својства-
Додадовме листа на фактори кои влијаат на интензитетот на флуоресценцијата.
За прв пат, Државната фармакопеја вклучува општи фармакопески статии „Оптичка микроскопија“ и „Одредување на дистрибуција на големината на честичките со дифракција на ласерска светлина“. За разлика од методот на микроскопија, методот за проучување на дисперзирани системи засновани на ласерско расејување на светлина овозможува проценка на сите честички, не е деструктивен и ви овозможува да мерите големини на честички во опсег од 0,1 μm до 3 mm, за разлика од оптичката микроскопија , кој се користи за карактеризирање на честички со големини од 1 микрон или повеќе.
Два посебни написи се посветени на губење на тежината за време на сушењето и одредување на вода. Покрај полумикрометодот на К. Фишер, опишан е и кулометриски метод (микрометод), кој овозможува квантифицирање на микроколичините на вода во лековите.
Во монографијата на Општата фармакопеја „Вискозитет“ е променета дефиницијата за нењутнови течности и се карактеризираат условите за одредување на вискозноста на ротационен вискометар. Додадени се следните пододдели како нови: „Вискометри со концентричен цилиндар (апсолутни вискометри)“, „Вискометри со систем на конусна рамнина (апсолутни вискометри)“ и „Вискометри со вретено (релативни вискометри)“.
Развојот на OFS „Електрична спроводливост“ беше предизвикан од потребата да се вклучи овој индикатор за квалитет и начинот на неговото одредување во FS „Прочистена вода“ и „Вода за инјектирање“.
Алтернатива или дополнителна на хроматографските методи за тестирање е методот на електрофореза. При ревидирање на Монографијата на Општата фармакопеја „Електрофореза“, посебно внимание беше посветено на описот на најшироко користениот метод во фармацевтската анализа на електрофореза на протеини во полиакриламид гел со натриум додекал сулфат. Во споредба со традиционалната електрофореза, воведувањето на капиларна електрофореза овозможи автоматско квантифицирање не само на наелектризираните големи молекули или микрочестички, туку и катјони, анјони и неутрални соединенија.
Методот на електрофореза со полиакриламид гел е широко користен за одвојување на различни протеини и проценка на нивната молекуларна тежина. Со менување на концентрацијата на полиакриламид во гелот, можете да го контролирате опсегот на молекуларните тежини на одвоените протеини, што е многу погодно за добивање точни резултати. Фракционирањето на протеинските молекули со помош на овој метод е широко користено за контрола на квалитетот на протеинските лекови.
За прв пат, автоматска елементарна анализа се воведува во практиката на домашната фармакопеја анализа, што овозможува значително да се поедностави анализата на органски соединенија кои содржат азот, сулфур, хлор, бром, кислород и други елементи. Определувањето се заснова на високотемпературно оксидативно распаѓање на супстанциите што се испитуваат и последователно селективно определување на производите на распаѓање што одговараат на овие елементи со помош на гасна хроматографија. Една од предностите на автоматската елементарна анализа е можноста да се користи еден стандарден примерок со позната содржина на елементот што се одредува за да се процени квалитетот на различни лекови за овој елемент.
Одредувањето на адсорпционата активност на ентеросорбентите е специфичен показател за квалитетот на оваа класа на лекови. Адсорпционата активност се користи за карактеризирање на капацитетот за апсорпција на ентеросорбентите; методите за негово одредување се рефлектирани во оваа монографија за општа фармакопеја.
Написите што ги опишуваат биолошките методи за контрола на квалитетот на лековите вклучени во XIII издание на Државниот фонд на Руската Федерација одговараат на современиот пристап кон биолошкото тестирање. Монографијата на Општата фармакопеја „Бактериски ендотоксини“ за првпат воведува опис на фотометриските методи за одредување на бактериски ендотоксини: турбидиметриски и хромогени.
Од монографијата на Општата фармакопеја „Биолошки методи за проценка на активноста на лековити растителни суровини и медицински препарати кои содржат срцеви гликозиди“, при нејзината ревизија, беше исклучен методот на биолошка проценка на содржината на срцеви гликозиди спроведен кај мачки.
Монографијата на Општата фармакопеја „Микробиолошка чистота“ е значително подобрена и дополнета со нови делови, вклучувајќи ги и оние кои се однесуваат на барањата за имунобиолошки медицински производи.
Ревизијата на Монографијата на Општата фармакопеја „Определување на ефикасноста на антимикробните конзерванси“ овозможи во неа да се воведат соодветни дополнувања и појаснувања во однос на категориите на лекови кои содржат конзерванси и критериумите за проценка на ефикасноста на антимикробните конзерванси во лековите.
Ревизија на Монографијата на Општата фармакопеја „Реагенси. Индикатори“ доведоа до значително зголемување на списокот на реагенси и индикатори кои се користат во фармакопејската анализа. Хемиските имиња на реагенсите и индикаторите се дадени во согласност со барањата на Меѓународната унија за чиста и применета хемија (IUPAC). Наведени се регистарските броеви на CAS (Chemical Abstracts Service) на хемиски супстанции вклучени во регистарот на Сервисот за хемиски апстракти. Направени се појаснувања и дополнувања на хемиските формули и физичките параметри на реагенсите и индикаторите.
При ревидирање на Општата фармакопеја, „Статистичка обработка на резултатите од хемиски експерименти и биолошки тестови“ беше поделена на две Општи фармакопеја: „Статистичка обработка на резултатите од хемиски експеримент“ и „Статистичка обработка на резултатите од одредувањето на специфичната фармаколошка активност на лекови со биолошки методи“.
За прв пат, XIII издание на Државниот фонд на Руската Федерација разви и вклучи такви општи фармацевтски супстанции како што се „Дозирани форми“, „Дозирани форми за инхалации“, „Трансдермални лепенки“, „Решенија“ и „Гранули со исечени цедени “.
Монографијата на Општата фармакопеја „Дозирани форми“ содржи основни термини и дефиниции, класификација на дозирани форми, општи барања за производство/производство, проценка на квалитетот, пакување, етикетирање и складирање на лекови во соодветни дозирани форми. Оваа монографија за општа фармакопеја содржи индикатори за квалитет кои се задолжителни за проценка на квалитетот на лекот во која било дозирана форма, како и индикатори за квалитет кои ги карактеризираат карактеристиките на производството/производството на лекот и неговите активни и помошни супстанции.
Воведена е 17 Општа фармакопеја монографија за дозирани форми за да се заменат соодветните написи на Државниот фонд на СССР, XI издание, со дополнувања и измени направени на нив.
Повеќето монографии на Општата фармакопеја за методи за проценка на фармацевтски и технолошки показатели за квалитетот на дозираните форми се вклучени во 13-тото издание на Државната фармакопеја на Руската Федерација за прв пат. Развиени се посебни OFS за методи на анализа претходно опишани во написите на Државната фармакопеја XI за дозирани форми (методи за одредување на волуменот на дозирани форми за парентерална употреба, абразија на таблети, време на целосна деформација на супозитории на база на липофили, распаѓање на таблети и капсули).
За прв пат е развиен и вклучен во Државниот фонд на Руската Федерација во XIII издание на Монографијата за Општа фармакопеја за такви методи за одредување фармацевтски и технолошки индикатори за квалитет на дозирани форми како „Видливи механички подмножества во дозирани форми за парентерална употреба и офталмолошки дозирани форми“, „Невидливи механички подмножества во дозирани форми за парентерална употреба“, „Тежина (волумен) на содржината на пакувањето“, „Униформност на дозирање“, „Еднообразност на масата на дозирани дозирани форми“, „Јачина на дробење на таблети“, „Дезинтеграција на супозитории и вагинални таблети“, „Распуштање за супозитории на база на липофилна основа“, „Степен на течност во прав“, „Распуштање за трансдермални фластери“.
Подсекцијата „Суровини од лековити растенија и методи на нејзина анализа“ вклучува 23 Општа фармакопеја и 55 FS. Барањата за земање примероци, складирање, пакување, етикетирање и транспорт на лековити растителни суровини и лековити билни препарати се претставени во потсекцијата „Општи написи“ во Монографијата на Општата фармакопеја „Земење примероци од лековити растителни суровини и лековити билни препарати“, Општа фармакопеја Монограф „Складирање на лековити растителни суровини и лековити билни препарати“ и Монографија на Општа фармакопеја „Пакување, етикетирање и транспорт на лековити билни суровини и лековити билни препарати“.
Општите барања за суровини за лековити растенија се дадени во Монографијата на Општата фармакопеја „Медицински растителни суровини“. 12 OFS се посветени на методи за анализа на лековити растителни материјали и лековити билни препарати. 8 Монографии на Општа фармакопеја ги опишуваат барањата за методи за анализа на лековити растителни материјали во зависност од морфолошките групи: цвеќиња, плодови, семиња, пупки, билки, лисја, кора и подземни органи. Во овој дел се претставени и 2 монографии на Општа фармакопеја за медицински производи од растително потекло: Монографија на Општа фармакопеја „Растителни масни масла“ и „Етерични масла“.
Монографијата на Општата фармакопеја „Суровини од лековити растенија“ беше развиена и вклучена за прв пат во Државниот фонд на Руската Федерација. Овој напис дава класификација на суровини од лековити растенија во зависност од морфолошките групи, мелењето, содржината на една или друга група биолошки активни супстанции, ги дава главните индикатори за квалитет на суровини од лековити растенија и општите барања за складирање и пакување.
Од 12 монографии на Општа фармакопеја за методи на анализа на суровини од лековити растенија, 3 монографии на Општа фармакопеја се вклучени во Државниот фонд на Руската Федерација во XIII издание за прв пат, 9 Монографии на Општа фармакопеја се ревидирани и воведени за да се заменат написите на Државниот фонд на СССР во XI-то издание. За прв пат вклучена во практиката на домашна фармакопеја анализа: Општа фармакопеја монографија „Определување на содржината на тешки метали и арсен во лековити растителни суровини и лековити растенија“
медицински препарати“, Монографија Општа фармакопеја „Определување содржина на резидуални пестициди во лековити растителни суровини и лековити билни препарати“, Монографија на Општа фармакопеја „Определување коефициент на апсорпција на вода и коефициент на потрошувачка на медицински растителни суровини“.
XIII издание на Државниот фонд на Руската Федерација вклучува нови видови лековити растителни суровини одобрени за медицинска употреба, како што се суво овошје од аронија, листови од гинко билоба, слатка трева од детелина и пупки од топола. Структурата на фармакопејските монографии за лековити растителни суровини е усогласена со барањата на светските фармакопески стандарди за лековити растителни суровини.
Подсекцијата „Групи на имунобиолошки медицински производи и методи на нивна анализа“ вклучува 43 монографии за Општа фармакопеја и 48 ФС за имунобиолошки лекови.
IMPs вклучуваат вакцини, токсоиди, серуми и алергени.
За прв пат, практиката на домашна фармакопеја анализа воведе OFS за поединечни групи на ILP, како што се „Третман и профилактички бактериофаги“, „Проботици“, „Проботици кои содржат бифид“, „Проботици што содржат Колакс“, „Лактоза -содржат пробиотици“, „Проботици кои содржат спори“ и „Лекови добиени со рекомбинантна ДНК методи“.
Од 48 FS за IMP вклучени во XIII издание на Државниот фонд на Руската Федерација, 5 FS беа развиени за прв пат во практиката на домашна фармакопеја анализа: „Вакцина против дизентерија против Shigella Sonne липополисахарид“, „Жива културна вакцина против рубеола ", "Инактивирана вакцина против сипаници", "Човечки имуноглобулин против сипаници" " ФС „Пирогени, ректални супозитории“ е развиен за прв пат во практиката на домашната и светската фармацевтска анализа.
Лековите од крв и крвна плазма на луѓе и животни се претставени со 13 OFS и 8 FS.
Медицинските производи од човечка крв и крвна плазма вклучуваат препарати од хуман албумин
ка, препарати за човечки имуноглобулин и препарати за фактор на коагулација на крв кои содржат еден од факторите на коагулација на крвта или нивна комбинација.
12 Општа фармакопеја Монографии за лекови од човечка и животинска крв и крвна плазма се претставени во XIII издание на Државната фармакопеја на Руската Федерација за прв пат.
Фармакопејалните монографии за фармацевтски супстанции од синтетичко и минерално потекло ги содржат хемиските имиња на лековите во согласност со барањата на Меѓународната унија за чиста и применета хемија (IUP), индикатори за квалитет, нивните стандардизирани вредности и соодветни методи за анализа на овие индикатори .
Методот на инфрацрвена спектрометрија, кој дава најсигурен резултат, се смета за главен метод за идентификација. За одреден број супстанции, 13-тото издание на Додатокот на Државниот фонд на Руската Федерација содржи цртежи на IR спектрите на стандардните примероци на овие фармацевтски супстанции.
За квантитативно определување, предност се дава на класичните титриметриски методи на анализа. Заедно со ова, широко се користат современи методи на физичка и хемиска анализа, како што се спектроскопија во ултравиолетовиот регион, гасна и течна хроматографија со високи перформанси, кои вклучуваат употреба на стандардни примероци. Содржината на активната супстанција е дадена во смисла на сува (ако се утврди губење на тежината при сушење), безводна (ако е одредена вода) или безводна супстанција која не содржи резидуални органски растворувачи.
Така, воведувањето во сила на Монографијата за Општа фармакопеја и ФС подготвени за следното, XIII издание на Државниот фонд на Руската Федерација не само што ќе ги укине или замени застарените написи на Државниот фонд на Руската Федерација од претходните изданија, туку исто така ќе обезбеди дека нивото на домашната фармакопеја анализа ги исполнува барањата на светските стандарди.
литература
1. Државна фармакопеја на СССР. 10-ти ед. М.: Медицина; 1968 година.
2. Државна фармакопеја на СССР. 11-ти ед. Vol. 1. М.: Медицина; 1987 година.
3. Државна фармакопеја на СССР. 11-ти ед. Vol. 2. М.: Медицина; 1989 година.
4. Државна фармакопеја на Руската Федерација. 12-ти ед. Дел 1. М.: Научен центар за експертиза на медицински производи; 2007 година.
Сојузна државна буџетска институција „Научен центар за експертиза на медицински производи“ на Министерството за здравство на Руската Федерација. Руска Федерација, 127051, Москва, булевар Петровски, 8.
Меркулов Вадим Анатолиевич. Првиот заменик генерален директор, д-р мед. науки, професор.
Сакањан Елена Ивановна. директор на Центарот за фармакопеја и меѓународна соработка, д-р Фарм. науки, професор.
Шемерјанкина Татјана Борисовна. Раководител на Одделот за државна фармакопеја и фармакопеја анализа, д-р. фарма. Sci. Мочикина Олга Алексеевна. Истражувач на Одделот за државна фармакопеја и фармакопеја анализа.
Буњатјан Наталија Дмитриевна. Заменик генерален директор за истражување, д-р Фарм. науки, професор.
1. Државна фармакопеја на СССР. 10-ти ед. Москва: Медицина; 1968 година (на руски).
2. Државна фармакопеја на СССР. 11-ти ед. V. 1. Москва: Медицина; 1987 година (на руски).
3. Државна фармакопеја на СССР. 11-ти ед. V. 2. Москва: Медицина; 1989 година (на руски).
4. Државна фармакопеја на Руската Федерација. 12-ти ед. V. 1. Москва: Федерална државна буџетска институција „Научен центар за стручна евалуација на лекови“ на Министерството за здравство на Руската Федерација; 2007 година (на руски).
Федерална државна буџетска институција „Научен центар за стручна евалуација на лекови“ на Министерството за здравство на Руската Федерација, булевар Петровски бр. 8, Москва, 127051, Руска Федерација.
Меркулов В.А. Првиот заменик генерален директор. Доктор на медицински науки, професор. Сакањан ЕИ. Директор на Центарот за фармакопеја и меѓународна соработка. Доктор на фармацевтски науки, професор.
Шемерјанкина ТБ. Раководител на Одделот за државна фармакопеја и анализа на фармакопеја. Кандидат за фармацевтски науки.
Мочикина О.А. Истражувач на Одделот за државна фармакопеја и анализа на фармакопеја.
Буњатјан Н.Д. Заменик генерален директор за научна работа. Доктор на фармацевтски науки, професор.
МИНИСТЕРСТВО ЗА ЗДРАВСТВО НА РУСКАТА ФЕДЕРАЦИЈА
ФАРМАКОПЕЈСКИ СТАТИИ
ЖеншенприсутникорениФС.2.5.0013.15
Панацис женшен радика За возврат за Глобалниот фондXI, кн. 2, уметност. 66
Собрано кон крајот на август - почетокот на септември и исушени корени на дивото и култивирано повеќегодишно тревно растение вистински женшен - Панакс женшен В. А. Меј, сем. Araliaceae - Araliaceae.
АВТЕНТИЧНОСТ
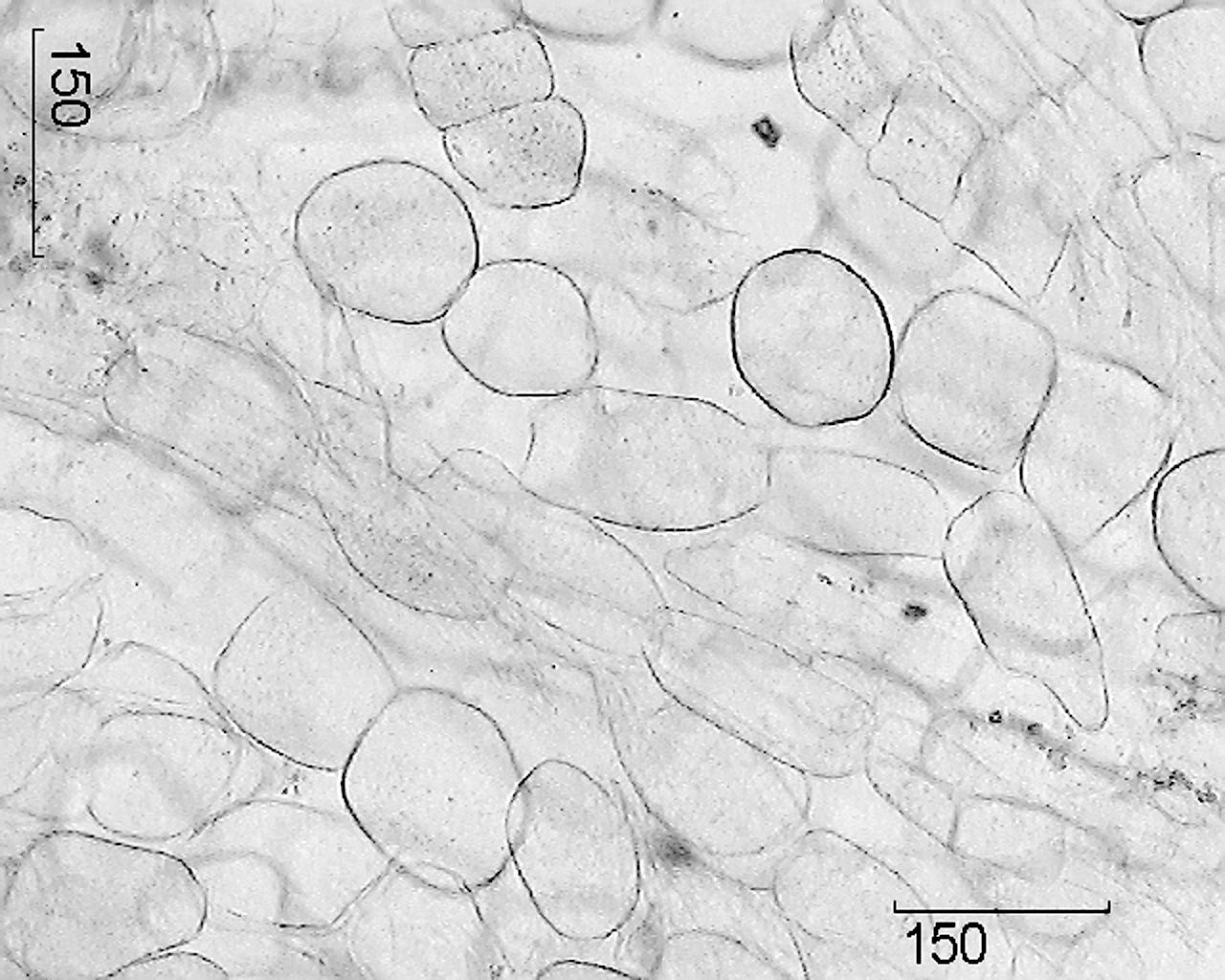
Надворешни знаци. Цели суровини.Корени долги до 25 cm, дебели 0,7–2,5 cm, со 2–5 големи гранки, поретко без нив. Корените се откорнати, надолжно, поретко спирално збрчкани, кревки, со рамномерна фрактура. „Телото“ на коренот е задебелено, речиси цилиндрично, со јасно дефинирани прстенести задебелувања на врвот. Во горниот дел на коренот има стеснет попречно збрчкан ризом - „врат“. Ризомот е краток со неколку лузни од паднатите стебла; на врвот формира „глава“, која е проширен остаток од стеблото и апикална пупка (понекогаш 2–3). Еден или повеќе непожелни корени понекогаш се протегаат од „вратот“. Можеби недостасуваат „вратот“ и „главата“. Бојата на корените на површината и на резот е жолтеникаво-бела, на свежа скршеница е бела. Мирисот е специфичен. Вкусот на екстрактот од вода е сладок, лут, а потоа зачинет-горчлив.
Мелени суровини.При испитување на смачканите суровини под лупа (10×) или стерео микроскоп (16×), видливи се парчиња корени со различни форми кои минуваат низ сито со дупки од 7 мм. Бојата на површината и на скршеницата е жолтеникаво-бела. Мирисот е специфичен. Вкусот на екстрактот од вода е сладок, лут, а потоа зачинет-горчлив.
Прашок. При испитување на прашокот под лупа (10×) или стерео микроскоп (16×), видлива е мешавина од смачкани честички од корени со различни форми со жолтеникаво-бела боја, кои минуваат низ сито со дупки од 2 мм. Мирисот е специфичен. Вкусот на екстрактот од вода е сладок, лут, а потоа зачинет-горчлив.
Микроскопски знаци. Цели суровини.Напречниот пресек на главниот корен открива тесен слој од светло-кафеав приклучок, широка кора, јасна линија на камбиум и дрво.
Главниот корен е покриен со перидерм, чии клетки се тенкоѕидни и лигнифицирани, несуберизирани. Флоемот и ксилемата се одделени со камбијалната зона, која поминува приближно низ средината на радиусот на коренот и
понекогаш тоа не е видливо. До периферијата, големоклеточните примарни радијални зраци на паренхимното ткиво се протегаат од примарниот ксилем, меѓу кој има секундарна ксилема, пресечена со бројни секундарни радијални зраци на главниот паренхим. Ксилемот се состои од тенкоѕидни паренхимски клетки кои содржат зрна скроб. Садовите на медуларните зраци имаат задебелени, лигнизирани ѕидови и се лоцирани поединечно или собрани во групи од 3-6. Клетките кои содржат жолти пигменти повремено се наоѓаат во дрвениот паренхим. Во центарот на коренот има нејасно препознатливи остатоци од примарна ксилема во форма на 2 зраци. Флоемот се состои главно од ситноклеточни елементи; содржи јасно видливи шизогени контејнери кои содржат капки секрет од светло жолта до црвено-кафеава. Зрната од скроб се мали, тркалезни, едноставни. Индивидуалните паренхимски клетки содржат друзен на калциум оксалат. Надворешниот дел на секундарниот кортекс се граничи со зона од неколку (4-6) редови на големи тангенцијално издолжени паренхимски клетки на фелодермот, тркалезни или овални, со малку задебелена обвивка.
|
|
||
|
|
|
|
|
|
|
|
Слика – Вистински корени од женшен.
1 – фрагмент од пресек на главниот корен (100×); 2 – фрагмент од плута (400×); 3 – фрагмент од пресек на адвентитивен корен: а – ксилемски садови, б – зрна скроб (400×); 4 – фрагмент од пресек на главниот корен со секреторен канал: а – обвивки на каналот, б – каналска празнина (400×); 5 – фрагмент од паренхимот на медуларните зраци: а – друзен од калциум оксалат, б – зрна скроб (400×); 6 – паренхимски клетки на медуларниот зрак (100×).
На пресек на адвентитивен корен, во центарот, зрак од садови од примарната ксилема е остаток од дијархичниот васкуларен сноп во примарната структура. Два сектори на секундарната ксилема се одделени со радијални зраци на главниот паренхим. Паренхимните клетки се тркалезни или овални, делумно или целосно исполнети со зрна скроб. Плута се состои од 5-7 слоеви правоаголни, тенкоѕидни ќелии, слабо лигнифицирани.
Мелени суровини. При испитување на притиснат примерок, треба да бидат видливи фрагменти од попречни и надолжни пресеци од главните и адвентивните корени.
Фрагментите од главниот корен се претставени со ксилемски зраци и садови, кои ги пополнуваат клетките на паренхимите на медуларните зраци со зрна од скроб, каналните шуплини и клетките на обвивката, клетките на паренхимите со пигменти и клетките на камбиумот.
Фрагментите од адвентитивниот корен се претставени со приклучоци, паренхим со зрна од скроб, садови, примарен и секундарен кортекс, садови, медуларни зраци.
Прашок.При испитување на микрослајд, видливи се фрагменти од епидермисот, плута, дрвото, паренхимот, како и друзен на калциум оксалат.
Одредување на главните групи на биолошки активни супстанции
Хроматографија со тенок слој
На почетната линија на аналитичка хроматографска плоча со слој силика гел со флуоресцентен индикатор со димензии 10 × 15 cm на алуминиумска подлога, нанесете 20 μl од испитниот раствор (види дел „Квантитативно определување“, подготовка на растворот А од тест раствор) и 50 μl стандарден примерок раствор (SS) на панаксосид Rg 1 (види дел „Квантитативно определување“ подготовка на раствор A CO панаксосид Rg 1). Плочата со нанесените примероци се суши на воздух, се става во комора, претходно се заситува најмалку 2 часа со растворувач мешавина од хлороформ - метанол - вода (26:14:3) и се хроматографија со асцендентна метода. Кога предниот дел на растворувачот поминува околу 80-90% од должината на плочата од почетната линија, тој се отстранува од комората, се суши додека не се отстранат трагите од растворувачите, се третира со фосфотонгстинска киселина со 20% алкохолен раствор и се загрева во рерната на 100–105 °C 3 минути, по што се гледа на дневна светлина.
Хроматограмот на испитниот раствор треба да покаже најмалку 6 зони на адсорпција од светло розова до темно розова; доминантната зона е на ниво на зона во хроматограмот на CO растворот на панаксосид Rg 1 ; дозволено е откривање на други адсорпциони зони.
Кога капка концентрирана сулфурна киселина ќе се нанесе на прашокот од коренот на женшен по 1-2 минути, се појавува тула-црвена боја, која се претвора во црвено-виолетова, а потоа виолетова (панаксозид).
Тестови
Влажност. Цели суровини мелени суровини, прав -не повеќе од 13%.
Обична пепел. Цели суровини мелени суровини, прав -не повеќе од 5%.
Пепел, нерастворлив во хлороводородна киселина. Цели суровини мелени суровини, прав -не повеќе од 2%.
Мелење на суровини.Цели суровини:честички што минуваат низ сито со дупки со големина од 3 mm - не повеќе од 5%. Скршени суровини:честички кои не минуваат низ сито со дупки со големина од 7 mm - не повеќе од 5%; честички што минуваат низ сито со дупки со големина од 0,5 mm - не повеќе од 5%. Прашок:честички кои не минуваат низ сито со дупки со големина од 2 mm - не повеќе од 5%; честички кои минуваат низ сито со дупки со големина од 0,18 mm - не повеќе од 5%.
Надворешна материја
Корените се затемнети од површината . Цели суровини мелени суровини -не повеќе од 3%.
Органска нечистотија. Цели суровини мелени суровини -не повеќе од 0,5%.
Минерална нечистотија . Цели суровини, мелени суровини, прав -не повеќе од 1%.
Тешки метали. Во согласност со барањата на Монографијата на Општата фармакопеја „Одредување на содржината на тешки метали и арсен во лековити растителни материјали и лековити билни препарати“.
Радионуклиди.Во согласност со барањата на Монографијата на Општата фармакопеја „Одредување на содржина на радионуклиди во лековити растителни материјали и лековити билни препарати“.
Остатоци од пестициди. Во согласност со барањата на Монографијата на Општата фармакопеја „Одредување на содржината на резидуални пестициди во лековити растителни материјали и лековити билни препарати“.
Микробиолошка чистота.Во согласност со барањата на Монографијата на Општата фармакопеја „Микробиолошка чистота“.
квантификација. Цели суровини мелени суровини, прав:количината на панаксозиди во однос на панаксосид Rg 1 - не помала од 2%; екстрактивни материи извлечени со 70% алкохол - најмалку 20%.
(„Државна фармакопеја на Руската Федерација. XIII издание. Том I“)
Овој општ фармакопејален член ги утврдува општите барања за складирање на фармацевтски супстанции, помошни супстанции и лекови и се однесува на сите организации во кои се складира медицински производи, земајќи го предвид видот на активноста на организацијата.
Складирањето на лековити растителни суровини и лековити билни препарати се врши во согласност со Монографијата на Општата фармакопеја „Складирање на лековити растителни суровини и лековити билни препарати“.
Складирање- процесот на чување на лековите додека не се искористат во утврдениот рок на траење, што е составен дел од циркулацијата на лековите.
Општи барања за капацитети за складирање
лекови и организација на нивното складирање
Складирањето на лековите мора да се врши во простории наменети за овие цели. Дизајнот, составот, димензиите на местата за складирање, нивната работа и опремата мора да обезбедат соодветни услови за складирање на различни групи лекови.
Комплексот на капацитети за складирање треба да вклучува:
- соба за прием (област) наменета за отпакување и примање пакувања со лекови и нивна прелиминарна проверка;
- просторија (зона) за земање мостри од лекови во согласност со барањата на Монографијата на Општата фармакопеја „Земење примероци“;
- просторија (зона) за карантинско складирање на лекови;
- простории за лекови кои бараат посебни услови за складирање;
- просторија (област) за складирање на одбиени, вратени, отповикани и/или лекови со истечен рок Наведените лекови и нивните локации за складирање мора да бидат јасно означени.
Областа за складирање е распределена во заедничка просторија за складирање во отсуство на посебна изолирана просторија.
Завршувањето на просториите за складирање на лекови мора да ги исполнува тековните санитарни и хигиенски барања; внатрешните површини на ѕидовите и таваните мора да бидат мазни, што овозможува влажно чистење.
Во секоја просторија за складирање потребно е да се одржуваат климатските услови, со запазување на температурата и влажноста утврдени со фармакопејската монографија или регулаторната документација за лекови.
Потребната размена на воздух во просториите за складирање се создава со помош на климатизери, вентилација за снабдување и издувни гасови или друга опрема. Природното и вештачкото осветлување во просториите за складирање мора да обезбеди точно и безбедно спроведување на сите операции извршени во просторијата. Доколку е потребно, треба да се обезбеди заштита на медицинските производи од сончево зрачење.
Просториите за чување лекови мора да бидат опремени со потребниот број на прописно проверени мерни инструменти (термометри, хигрометри, психрометри итн.) за следење и снимање на температурата и влажноста, што се врши најмалку еднаш дневно.
Мерните инструменти се поставуваат на растојание од најмалку 3 метри од вратите, прозорците и уредите за греење на место достапно за читање, на висина од 1,5-1,7 метри од подот. Во исто време, се препорачува да се постават на места каде што постои најголема веројатност за флуктуации на температурата и влажноста или најчесто се забележуваат отстапувања од бараните параметри.
Евиденцијата за регистрација мора да ги демонстрира условите за температура и влажност утврдени во просториите и, доколку тие не се усогласени, корективни дејства.
Просториите за складирање мора да бидат опремени со доволен број кабинети, сефови, лавици, складишни единици и палети. Опремата мора да биде во добра состојба и чиста.
Полиците, шкафовите и другата опрема мора да се инсталираат на таков начин што ќе обезбедат пристап до лекови, слободен премин на персоналот и, доколку е потребно, достапност на операциите на товарење и растоварање, како и достапност до опремата, ѕидовите и подовите на просторијата. за чистење.
Во просториите за чување лекови мора да се одржуваат соодветни санитарни услови. Фреквенцијата и методите на чистење на просториите мора да бидат во согласност со барањата на регулаторните документи. Употребените санитарни средства за дезинфекција мора да бидат безбедни; ризикот од контаминација на складираните лекови со овие производи мора да се елиминира.
Треба да се развијат специфични упатства за чистење на истурените или расфрлани медицински производи за да се обезбеди целосна елиминација и да се спречи контаминација на други медицински производи.
При вршење работи во простории за чување лекови, вработените мора да носат посебна облека и обувки и да ги почитуваат правилата за лична хигиена.
Во просториите за складирање, лековите се ставаат во согласност со условите за складирање наведени во фармакопејскиот напис или во регулаторната документација за лековите, земајќи ги предвид нивните физичкохемиски и опасни својства, фармаколошките и токсиколошките ефекти, видот на дозирана форма на лекот и начинот на неговата употреба, агрегатната состојба на лекот. При користење на компјутерска технологија, дозволено е ставање на лекови по азбучен ред, по шифра.
Мора да се идентификуваат решетките, кабинетите и полиците наменети за чување лекови. Исто така, неопходно е да се идентификуваат складираните лекови со помош на решетката картичка или, кога се користи компјутерска технологија, со користење на шифри и електронски уреди.
Кога операциите за растовар и товарење се вршат рачно, висината на редење на лековите не треба да надминува 1,5 метри. Кога се користат механизирани уреди за време на операциите на истовар и товарење, лековите треба да се чуваат во неколку нивоа. Во исто време, вкупната висина на поставување на лекови на решетките не треба да ги надминува можностите на механизмите за товарење и растоварување.
Лековите во просториите за складирање мора да се ставаат во кабинети, лавици, полици, палети итн. Не е дозволено ставање лекови на подот без палета.
Палетите може да се постават на подот во еден ред или на лавици во неколку нивоа, во зависност од висината на решетката. Не е дозволено да се поставуваат палети со лекови во повеќе редови во висина без употреба на лавици.
Кога се создаваат услови за чување на одреден лек, неопходно е да се води според барањата наведени во фармакопејската монографија или регулаторната документација за овој лек, утврдена од производителот (програмер) на лекот врз основа на резултатите од стабилноста. студија во согласност со Монографијата на Општата фармакопеја „Рок на употреба на медицинските производи“.
Лековите се чуваат во пакување (потрошувачка, група) што ги задоволува барањата на регулаторната документација за овој лек.
Лековите се чуваат на релативна влажност од не повеќе од 60%+/-5% во зависност од релевантната климатска зона (I, II, III, IVA, IVB), освен ако не се наведени посебни услови за складирање во регулаторната документација.
Лековите треба да се чуваат за да се спречи контаминација, мешање и вкрстена контаминација. Неопходно е да се избегнуваат туѓи мириси во местата за складирање.
Во организацијата мора да се имплементира систем за евидентирање на лекови со ограничен рок на употреба. Доколку се складираат неколку серии со исто име на лекот, тогаш лекот чиј рок на траење истекува порано од другите треба прво да се земе за употреба.
Одбиените медицински производи мора да се идентификуваат и да се чуваат во соодветна просторија (област) под услови кои не дозволуваат нивна неовластена употреба.
Карактеристики на складирање на одредени групи на лекови
Лековите со опасни својства (запаливи, експлозивни, радиофармацевтски, каустични, корозивни, компресирани и течни гасови итн.) треба да се чуваат во специјално дизајнирани простории опремени со дополнителна безбедносна и безбедносна опрема.
За време на складирањето, неопходно е да се обезбеди безбедност и деклариран квалитет на лековите, да се спречи можноста лековите да ги покажат своите опасни својства и да се создадат безбедни работни услови за вработените кои работат со такви лекови.
При уредување на простории и организирање складирање на опасни лекови, неопходно е да се води според барањата на федералните закони и регулаторните правни акти на Руската Федерација.
Складирањето на наркотични и психотропни лекови мора да се врши во согласност со федералните закони и прописи на Руската Федерација.
При складирање на лекови кои бараат заштита од влијанието на факторите на животната средина (светлина, температура, атмосферски состав на воздухот итн.), Потребно е да се обезбеди режим на складирање наведен во фармакопејската монографија или регулаторната документација. Отстапувањата од регулираните услови се дозволени само еднаш за краток период (не повеќе од 24 часа), освен ако посебните услови, на пример, трајно складирање на ладно место, не се посебно наведени.
Лековите кои можат да ги променат своите својства под влијание на светлосната енергија (оксидираат, намалуваат, се распаѓаат, ја менуваат бојата итн.) се чувствителни на фотографија или светлина; лековите кои се отпорни на светлина се фотостабилни. Влијанието на светлосната енергија може да се манифестира со изложување на директна сончева светлина, расфрлана светлина во видливиот регион на светлосниот спектар и зрачење во ултравиолетовиот регион.
Обележувањето на фотосензитивните лекови обично го содржи упатството: „Чувајте го на место заштитено од светлина“. Лековите кои бараат заштита од светлина треба да се чуваат во простории или специјално опремени места кои обезбедуваат заштита од природна и вештачка светлина.
Фармацевтските супстанции за кои е потребна заштита од светлина треба да се чуваат или во амбалажа направена од материјали за заштита од светлина или во темна просторија или кабинет. Ако се користат стаклени садови за лекови за пакување на фармацевтски супстанции кои се особено чувствителни на светлина, садот мора да биде покриен со црна хартија отпорна на светлина.
Фотосензитивните медицински производи треба да се пакуваат во секундарно пакување кое штити од светлина и/или треба да се чува на место заштитено од светлина.
Лековите кои кога се во контакт со вода, влага, можат да испуштаат гасови и слично, се чувствителни на влага. Обележувањето на лековите чувствителни на влага обично го содржи упатството: „Чувајте го на суво место“.
При складирање на такви лекови, неопходно е да се осигура дека релативната влажност не надминува 50% на собна температура (при нормални услови на складирање) или еквивалентен притисок на пареа на друга температура. Исполнувањето на барањето предвидува и складирање на медицински производ чувствителен на влага во херметички (непропустливи) потрошувачки пакувања што ја обезбедува наведената заштита и усогласеност со условите за складирање за време на циркулацијата на лекот.
За одржување на ниска содржина на влага за време на складирањето на лековите, средствата за сушење се користат во пропишани случаи, под услов да се избегнува нивниот директен контакт со лекот.
Лековите со хигроскопски својства мора да се чуваат на релативна влажност од не повеќе од 50% во пакување, кое е стаклен сад за лекови, херметички затворен или во пакување со дополнителна заштита, на пример, во пластична кеса, во согласност со барањата на фармакопејската монографија или регулаторната документација.
Некои групи на лекови ги менуваат своите својства под влијание на атмосферски гасови, како што се кислород или јаглерод диоксид. За да се обезбеди заштита на лековите од ефектите на гасовите, се препорачува лековите да се чуваат во затворено пакување направено од материјали непропустливи за гасови. Ако е можно, пакувањето треба да се наполни до врвот и цврсто да се затвори.
Лекови кои се всушност испарливи лекови или лекови кои содржат испарлив растворувач; раствори и мешавини на испарливи материи; Лековите кои се распаѓаат со формирање на испарливи производи бараат услови за складирање кои ги штитат од испарување и сушење. Се препорачува лековите да се чуваат на ладно место, во херметички затворено пакување од материјали непропустливи за испарливи материи или во примарно и секундарно (потрошувачко) пакување во согласност со барањата наведени во фармакопејската монографија или регулаторната документација.
Лековите, кои се фармацевтски супстанци кои содржат вода за кристализација (кристално хидрати), покажуваат својства на хигроскопски супстанции. Се препорачува да се чуваат кристалните хидрати во херметички затворено пакување во согласност со барањата наведени во фармакопејската монографија или регулаторната документација. Како по правило, кристалните хидрати се чуваат на температури од 8 до 15 ° C и релативна влажност на воздухот не повеќе од 60%.
Лековите кои ги менуваат својствата под влијание на температурата на околината се термочувствителни. Лековите можат да ги променат своите својства кога се изложени на собна температура или повисока (лекови кои се отпорни на топлина) или кога се изложени на ниски температури, вклучително и замрзнување.
При складирање на лекови чувствителни на топлина, неопходно е да се обезбеди температурен режим регулиран со барањата на фармакопејската монографија или регулаторната документација наведена на примарното и/или секундарното (потрошувачко) пакување на лекот.
Лековите кои се отпорни на топлина треба да се чуваат во специјално опремени простории (фрижидери) или во простории за складирање опремени со доволен број ладилни кабинети и фрижидери. За складирање на термолабилни лекови треба да се користат фармацевтски фрижидери или фрижидери за крв и крвни продукти.
Соодветниот квалитет на имунобиолошките лекови, безбедноста и ефективноста на нивната употреба е обезбедена со системот „ладен синџир“, кој мора да се имплементира на сите четири нивоа.
Резолуција на главниот државен санитарен лекар на Руската Федерација бр. 15 од 10 април 2002 година „За спроведување на санитарните и епидемиолошките правила СП 3.3.2.1120-02“
Фрижидерите (коморите, кабинетите) мора да се постават на температура што одговара на температурните услови за чување на лековите содржани во нив. Имунобиолошките медицински производи треба да се чуваат на температура не поголема од 8 °C. Секое пакување имунобиолошки медицински производ во фрижидер мора да има пристап до ладен воздух. Имунобиолошките лекови не треба да се чуваат заедно во фрижидер со други медицински производи.
За следење на температурните услови на складирање на термолабилни лекови, сите фрижидери (комори, кабинети) мора да бидат опремени со термометри. Континуирано следење на температурниот режим се врши со помош на термографи и температурни рекордери, чии читања се снимаат најмалку два пати на ден.
Температурниот режим на полиците на фрижидерот е различен: температурата е пониска во близина на одделот за замрзнување, повисока во близина на панелот на вратата за отворање.
Обезбедувањето ладно место значи чување на лековите во фрижидер на температура од 2 до 8 ° C, избегнувајќи замрзнување. Складирањето на ладно значи складирање на лекови на температура од 8 до 15 °C. Во овој случај, дозволено е чување на лекови во фрижидер, со исклучок на лекови кои, кога се чуваат на температура во фрижидер под 8 ° C, можат да ги променат нивните физички и хемиски карактеристики, на пример, тинктури, течни екстракти итн.
Складирањето на собна температура подразбира температурен опсег од 15 до 25 °C или, во зависност од климатските услови, до 30 °C. Складирањето во замрзнувач обезбедува температура на лековите од -5 до -18 °C. Складирањето во длабоко замрзнување бара температури под -18 °C.
Препорачливо е лековите да се ставаат на места и на полици во фрижидер кои одговараат на нивните температурни услови за складирање. Не е дозволено чување имунобиолошки лекови на плочата на вратата од фрижидерот.
Во просториите за складирање, неопходно е да се обезбедат услови за складирање на лекови кои бараат заштита од изложување на ниски температури, за кои фармакопејската монографија или регулаторната документација поставува пониска температурна граница за складирање.
Не е дозволено замрзнување на лекови кои ги имаат соодветните барања во фармакопејската монографија или регулаторната документација и се наведени на примарното или секундарното пакување, вклучително и инсулински препарати, адсорбирани имунобиолошки препарати итн.
Не е дозволено замрзнување на лекови сместени во амбалажа кои можат да се уништат со замрзнување, на пример, лекови во ампули, стаклени шишиња итн.
Дефинициите употребени во фармакопејата кои ги карактеризираат температурните услови за складирање на лекови се дадени во табелата.
Неопходно е да се обезбеди усогласеност со условите за складирање на лековите и одржување на нивниот интегритет за време на транспортот.
За лекови кои се особено чувствителни на промени во температурата (вакцини, серуми и други имунобиолошки медицински производи, инсулински медицински производи итн.), за време на транспортот мора да се почитува температурниот режим регулиран со фармакопејската монографија или регулаторната документација.
Дефиниции кои ги карактеризираат начините на складирање на лекови