Структурата на атомот на телуриум. Телуриум. Опис на телуриум. Својства на телуриумот Во кое семејство припаѓа телуриумот?
ДЕФИНИЦИЈА
Телуриумлоцирани во петтиот период од VI групата на главната (А) подгрупа на Периодниот систем.
Се однесува на елементи стр- семејства. Металоиден. Ознака - Те. Сериски број - 52. Релативна атомска маса - 127,60 аму.
Електронска структура на атомот на телуриум
Атомот на телуриум се состои од позитивно наелектризирано јадро (+52), внатре во кое има 52 протони и 76 неутрони, а 52 електрони се движат наоколу во пет орбити.
Сл.1. Шематска структура на атом на телуриум.
Распределбата на електроните меѓу орбиталите е како што следува:
52Те) 2) 8) 18) 18) 6 ;
1с 2 2с 2 2стр 6 3с 2 3стр 6 3г 10 4с 2 4стр 6 4г 10 5с 2 5стр 4 .
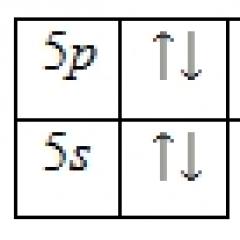
Надворешното енергетско ниво на атомот на телуриум содржи 6 електрони, кои се валентни електрони. Енергетскиот дијаграм на основната состојба ја има следната форма:

Валентните електрони на атом на телуриум може да се карактеризираат со множество од четири квантни броеви: n(главен квантум), л(орбитална), m l(магнетна) и с(врти):
|
Подниво |
||||
Примери за решавање проблеми
ПРИМЕР 1
Така, за честичките S +6, S 0, S +4 и S -2, вкупниот број на електрони во електронските обвивки ќе биде 10, 16, 12 и 18, соодветно. Тогаш табелата ќе изгледа вака:
ПРИМЕР 2
Така, за честичките C +4, Al +3, F и C 0, вкупниот број на електрони во електронските обвивки ќе биде еднаков на 2, 10, 10 и 6, соодветно. Тогаш табелата ќе изгледа вака:
|
телуриум елемент, телуриум Википедија
Телуриум / Tellurium (Te), 52
(моларна маса)
127,60 (3) а. e.m. (g/mol)
(+6e) 56.211 (−2e) pm
2.1 (Полинг скала)
6, +4 , +2, −2
(прв електрон)
869,0 (9,01) kJ/mol (eV)
17,91 kJ/mol
49,8 kJ/mol
25,8 J/(K mol)
20,5 cm³/mol
шестоаголна
(300 K) 14,3 W/(m K)
| 52 | |
| Те 127,60 | |
| 4d105s25p4 | |
Телуриум- хемиски елемент од 16-та група (според застарената класификација - главната подгрупа од групата VI, халкогени), 5-ти период во периодниот систем, има атомски број 52; означено со симболот Те(лат. Tellurium), спаѓа во семејството на металоиди.
- 1. Историја
- 2 Потекло на името
- 3 Да се биде во природа
- 3.1 Видови депозити
- 4 Потврда
- 4.1 Цени
- 5 Физички својства
- 6 Хемиски својства
- 7 изотопи
- 8 Апликација
- 8.1 Легури
- 8.2 Термоелектрични материјали
- 8,3 Полупроводници со тесен јаз
- 8.4 Високотемпературна суперспроводливост
- 8.5 Производство на гума
- 8.6 Производство на чалкогенидни чаши
- 8.7 Извори на светлина
- 8,8 CD-RW
- 9 Биолошка улога
- 9.1 Физиолошки ефект
- 10 Белешки
- 11 Врски
Приказна
За прв пат бил откриен во 1782 година во златните руди на Трансилванија од страна на рударскиот инспектор Франц Јозеф Милер (подоцна барон фон Рајхенштајн), на територијата на Австро-Унгарија. Во 1798 година, Мартин Хајнрих Клапрот го изолирал телуриумот и ги утврдил неговите најважни својства.
потеклото на името
Од латинскиот телус, генитив телурис, Земја.
Да се биде во природа
Содржината во земјината кора е 1·10−6% по маса. Познати се околу 100 минерали на телуриум. Најчести телуриди се бакар, олово, цинк, сребро и злато. Во многу сулфиди е забележана изоморфна мешавина на телуриум, но изоморфизмот Te - S е помалку изразен отколку во серијата Se - S, а сулфидите содржат ограничена мешавина на телуриум. Помеѓу минералите на телуриум, алтаит (PbTe), силванит (AgAuTe4), калаверит (AuTe2), хесит (Ag2Te), кренерит, петзит (Ag3AuTe2), мутманит, монтбреуит (Au2Te3), нагиагит (2Te3), особено тетраемит (4) важност. Постојат кислородни соединенија на телуриум, на пример, TeO2 - телуриум окер.
Домашниот телуриум се јавува и заедно со селенот и сулфурот (јапонскиот телуричен сулфур содржи 0,17% Te и 0,06% Se).
Видови депозити
Повеќето од споменатите минерали се развиени во нискотемпературни наоѓалишта на злато-сребро, каде што обично се изолираат по најголемиот дел од сулфидите заедно со природното злато, сулфосолите на среброто, олово, а исто така и со минералите на бизмут. И покрај развојот на голем број минерали на телуриум, најголемиот дел од телуриумот извлечен од индустријата е дел од сулфиди на други метали. Особено, телуриумот, во нешто помала мера од селенот, е вклучен во составот на халкопирит во бакар-никелските наслаги од магматично потекло, како и халкопирит развиен во хидротермалните наоѓалишта на бакар пирит. Телуриум се наоѓа и во пирит, халкопирит, молибденит и галена на наоѓалишта на порфирска бакарна руда, полиметални наоѓалишта од типот Алтај, галена на наоѓалишта на олово-цинк поврзани со скарни, сулфид-кобалт, антимон-жива и некои други. Содржината на телуриум во молибденит се движи од 8-53 g/t, во халкопирит 9-31 g/t, во пирит - до 70 g/t.
Потврда
Главен извор е тињата од електролитичко рафинирање на бакар и олово. Тињата се отпушта, телуриумот останува во гарежот, кој се мие со хлороводородна киселина. Телуриумот се изолира од добиениот раствор на хлороводородна киселина со поминување на сулфур диоксид SO2 низ него.
Сулфурна киселина се додава за да се одделат селенот и телуриумот. Во овој случај, телуриум диоксид TeO2 паѓа, а H2SeO3 останува во раствор.
Телуриумот се редуцира од TeO2 оксид со јаглен.
За прочистување на телуриумот од сулфур и селен, се користи неговата способност, под влијание на редукционо средство (Al, Zn) во алкална средина, да се трансформира во растворлив динатриум дителлурид Na2Te2:
За да се таложи телуриум, воздухот или кислородот се пренесуваат низ растворот:
За да се добие телуриум со посебна чистота, тој се хлорира
Добиениот тетрахлорид се прочистува со дестилација или ректификација. Тетрахлоридот потоа се хидролизира со вода:
,а добиениот TeO2 се редуцира со водород:
Цените
Телуриумот е редок елемент, а значителната побарувачка со мал обем на производство ја одредува неговата висока цена (околу 200–300 долари за кг, во зависност од чистотата), но и покрај тоа, опсегот на неговите апликации постојано се шири.
Физички својства
Телуриумот е кршлива, сребрено-бела супстанција со метален сјај. во тенки слоеви, кога е изложен на светлина, црвено-кафеава, во парови, златно-жолта. Кога се загрева, станува пластична. Кристалната решетка е хексагонална. Коефициентот на термичка експанзија е 1,68·10-5 K−1. Дијамагнетна. Полупроводник со бенд јаз од 0,34 eV, тип на спроводливост - p во нормални услови и при покачени температури, n - при ниски температури (гранична на премин - од минус 80 до минус 100 ° C, во зависност од чистотата).
Хемиски својства
Во хемиските соединенија, телуриумот покажува состојби на оксидација -2; +2; +4; +6. Тој е аналог на сулфур и селен, но е хемиски помалку активен од сулфурот. Се раствора во алкали, подложен е на дејството на азотни и сулфурни киселини, но е слабо растворлив во разредена хлороводородна киселина. Металот телуриум почнува да реагира со вода на 100 °C.
Со кислородот формира соединенија TeO, TeO2, TeO3. во форма на прав, се оксидира во воздухот дури и на собна температура, формирајќи TeO2 оксид. Кога се загрева во воздух, гори, формирајќи TeO2 - силно соединение кое е помалку испарливо од самиот телуриум. Ова својство се користи за прочистување на телуриумот од оксиди, кои се редуцираат со водород што тече на температура од 500-600 °C. Телуриум диоксидот е слабо растворлив во вода, но растворлив во кисели и алкални раствори.
Во стопена состојба, телуриумот е прилично инертен, па графитот и кварцот се користат како контејнерски материјали при неговото топење.
Телуриумот формира соединение со водород кога се загрева, лесно реагира со халогени и е во интеракција со сулфур и фосфор и метали. Кога реагира со концентрирана сулфурна киселина, формира сулфит. Формира слаби киселини: хидротелурна киселина (H2Te), телурна киселина (H2TeO3) и телуринска киселина (H6TeO6), чии повеќето соли се слабо растворливи во вода.
Изотопи
Главна статија: Изотопи на телуриумПознати се 38 нуклиди и 18 нуклеарни изомери на телуриум со атомски броеви од 105 до 142. Телуриумот е најлесниот елемент, чии познати изотопи се предмет на алфа распаѓање (изотопи од 106Te до 110Te). Атомската маса на телуриум (127,60 g/mol) ја надминува атомската маса на следниот елемент, јод (126,90 g/mol).
Во природата се јавуваат осум изотопи на телуриум. Шест од нив, 120Te, 122Te, 123Te, 124Te, 125Te и 126Te, се стабилни. Останатите два - 128Te и 130Te - се радиоактивни, и двата се подложени на двојно бета распаѓање, претворајќи се во ксенонски изотопи 128Xe и 130Xe, соодветно. Стабилните изотопи сочинуваат само 33,3% од вкупната количина на телуриум пронајдена во природата, што е овозможено со екстремно долгиот полуживот на природните радиоактивни изотопи. Тие се движат од 7,9·1020 до 2,2·1024 години. Изотопот 128Te има најдолг потврден полуживот од кој било радионуклид - 2,2 1024 години или 2,2 септилиони години, што е околу 160 трилиони пати повеќе од проценетата старост на Универзумот.
Апликација
Легури
Телуриумот се користи во производството на оловни легури со зголемена еластичност и цврстина (се користи, на пример, во производството на кабли). Со воведувањето на 0,05% телуриум, загубата на оловото поради растворање под влијание на сулфурна киселина се намалува за 10 пати, а тоа се користи во производството на оловно-киселински батерии. Исто така, важно е оловото легирано со телуриум да не омекне кога се обработува со пластична деформација, а тоа овозможува да се користи технологијата за производство на батериски тековни колектори со методот на ладно сечење и значително да се зголеми работниот век и специфичните карактеристики на батеријата. .
Термоелектрични материјали
Бизмут телурид еден кристалНеговата улога е исто така голема во производството на полупроводнички материјали и особено телуриди на олово, бизмут, антимон и цезиум. Во наредните години, производството на лантанидни телуриди, нивните легури и легури со метални селениди ќе станат многу важни за производство на термоелектрични генератори со многу висока (до 72-78%) ефикасност, што ќе овозможи нивна употреба во енергетскиот сектор и во автомобилската индустрија.
На пример, многу висок термички емф неодамна беше откриен во манган телурид (500 μV/K) и во неговата комбинација со бизмут, антимон и селениди на лантанид, што овозможува не само да се постигне многу висока ефикасност во термогенераторите, туку и да се имплементирајте го во една фаза полупроводнички фрижидер ладење до криогени (температурно ниво на течен азот) температури, па дури и пониски. Најдобриот материјал базиран на телуриум за производство на полупроводнички фрижидери во последниве години е легура на телуриум, бизмут и цезиум, што овозможи да се добие рекордно ладење до -237 °C. Во исто време, како термоелектричен материјал, ветувачка е легура на телуриум-селен (70% селен), која има коефициент на термо-EMF од околу 1200 μV/K.
Полупроводници со тесен јаз
Апсолутно исклучителна важност добија и легурите на CRT (кадмиум-жива-телуриум), кои имаат фантастични карактеристики за откривање на радијацијата од лансирање на ракети и набљудување на непријателот од вселената преку атмосферски прозорци (облачноста не е важна). MCT е еден од најскапите материјали во модерната електронска индустрија.
Високотемпературна суперспроводливост
Голем број системи кои содржат телуриум неодамна открија во нив постоење на три (можеби четири) фази, во кои суперспроводливоста не исчезнува на температура малку над точката на вриење на течниот азот.
Производство на гума
Посебна област на примена на телуриум е неговата употреба во процесот на вулканизација на гума.
Производство на чалкогенидни чаши
Телуриумот се користи за топење на специјални степени на стакло (каде што се користи во форма на диоксид); специјални очила допирани со метали од ретки земји се користат како активни тела во оптичките квантни генератори.
Покрај тоа, некои очила на база на телуриум се полупроводници, својство што се користи во електрониката.
Специјални оценки на телуриумско стакло (предностите на таквото стакло се проѕирност, фузибилност и електрична спроводливост) се користат во изградбата на специјална хемиска опрема (реактори).
Извори на светлина
Телуриумот наоѓа ограничена употреба во производството на светилки со неговите пареи - тие имаат спектар многу близок до оној на сонцето.
CD-RW
Легурата на телуриум се користи во компактни дискови што можат да се препишуваат (особено, Mitsubishi Chemical Corporation брендот „Verbatim“) за да се создаде деформабилен рефлективен слој.
Биолошка улога
Микро количини на телуриум секогаш се наоѓаат во живите организми; неговата биолошка улога не е јасна.
Физиолошко дејство
Телуриумот и неговите испарливи соединенија се токсични. Ако влезе во телото, предизвикува гадење, бронхитис и пневмонија. MPC во воздухот варира за различни соединенија 0,007-0,01 mg/m³, во вода 0,001-0,01 mg/l. Канцерогеноста на телуриумот не е потврдена.
Општо земено, соединенијата на телуриум се помалку токсични од соединенијата на селен.
Во случај на труење, телуриумот се излачува од телото во форма на испарливи органотелуриумски соединенија со непријатен мирис - алкил телуриди, главно диметил телурид (CH3)2Te. Нивниот мирис потсетува на лук, па кога дури и мали количини телуриум влегуваат во телото, воздухот што го издишува човекот го добива овој мирис, што е важен симптом на труење со телуриум.
Белешки
- Мајкл Е. Визер, Норман Холден, Тајлер Б. Гленда О'Конор, Томас Валчик, Шиге Јонеда, Ксијанг-Кун Жу. Атомски тежини на елементите 2011 (IUPAC Technical Report) // Чиста и применета хемија. - 2013. - Ред. 85, бр. 5. - P. 1047-1078. - DOI: 10.1351/PAC-REP-13-03-02.
- Tellurium: electronegativities (англиски). WebElements. Преземено на 5 август 2010 година.
- Leddicotte, G. W. (1961), „Радиохемијата на телуриумот“, серијал за нуклеарни науки, Поткомитет за радиохемија, Национална академија на науките-Национален совет за истражување, стр. 5,
- Редакциски тим: Зефиров Н.С. (главен уредник). Хемиска енциклопедија: во 5 тома - Москва: Советска енциклопедија, 1995. - Т. 4. - стр. 514. - 639 стр. - 20.000 примероци. - ISBN 5-85270-039-8.
- WebElements Периодичен систем на елементите | Телуриум | кристални структури
- Глинка Н.Л. Општа хемија. - М.: „Хемија“, 1977 година, ревидирана. - P. 395. - 720 стр.
- 1 2 3 4 Телуриум - статија од Големата советска енциклопедија
- 1 2 G. Audi, O. Bersillon, J. Blachot и A. H. Wapstra (2003). „Евалуацијата на NUBASE на нуклеарните својства и својствата на распаѓање“. Нуклеарна физика А 729 : 3–128. DOI:10.1016/j.nuclphysa.2003.11.001. Бибкод: 2003NuPhA.729....3A.
- Изотопот на телуриум-123 се сметаше за радиоактивен (β--активен со полуживот од 6·1014 години), но по дополнителни мерења беше откриено дека е стабилен во рамките на чувствителноста на експериментот.
- 2,2 квадрилиони години - на долги размери.
- Телуриум. Меѓународна програма за хемиска безбедност (28 јануари 1998 година). Преземено на 12 јануари 2007 година. Архивирано од оригиналот на 4 август 2012 година.
- Рајт, П. Л. (1966). „Компаративен метаболизам на селен и телуриум кај овци и свињи“. АЈП – Наследство 211 (1): 6–10. PMID 5911055.
- (1989) „Телуриум-интоксикација“. Klinische Wochenschrift 67 (22): 1152–5. DOI: 10.1007/BF01726117. PMID 2586020.
- Тејлор, Ендрју (1996). „Биохемија на телуриум“. Истражување на биолошки елементи во трагови 55 (3): 231-239. DOI: 10.1007/BF02785282. PMID 9096851.
Врски
- Телуриум на Webelements
- Телуриум во популарната библиотека за хемиски елементи
| Врски телуриум | |
|---|---|
|
Телуриум хексафлуорид (TeF6) Телуриум диоксид (TeO2) натриум ортотелурат (Na6TeO6) амониум телурат ((NH4)2TeO4) берилиум телурид (BeTe) бизмут(III) телурид (Bi2Te3) телурид (Bi2Te3) Телурид (Bi2Te3) идеја (Na2Te ) калај телурид (SnTe) жива телурид (HgTe) олово телурид (PbTe) цинк телурид (ZnTe) калиум телурит (K2TeO3) натриум телурит (Na2TeO3) телуринска киселина (H2TeO4 2H2TeO4 2H2TelourTe4Hydroph) средно (TeBr4) Калиум тетрахидроортотелурат K2H4TeO6 Телуриум тетрајодид (TeI4) Телуриум тетрафлуорид (TeF4) Телуриум тетрахлорид (TeCl4) Телуриум триоксид (TeO3) Дикалиум трителлурид (K2Te) |
| Периодичен систем на хемиски елементи од Д.И. Менделеев | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
| 1 | Х | Тој | ||||||||||||||||||||||||||||||
| 2 | Ли | Биди | Б | В | Н | О | Ф | Не | ||||||||||||||||||||||||
| 3 | Na | Мг | Ал | Си | П | С | Cl | Ар | ||||||||||||||||||||||||
| 4 | К | Ca | Sc | Ти | В | Кр | Мн | Fe | Ко | Ни | Cu | Zn | Га | Ге | Како | Се | Бр | Кр | ||||||||||||||
| 5 | Rb | Ср | Y | Зр | Nb | Мо | Tc | Ру | Rh | Pd | Аг | Cd | Во | Сн | Сб | Те | Јас | Xe | ||||||||||||||
| 6 | Cs | Ба | Ла | Це | Пр | Нд | ПМ | См | ЕУ | Гд | Тб | Дај | Хо | Ер | Тм | Yb | Лу | Хф | Та | В | Одг | Ос | Ир | Pt | Ов | Хг | Тл | Pb | Би | По | На | Rn |
| 7 | о | Ра | Ак | Т | Па | У | Нп | Пу | Am | Цм | Бк | Сп | Ес | Fm | MD | Бр | Lr | Рф | Дб | Sg | Бх | Хс | Планината | Дс | Rg | Cn | Уут | Fl | Уап | Lv | Uus | Ууо |
| 8 | Ууе | Ubn | Убу | Убб | Убт | Ubq | УБП | Убх | ||||||||||||||||||||||||
телуриум Википедија, телуриум Харков, елемент телуриум, телуриум, телуриум фотографија, телурит, телуриум, телуриум сорокин, телуриум сорокин преземање, телурократија
Телуриум Информации за
Телуриумот е хемиски елемент од групата 16 (според застарената класификација - главната подгрупа од групата VI, халкогени), период 5 во периодниот систем, има атомски број 52; означен со симболот Те (лат. Tellurium), припаѓа на семејството на металоиди.
Содржината во земјината кора е 1·10-6% по маса. Познати се околу 100 минерали на телуриум. Најчести телуриди се бакар, олово, цинк, сребро и злато.
Во многу сулфиди е забележана изоморфна мешавина на телуриум, но изоморфизмот Te - S е помалку изразен отколку во серијата Se - S, а сулфидите содржат ограничена мешавина на телуриум. Меѓу минералите на телуриум, алтаит (PbTe), силванит (AgAuTe4), калаверит (AuTe2), хесит (Ag2Te), кренерит [(Au, Ag)Te], пецит (Ag3AuTe2), мутманит [(Ag, Au)Te] се особено значење , монбрејт (Au2Te3), нагиагит (4S5), тетрадимит (Bi2Te2S). Постојат кислородни соединенија на телуриум, на пример TeO2 - телуриум окер. Домашниот телуриум се јавува и заедно со селенот и сулфурот (јапонскиот телуричен сулфур содржи 0,17% Te и 0,06% Se).
Резерви на наоѓалишта на телуриум во 2012 година, тони *
| Перу | 3,600.0 |
| САД | 3,500.0 |
| Канада | 800.0 |
| Други земји | 16,100.0 |
| Вкупни залихи | 24,000.0 |
* Податоци од Геолошкиот институт на САД
Главниот извор на телуриум е тињата произведена за време на електролитичкото прочистување на блистер (аноден) бакар. За секои 500 тони бакарна руда, обично има една фунта (0,45 кг) телуриум. Телуриумот се произведува првенствено во САД, Кина, Белгија, Русија, Јапонија и Канада.
Анодната кашеста маса содржи селениди и телуриди на благородни метали во композиции со формулата M2Se или M2Te (M = Cu, Ag, Au). На температури од 500 °C, анодната тиња се загрева со натриум карбонат во присуство на воздух. Металните јони се редуцираат на метали додека телуридот се претвора во натриум телурит - M2Te + O2 + Na2CO3 > Na2TeO3 + 2M + CO2.
Телуритите се испуштаат од мешавините со вода и обично се присутни како хидротелурити HTeO3– во раствор. Во текот на овој процес се формираат и селенити, но тие можат да се одвојат со додавање на сулфурна киселина. Хидротелуритите се трансформираат во нерастворлив телуриум диоксид, додека селенитите остануваат во раствор - HTeO3- + ОH– + H2SO4 > TeO2 + SO42- + 2H2O.
Редукцијата до метал се врши или со електролиза или со реакција на телуриум диоксид со сулфур диоксид во сулфурна киселина - TeO2 + 2 SO2 + 2H2O > Te + SO42- + 4H+.
Телуриумот од комерцијална класа обично се продава како прашок и исто така е достапен во форма на плочи, инготи или прачки.
Најголем потрошувач на телуриум е металургијата, каде што се користи во железо, бакар и легури на олово. Додавањето телуриум на нерѓосувачки челик и бакар ги прави овие метали поизводливи. Додавањето на телуриум овозможува да се добие податливо леано железо, кое, кога се топи, ги има предностите на сивото леано железо: течно лиење, својства на лиење и обработливост. Во олово, телуриумот ја подобрува силата и издржливоста и го намалува корозивното дејство на сулфурната киселина.
Полупроводници и електроника. Кадмиум телурид (CdTe) се користи во соларни ќелии. Тестовите на Лабораторијата за обновливи извори на енергија во САД покажаа дека овој материјал дава многу придобивки за работата на новата генерација соларни ќелии. Масовното комерцијално производство на соларни ќелии со употреба на CdTe во последниве години доведе до значително зголемување на побарувачката за телуриум. Ако дел од кадмиумот во CdTe се замени со цинк, се формира односот (Cd,Zn), кој се користи во сензорите за рендгенски зраци во цврста состојба.
Апсолутно исклучителна важност добија легурите на CRT (кадмиум-жива-телуриум), кои имаат фантастични карактеристики за откривање на радијацијата од лансирање на ракети и набљудување на непријателот од вселената преку атмосферски прозорци (облачноста не е важна). MCT е еден од најскапите материјали во модерната електронска индустрија.
Органотелуриди како што се етан телурид, диетил телурид, диизопропил телурид, диетил и метил телурид, алил телурид се користат како основа за органометална фаза на раст епитаксијата за производство на повеќеслојни полупроводнички соединенија.
Голем број системи кои содржат телуриум неодамна открија во нив постоење на три (можеби четири) фази, во кои суперспроводливоста не исчезнува на температура малку над точката на вриење на течниот азот.
Телуриумот како телуриум оксид се користи за создавање слоеви на оптички дискови што може да се препишуваат, вклучително и Compact Discs Rewritable (CD-RW), Rewritable Blu-ray Digital Video Discs и Rewritable (DVD-RW).
Телуриумот се користи во новите мемориски чипови за промена на фазата развиени од Интел. Бизмут телурид (Bi2Te3) и олово телурид се користат во елементи на термоелектрични уреди. Оловниот телурид се користи и во инфрацрвени сензори.
Други употреби. Телуриумот се користи за боење на керамика. Феноменот на силно зголемување на оптичката рефракција по додавање на селениди и телуриди во стаклото се користи во производството на стаклени влакна за телекомуникациите. Мешавините на селен и телуриум се користат со бариум пероксид како оксидирачки агенс во одложениот прав за капачиња за електрично минирање.
Органските телуриди се користат како иницијатори за радикална полимеризација; моно- и дителлуридите богати со електрони имаат антиоксидантна активност. Телуриумот може да се користи наместо сулфур или селен за вулканизација на гума. Гумата произведена на овој начин покажува подобрена термичка отпорност. Телуритите се користат за да се идентификуваат патогените одговорни за дифтерија.
Потрошувачката на телуриум во земјите низ светот се дистрибуира на следниов начин: Кина - 80-100 тони, Русија - 10 тони, САД - 50-60 тони. Вкупно, околу 400 тони телуриум се трошат годишно во целиот свет. Табелата подолу дава приближни податоци за производството на телуриум во светот (податоци од USGS, различни прегледи и написи на пазарот).
Производство на телуриум во светот, тони*
| година | 2008 | 2009 | 2010 | 2011 | 2012 |
| Белгија | 50.0 | 50.0 | 50.0 | 50.0 | 50.0 |
| Канада | 19.0 | 16.0 | 8.0 | 6.0 | 6.0 |
| Кина | 65.0 | 60.0 | 65.0 | 70.0 | 70.0 |
| Јапонија | 46.5 | 49.2 | 47.0 | 40.0 | 35.0 |
| Казахстан | 18.0 | 17.0 | 18.0 | 18.0 | 17.0 |
| Перу | 28.0 | 7.0 | -- | -- | -- |
| Русија | 34.0 | 33.0 | 34.0 | 34.0 | 35.0 |
| САД | 50.0 | 50.0 | 50.0 | 50.0 | 45.0 |
| Други земји | 79.5 | 97.8 | 128.0 | 132.0 | 122.0 |
| Вкупно | 390.0 | 380.0 | 400.0 | 400.0 | 380.0 |
* Податоци од Геолошкиот институт на САД
Телуриумот е редок елемент, а значителната побарувачка со мал обем на производство ја одредува неговата висока цена (околу 200-300 долари за кг, во зависност од чистотата), но и покрај тоа, опсегот на неговите апликации постојано се шири.
Цената на телуриумот во 2000 година беше околу 30 американски долари за килограм. Помеѓу 2004 и 2011 година, цените на телуриумот постојано се зголемуваа, со исклучок на 2009 година. Во текот на овие години, цената на телуриумот беше одредена од значителното зголемување на побарувачката и ограничената понуда. Во 2011 година, цената на телуриумот достигна 350 американски долари за килограм. Сепак, во 2012 година, цените на телуриумот нагло паднаа на приближно 150 американски долари за килограм.
Пазарот на телуриум моментално се соочува со голем број предизвици. Како нуспроизвод на производството на бакар, пазарот на телуриум е многу зависен од трендовите на главниот (бакар) пазар. Намалувањето на производството на бакар заедно со употребата на нови алтернативни технологии за производство на овој метал, на пример, ќе влијае на обемот на понудата на телуриум.
Бидејќи обемот на понудата е доведен во прашање, цената на материјалот вртоглаво расте. Според многу пазарни прогнози, цената на телуриумот повторно ќе порасне во следните 2-3 години. Познато е дека на пазарот има низа различни производи за замена на телуриум, кои веќе почнуваат да се користат во услови на недостиг од снабдување. Сепак, како што забележуваат експертите, ниту една од замените не ги има истите својства како телуриумот. Дополнително, потенцијалното зголемување на побарувачката за телуриум би можело да произлезе од развојот во секторот за соларни тенок филм.
Телуриум - хемиски елементкои припаѓаат на 16-тата група, лоцирани во периодниот систем, атомски број 52 и означени со латинскиот Te - специјална идентификација. Елементот припаѓа на металоидите. Телуриум формула — 4d10 5s2 5p4.
Телуриум - елементима бело-сребрена нијанса и метален сјај и кревка структура. На високи температури, како и многу метали, телуриумот станува еластичен.
Потекло на телуриум
Елементот бил откриен во рудници за злато во планините на Трансилванија. Човештвото знае најмалку сто минерали кои содржат телуриум. Особено, тоа се сребро, злато, бакар и цинк. Постојат различни соединенија на телуриум,на пример, ова се некои видови окер. Во својата чиста форма, во еден депозит можете да најдете селен, телуриуми сулфур, што укажува на можноста елементот да е мајчин.

Сите споменати минерали почесто се наоѓаат во исто наоѓалиште со сребро, олово и бизмут. Во индустриски услови, во најголем дел телуриуме хемиски изолиран од други метали, и покрај фактот што неговите главни минерали се доста чести. Конкретно, во доволни количини е содржан во халкопирит, кој е дел од рудите на никел-бакар и бакар пирит.
Дополнително, може да се најде во молибденит и галена, исто така се наоѓа во бакарни руди, полиметални наоѓалишта и наоѓалишта на олово-цинк. Овие минерали исто така содржат сулфидни и антимон карпи кои содржат кобалт и жива.
Претежно во индустријата, телуриумот се извлекува од тињата, која се формира со електролитичко рафинирање на бакар и олово. При обработката тињата се согорува, а изгорените остатоци содржат одредена содржина на телуриум. За да се изолира потребниот елемент, пепелниците се мијат со хлороводородна киселина.

За да се одвои металот од добиениот киселински раствор, преку него мора да се помине сулфур диоксид. Добиени на овој начин телуриум оксид, се обработува со јаглен за да се добие чист елемент од него. За негово понатамошно прочистување се користи постапка на хлорирање.
Ова произведува тетрахлорид, кој мора да се прочисти со дестилација или исправка. Следно, тоа се хидролизира, и како резултат телуриум хидроксидсе намалува со водород.
Примени на телуриум
Овој метал се користи во производството на многу различни материјали (бакар, олово, железо), па затоа металуршката индустрија е нејзин главен потрошувач. Телуриумот ги прави нерѓосувачкиот челик и бакарот поизводливи. Исто така, додавањето на овој елемент на податливо леано железо му дава позитивни својства на сивото леано железо.
Неговите квалитети на леење и обработливост се подобрени. Тој е во состојба значително да ги подобри физичките својства на оловото, намалувајќи ја негативната корозија од сулфурна киселина за време на нејзината обработка.

Телуриумот е широко користен во полупроводнички уреди и електроника. Особено, се користи за производство на соларни ќелии. Употребата на телуриум отвора широки перспективи во примената на овие напредни технологии. Процентот на производство на ваква опрема значително се зголеми во последните години. Ова доведе до забележително зголемување на прометот на телуриум на светскиот пазар.
Металот се користи, вклучително и во вселенскиот технолошки развој, особено, ова се легури со додавање на телуриум, кои имаат уникатни својства. Тие се користат во технологии за откривање на зрачењето оставено од вселенските летала.
Поради оваа причина, скапата легура е во голема мера барана во воената индустрија, за следење на непријателот во вселената. Во прилог на оваа смеса селен – телуриуме дел од прашокот за одложување во капачињата на детонаторите за експлозивни направи произведени од воени фабрики.

Различни соединенија на телуриум се користат во производството на полупроводнички соединенија со повеќеслојна структура. Многу соединенија кои вклучуваат телуриум покажуваат извонредна суперспроводливост.
Телуриумот работи и во корист на обичните луѓе. Конкретно, металниот оксид се користи во производството на компактни дискови за да се создаде тенок слој што може да се препишува на нив. Таа е присутна и во некои микроциркули, на пример, оние произведени од Интел. Бизмут телурид е вклучен во многу термоелектрични уреди и инфрацрвени сензори.
Овој метал се користи и при сликање керамички производи. Во производството на фиберглас за информативни комуникации (телевизија, Интернет, итн.), Учеството на телуриум во производството на кабли се заснова на позитивното својство на телуридите и селенидите за зголемување на оптичката рефракција кога се додава во стаклото.

Вулканизацијата на гума вклучува и употреба на супстанции блиски до метал - селен или сулфур, кои може да се заменат, ако е можно, со телуриум. Гумата со својот додаток ќе покаже многу подобри квалитети. Телуриумот ја најде својата ниша и во медицината - се користи во дијагнозата на дифтерија.
Цена на телуриум
Во однос на потрошувачката на овој редок метал во светот, Кина е на прво место, Русија е на второ, а САД се на трето. Вкупната потрошувачка е 400 тони метал годишно. Телуриумот обично се продава во форма на прав, прачки или.
Поради малиот обем на производство, поради неговата релативно мала содржина во карпите, цената на телуриумот е доста висока. Приближно, ако не се земат предвид постојаните поскапувања за телуриум, купиНа светскиот пазар може да се продава за 200-300 долари за килограм метал. Цената зависи и од степенот на прочистување на металот од несакани нечистотии.
Но, и покрај непристапноста на овој уникатен елемент, секогаш постои значителна побарувачка за него, со постојани трендови на раст. Секоја година се проширува опсегот на области кои бараат употреба на телуриум и неговите соединенија.
Лесно е да се следи трендот на пораст на цените на телуриумот со споредување на цените на почетокот на 2000 година, кога изнесуваше 30 долари за 1 кг и десет години подоцна, кога достигна 350 долари. И покрај фактот што една година подоцна сè уште падна, постои сериозна тенденција за раст на цените, поради падот на обемот на производството на телуриум.

Факт е дека пазарот на телуриум директно зависи од обемот на производството, бидејќи телуриумот е еден од нуспроизводите при неговото извлекување. Во моментов, пазарот на бакар значително го намали својот промет, а се појавија и нови технологии за негово производство, чии карактеристики значително ќе влијаат на обемот на дополнителен произведен телуриум.
Ова секако ќе се одрази на неговите залихи, а природно и на цените. Според проценките, ново покачување на цената се очекува за неколку години. И покрај фактот дека телуриумот има одредени аналози во индустријата, тие немаат такви вредни својства.
Ваквата состојба на светскиот пазар воопшто не е корисна за многу производители чие производство вклучува телуриум. Конкретно, станува збор за производители на соларни панели, чии производи во последниве години добиваат се поголема популарност.
17,91 kJ/mol
49,8 kJ/mol
шестоаголна
а =4,457 в =5,929
(300 K) 14,3 W/(m K)
Домашниот телуриум се јавува и заедно со селенот и сулфурот (јапонскиот телуричен сулфур содржи 0,17% Te и 0,06% Se).
Видови депозити
Повеќето од споменатите минерали се развиени во нискотемпературни наоѓалишта на злато-сребро, каде што обично се изолираат по најголемиот дел од сулфидите заедно со природното злато, сулфосолите на среброто, олово, а исто така и со минералите на бизмут. И покрај развојот на голем број минерали на телуриум, најголемиот дел од телуриумот извлечен од индустријата е дел од сулфиди на други метали. Особено, телуриумот, во нешто помала мера од селенот, е вклучен во составот на халкопирит во бакар-никелските наслаги од магматично потекло, како и халкопирит развиен во хидротермалните наоѓалишта на бакар пирит. Телуриум се наоѓа и во пирит, халкопирит, молибденит и галена на наоѓалишта на порфирска бакарна руда, полиметални наоѓалишта од типот Алтај, галена на наоѓалишта на олово-цинк поврзани со скарни, сулфид-кобалт, антимон-жива и некои други. Содржината на телуриум во молибденит се движи од 8-53 g/t, во халкопирит 9-31 g/t, во пирит - до 70 g/t.
Потврда
Хемиски својства
Во хемиските соединенија, телуриумот покажува состојби на оксидација -2; +2; +4; +6. Тој е аналог на сулфур и селен, но е хемиски помалку активен од сулфурот. Се раствора во алкали, подложен е на дејството на азотни и сулфурни киселини, но е слабо растворлив во разредена хлороводородна киселина. Металот телуриум почнува да реагира со вода на 100 °C.
Со кислородот формира соединенија TeO, TeO 2, TeO 3. Во форма на прав, се оксидира во воздухот дури и на собна температура, формирајќи TeO 2 оксид. Кога се загрева во воздух, гори, формирајќи TeO 2 - силно соединение кое е помалку испарливо од самиот телуриум. Ова својство се користи за прочистување на телуриумот од оксиди, кои се редуцираат со водород што тече на температура од 500-600 °C. Телуриум диоксидот е слабо растворлив во вода, но растворлив во кисели и алкални раствори.
Во стопена состојба, телуриумот е прилично инертен, па графитот и кварцот се користат како контејнерски материјали при неговото топење.
Телуриумот формира соединение со водород кога се загрева, лесно реагира со халогени и комуницира со сулфур, фосфор и метали. Кога реагира со концентрирана сулфурна киселина, формира сулфит. Формира слаби киселини: хидротелурна киселина (H 2 Te), телурна киселина (H 2 TeO 3) и телуринска киселина (H 6 TeO 6), чии повеќето соли се слабо растворливи во вода.
Изотопи
Апликација
Легури
Телуриумот се користи во производството на оловни легури со зголемена еластичност и цврстина (се користи, на пример, во производството на кабли). Со воведувањето на 0,05% телуриум, загубата на оловото поради растворање под влијание на сулфурна киселина се намалува за 10 пати, а тоа се користи во производството на оловно-киселински батерии. Исто така, важно е оловото легирано со телуриум да не омекне кога се обработува со пластична деформација, а тоа овозможува да се користи технологијата за производство на батериски тековни колектори со методот на ладно сечење и значително да се зголеми работниот век и специфичните карактеристики на батеријата. .
Составот на легура CZT (кадмиум цинк телурид, CdZnTe) се користи во производството на детектори за Х-зраци и гама зрачење кои работат на собна температура.
Термоелектрични материјали
Неговата улога е исто така голема во производството на полупроводнички материјали и особено телуриди на олово, бизмут, антимон и цезиум. Во наредните години, производството на лантанидни телуриди, нивните легури и легури со метални селениди ќе станат многу важни за производство на термоелектрични генератори со многу висока (до 72-78%) ефикасност, што ќе овозможи нивна употреба во енергетскиот сектор и во автомобилската индустрија.
На пример, многу висок термички емф неодамна беше откриен во манган телурид (500 μV/K) и во неговата комбинација со бизмут, антимон и селениди на лантанид, што овозможува не само да се постигне многу висока ефикасност во термогенераторите, туку и да се имплементирајте го во една фаза полупроводнички фрижидер ладење до криогени (температурно ниво на течен азот) температури, па дури и пониски. Најдобриот материјал базиран на телуриум за производство на полупроводнички фрижидери во последниве години е легура на телуриум, бизмут и цезиум, што овозможи да се добие рекордно ладење до -237 °C. Во исто време, легурата на телуриум-селен (70% селен), која има коефициент на термо-EMF од околу 1200 μV/K, ветува како термоелектричен материјал.
Полупроводници со тесен јаз
Апсолутно исклучителна важност добија и легурите на CRT (кадмиум - телуриум), кои имаат фантастични карактеристики за откривање на радијацијата од лансирање ракети и набљудување на непријателот од вселената преку атмосферски прозорци (облачноста не е важна). MCT е еден од најскапите материјали во модерната електронска индустрија.
Високотемпературна суперспроводливост
Голем број системи кои содржат телуриум неодамна открија во нив постоење на три (можеби четири) фази, во кои суперспроводливоста не исчезнува на температура малку над точката на вриење на течниот азот.
Производство на гума
Посебна област на примена на телуриум е неговата употреба во процесот на вулканизација на гума.
Производство на чалкогенидни чаши
Телуриумот се користи за топење на специјални степени на стакло (каде што се користи во форма на диоксид); специјални очила допирани со метали од ретки земји се користат како активни тела во оптичките квантни генератори.
Покрај тоа, некои очила на база на телуриум се полупроводници, својство што се користи во електрониката.
Специјални оценки на телуриумско стакло (предностите на таквото стакло се проѕирност, фузибилност и електрична спроводливост) се користат во изградбата на специјална хемиска опрема (реактори).
Телуриумот наоѓа ограничена употреба во производството на светилки со неговите пареи - тие имаат спектар многу близок до оној на сонцето.
CD-RW
Легурата на телуриум се користи во компактни дискови што можат да се препишуваат (особено, Mitsubishi Chemical Corporation брендот „Verbatim“) за да се создаде деформабилен рефлективен слој.
Биолошка улога
Физиолошко дејство
Телуриумот и неговите испарливи соединенија се токсични. Ако влезе во телото, предизвикува гадење, бронхитис и пневмонија. MPC во воздухот варира за различни соединенија 0,007-0,01 mg/m³, во вода 0,001-0,01 mg/l. Канцерогеноста на телуриумот не е потврдена.
Во случај на труење, телуриумот се излачува од телото во форма на испарливи органотелуриумски соединенија со непријатен мирис - алкил телуриди, главно диметил телурид (CH 3) 2 Te. Нивниот мирис наликува на мирисот на лук, затоа, кога дури и мали количини на телуриум влегуваат во телото, воздухот што го издишува лицето го добива овој мирис, што е важен симптом на труење со телуриум.
Напишете преглед за написот „Телуриум“
Белешки
- Мајкл Е. Визер, Норман Холден, Тајлер Б. Гленда О'Конор, Томас Валчик, Шиге Јонеда, Ксијанг-Кун Жу.(англиски) // Чиста и применета хемија. - 2013. - Ред. 85, бр. 5 . - P. 1047-1078. - DOI: 10.1351/PAC-REP-13-03-02.
- (Англиски) . WebElements. Преземено на 5 август 2010 година.
- Ледикот, Г. В. (1961),
, Серија за нуклеарни науки, Поткомитет за радиохемија, Национална академија на науките-Национален совет за истражување, стр. 5 ,
- Редакциски тим: Зефиров Н.С. (главен уредник).Хемиска енциклопедија: во 5 тома - Москва: Советска енциклопедија, 1995. - Т. 4. - стр. 514. - 639 стр. - 20.000 примероци. - ISBN 5-85270-039-8.
- Глинка Н.Л.Општа хемија. - М.: „Хемија“, 1977 година, ревидирана. - P. 395. - 720 стр.
- Телуриум- статија од Големата советска енциклопедија
- G. Audi, O. Bersillon, J. Blachot и A. H. Wapstra (2003). "". Нуклеарна физика А 729 : 3–128. DOI:10.1016/j.nuclphysa.2003.11.001. Бибкод:.
- Изотопот на телуриум-123 се сметаше за радиоактивен (β--активен со полуживот од 6·10 14 години), но по дополнителни мерења беше откриено дека е стабилен во рамките на чувствителноста на експериментот.
- 2,2 квадрилиони години - на долги размери.
- . Меѓународна програма за хемиска безбедност (28 јануари 1998 година). Преземено на 12 јануари 2007 година.
- Рајт, П. Л. (1966). "". АЈП – Наследство 211 (1): 6–10. PMID 5911055.
- (1989) „Телуриум-интоксикација“. Klinische Wochenschrift 67 (22): 1152–5. DOI: 10.1007/BF01726117. PMID 2586020.
- Тејлор, Ендрју (1996). „Биохемија на телуриум“. Истражување на биолошки елементи во трагови 55 (3): 231-239. DOI: 10.1007/BF02785282. PMID 9096851.
Врски
| Периодичен систем на хемиски елементи од Д.И. Менделеев | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Те | ||||||||||||||||||||||||||||||||
| Земјени алкални метали | ||||||||||||||||||||||||||||||||
Извадок што го карактеризира Телуриум
Вечерта, Наполеон, меѓу две нарачки - едната за испорака на подготвените фалсификувани руски банкноти за увоз во Русија што е можно поскоро, а другата за пукање во Саксон, во чие пресретнато писмо се пронајдени информации за нарачки за француската армија - направил. трета наредба - за вклучувањето на полскиот полковник, кој непотребно се фрли во реката, во почесната група (Legion d'honneur), чиј шеф беше Наполеон.Qnos vult perdere – dementat. [Кого сака да го уништи, ќе го лиши од памет (лат.)]
Во меѓувреме, рускиот император веќе живеел во Вилна повеќе од еден месец, правејќи прегледи и маневри. Ништо не беше подготвено за војната што сите ја очекуваа и за која царот дојде од Санкт Петербург да се подготви. Немаше генерален план за акција. Двоумењето околу тоа кој план, од сите што беа предложени, да се донесе, само уште повеќе се засили по едномесечниот престој на царот во главниот стан. Секоја од трите војски имала посебен врховен командант, но немало заеднички командант над сите војски, а царот не ја презел оваа титула.
Колку подолго живееше царот во Вилна, толку помалку се подготвуваа за војна, уморни од тоа да ја чекаат. Сите аспирации на луѓето што го опкружуваат суверенот се чинеше дека беа насочени само кон тоа да го натераат суверенот, а притоа да има пријатно време, да заборави на претстојната војна.
По многу балови и празници меѓу полските магнати, меѓу дворјаните и самиот суверен, во јуни еден од полските генерални аѓутанти на суверенот дојде до идеја да му даде вечера и бал на суверенот во име на неговиот генерал. аѓутанти. Оваа идеја беше радосно прифатена од сите. Императорот се согласи. Адјутантите на генералот собирале пари со претплата. Лицето кое можеше да му биде најпријатно на суверенот беше покането да биде водителка на топката. Грофот Бенигсен, земјопоседник на провинцијата Вилна, ја понудил својата селска куќа за овој празник, а на 13 јуни била закажана вечера, бал, возење со брод и огномет во Закрет, селската куќа на грофот Бенигсен.
На самиот ден кога Наполеон дал наредба да го преминат Неман и неговите напредни трупи, туркајќи ги назад Козаците, ја преминале руската граница, Александар ја поминал вечерта на дачата на Бенигсен - на балот што го дале аѓутантите на генералот.
Тоа беше весел, брилијантен празник; стручњаците во бизнисот рекоа дека ретко толку убавици се собрале на едно место. Грофицата Безухова, заедно со другите руски дами кои дојдоа по суверенот од Санкт Петербург во Вилна, беше на овој бал, помрачувајќи ги софистицираните полски дами со својата тешка, таканаречена руска убавина. Таа беше забележана, а суверенот ја почести со оро.
Борис Друбецкој, en garcon (ерген), како што рече, откако ја остави сопругата во Москва, беше исто така на овој бал и, иако не беше генерал-адјутант, беше учесник за голема сума во претплатата за топката. Борис сега беше богат човек, многу напреден во чест, повеќе не бараше покровителство, туку стоеше на рамномерна основа со највисоките врсници.
Во дванаесет часот навечер сè уште танцуваа. Хелен, која немала достоен господин, самата му ја понудила мазурка на Борис. Седнаа во третиот пар. Борис, ладнокрвно гледајќи во сјајните голи рамења на Хелен кои штрчеа од нејзината темна газа и златен фустан, зборуваше за старите познаници и во исто време, незабележан од себе и од другите, ниту една секунда не престана да го гледа суверенот, кој беше во истата просторија. Царот не танцуваше; застана на прагот и прво го запре едното или другото со оние нежни зборови што сам знаеше да ги каже.
На почетокот на мазурката, Борис видел дека генерал-адјутантот Балашев, еден од најблиските луѓе на суверенот, му пришол и недворно застанал блиску до суверенот, кој разговарал со една полска дама. Откако разговараше со госпоѓата, суверенот погледна прашално и, очигледно сфаќајќи дека Балашев постапил така само затоа што имало важни причини, благо кимна со главата на госпоѓата и се сврте кон Балашев. Штом Балашев почна да зборува, на лицето на суверенот беше изразено изненадување. Го фати Балашев за рака и тргна со него низ ходникот, несвесно расчистувајќи ги трите фази од широкиот пат од двете страни од оние што стоеја настрана пред него. Борис го забележа возбудениот лик на Аракчеев додека суверенот шеташе со Балашев. Аракчеев, гледајќи од под веѓите во суверенот и грчејќи го црвениот нос, се оттргна од толпата, како да очекуваше дека суверенот ќе се сврти кон него. (Борис сфатил дека Аракчеев е љубоморен на Балашев и бил незадоволен што некои очигледно важни вести не му биле пренесени на суверенот преку него.)
Но, суверенот и Балашев поминаа, без да го забележат Аракчеев, низ излезната врата во осветлената градина. Аракчеев, држејќи го мечот и налутено гледајќи наоколу, одеше зад нив дваесетина чекори.
Додека Борис продолжуваше да прави фигури од мазурка, постојано го мачеше помислата какви вести донел Балашев и како да дознае за тоа пред другите.
Во фигурата каде што требаше да избере дами, шепотејќи ѝ на Хелен дека сака да ја земе грофицата Потоцкаја, која изгледаше како да излезе на балконот, тој, лизгајќи ги нозете по паркетот, истрча од излезната врата во градината и , забележувајќи го суверенот како влегува на терасата со Балашев, застана. Царот и Балашев се упатија кон вратата. Борис, во брзање, како да нема време да се оддалечи, со почит се притисна на надвратницата и ја наведна главата.
Со емоција на лично навреден човек, царот ги заврши следните зборови:
- Влезете во Русија без објавување војна. „Ќе склучам мир само кога нема да остане ниту еден вооружен непријател на мојата земја“, рече тој. На Борис му се чинеше дека суверенот е задоволен да ги искаже овие зборови: тој беше задоволен од формата на изразување на своите мисли, но беше незадоволен од фактот што Борис ги слушна.
- За никој ништо да не знае! – додаде суверенот намуртено. Борис сфати дека тоа се однесува на него и, затворајќи ги очите, малку ја наведна главата. Императорот повторно влезе во салата и остана на балот околу половина час.
Борис прв ја дознал веста за преминувањето на Неман од страна на француските војници и благодарение на тоа имал можност на некои важни личности да им покаже дека знае многу работи скриени од другите и преку тоа имал можност да се издигне повисоко во мислењето на овие лица.
Посебно неочекувана беше неочекуваната вест за Французинот кој го премина Неман по еден месец неостварено исчекување и тоа на бал! Императорот, во првата минута од приемот на веста, под влијание на огорченост и навреда, го нашол она што подоцна станало познато, изрека која и самиот му се допаднала и целосно ги изразил своите чувства. Враќајќи се дома од балот, суверенот во два часот по полноќ испратил по секретарот Шишков и наредил да се напише наредба до војниците и репис до фелдмаршалот принц Салтиков, во кој тој секако барал да се стават зборовите дека тој нема да склучи мир додека барем еден вооружен Французин не остане на руска територија.
Следниот ден следното писмо му било напишано на Наполеон.
„Господине слободно. J"ai appris hier que malgre la loyaute avec laquelle j"ai maintenu mes ангажмани envers Votre Majeste, ses troupes ont franchis les frontieres de la Russie, et je recois a l"instant de Petersbourg une note par laquelle le comte de Lauris cette aggression, annonce que Votre Majeste s"est consideree comme en etat de guerre avec moi des le moment ou le prince Kourakine a fait la demande de ses пасоши. Les motifs sur lesquels le duc de Bassano fondait son refus de les lui delivrer, n „auraient jamais pu me faire supposer que cette demarche servirait jamais de pretexte a l“ агресија. En effet cet ambassadeur n"y a jamais ete autorise comme il l"a declare lui meme, et aussitot que j"en fus informe, je lui ai fait connaitre combien je le desapprouvais en lui donnant l"ordre de rester. Si Votre Majeste n"est pas intentionnee de verser le sang de nos peuples pour un malentendu de ce genre et qu"elle consente a retirer ses troupes du territoire russe, je regarderai ce qui s"est passe comme non avenu, et un accommodement nous sera е можно. Dans le cas contraire, Votre Majeste, je me verrai force de repousser une attaque que rien n"a provoquee de ma part. Il depend encore de Votre Majeste d"eviter a l"humanite les calamites d"une nouvelle guerre.
Je suis, итн.
(ознака) Александар“.
[„Господару брате! Вчера ми стана јасно дека, и покрај директноста со која ги почитував моите обврски кон Вашето Царско Височество, вашите војници ги преминаа руските граници и дури сега добив белешка од Санкт Петербург, со која грофот Лауристон ме известува за оваа инвазија , дека Вашето Височество сметате дека сте во непријателски односи со мене од времето кога принцот Куракин ги побара своите пасоши. Причините на кои војводата од Басано го засновал своето одбивање да ги издаде овие пасоши никогаш не можеле да ме наведат да претпоставам дека чинот на мојот амбасадор послужил како причина за нападот. А всушност тој немаше заповед од мене да го направи тоа, како што самиот најави; и штом дознав за ова, веднаш му изразив незадоволство на принцот Куракин, наредувајќи му да ги извршува должностите што му се доверени како и досега. Ако Вашето Височество не е склоно да ја пролее крвта на нашите поданици поради таквото недоразбирање и ако се согласите да ги повлечете вашите трупи од руските поседи, тогаш ќе игнорирам сè што се случи и ќе биде возможен договор меѓу нас. Во спротивно, ќе бидам принуден да одбијам напад што не беше испровоциран од ништо од моја страна. Ваше Височество, сè уште имате можност да го спасите човештвото од злото на нова војна.
(потпишан) Александар“. ]
На 13 јуни, во два часот по полноќ, суверенот, повикувајќи го Балашев кај себе и читајќи му го неговото писмо до Наполеон, му наредил да го земе ова писмо и лично да му го предаде на францускиот цар. Испраќајќи го Балашев, суверенот повторно му ги повтори зборовите дека нема да склучи мир додека барем еден вооружен непријател не остане на руска почва и нареди овие зборови да му се пренесат на Наполеон без да успее. Царот не ги напишал овие зборови во писмото, бидејќи со својата тактичност чувствувал дека овие зборови не се згодни да се пренесат во моментот кога се правел последниот обид за помирување; но секако му наредил на Балашев лично да му ги предаде на Наполеон.
Откако замина ноќта на 13-ти кон 14-ти јуни, Балашев, придружуван од трубач и двајца Козаци, пристигна во зори во селото Риконти, кај француските пунктови од оваа страна на Неман. Тој беше запрен од стражарите на француската коњаница.
Француски подофицер на хусар, во темноцрвена униформа и бушава капа, му се развикал на Балашев додека се приближувал, наредувајќи му да застане. Балашев не застанал веднаш, туку продолжил да чекори по патот.
Подофицерот, намуртен и мрморејќи некаква клетва, напредуваше со градите на коњот кон Балашев, ја зеде сабјата и грубо му викна на рускиот генерал, прашувајќи го: дали е глув, дека не слуша што е што му се вели. Балашев се легитимирал. Подофицерот го испратил војникот кај офицерот.
Не обрнувајќи внимание на Балашев, подофицерот почна да разговара со своите другари за неговата полковна работа и не го погледна рускиот генерал.
Беше невообичаено чудно за Балашев, откако беше близок до највисоката моќ и моќ, по разговорот пред три часа со суверенот и генерално навикнат на почести од неговата служба, да го види овде, на руска почва, овој непријателски и најважно. непочитуван однос кон себе од брутална сила.
Сонцето само што почна да изгрева од зад облаците; воздухот беше свеж и росен. По пат, стадото било избркано од селото. Во полињата, една по една, како меурчиња во вода, чугите оживуваат со шут.
Балашев погледна околу себе чекајќи да дојде офицер од селото. Руските Козаци, трубачот и француските хусари немо се гледаа од време на време.
Француски хусарски полковник, очигледно штотуку станал од креветот, излегол од селото на убав, добро нахранет сив коњ, придружуван од двајца хусари. Офицерот, војниците и нивните коњи носеа чувство на задоволство и чувство на чувство.
Ова беше прв пат од кампањата, кога војниците сè уште беа во добра состојба, речиси еднаква на инспекцијата, мирната активност, само со допир на паметна воинственост во облеката и со морална конотација на таа забава и потфат што секогаш ги придружува почеток на кампањите.
Францускиот полковник имаше потешкотии да го задржи зевањето, но беше љубезен и, очигледно, го сфати целосното значење на Балашев. Тој го одведе покрај своите војници покрај синџирот и рече дека неговата желба да биде претставен на царот веројатно веднаш ќе се исполни, бидејќи царскиот стан, колку што знаел, не бил далеку.
Тие се возеа низ селото Риконти, покрај француските хусари, стигнувајќи до столбовите, стражарите и војниците кои го поздравуваа својот полковник и љубопитно ја испитуваа руската униформа, и избркаа на другата страна од селото. Според полковникот, на два километри оддалечен бил началникот на дивизијата, кој би го примил Балашев и ќе го испратил до целта.
Сонцето веќе изгреа и весело светеше на светлото зеленило.
Тие штотуку излегоа од таверната на планината, кога од под планината се појави група коњаници да ги пречека, пред кои, на црн коњ со запрег што сјае на сонце, јаваше висок човек со капа со пердуви и црни коса свиткана до рамениците, во црвена наметка и со долги нозе испакнати напред, како француското возење. Овој човек галопираше кон Балашев, неговите пердуви, камења и златна плетенка светкаа и трепереа на светлото јунско сонце.
Балашев беше веќе два коња подалеку од коњаникот што галопира кон него со свечено театарско лице во нараквици, пердуви, ѓердани и злато, кога Јулнер, францускиот полковник, со почит шепна: „Le roi de Naples“. [Кралот на Неапол.] Навистина, тоа беше Мурат, сега наречен крал на Неапол. Иако беше сосема неразбирливо зошто тој е наполитанскиот крал, тој беше наречен така, а и самиот беше убеден во тоа и затоа имаше посвечен и поважен изглед од порано. Тој беше толку сигурен дека навистина е наполитанскиот крал, што во пресрет на неговото заминување од Неапол, додека се шеташе со сопругата низ улиците на Неапол, неколку Италијанци му викнаа: „Вива ил ре!“ [Да живее кралот! (италијански) ] се сврте кон сопругата со тажна насмевка и рече: „Les malheureux, ils ne savent pas que je les quitte demain! [Несреќни луѓе, не знаат дека утре ќе ги оставам!]
Но, и покрај тоа што тој цврсто веруваше дека тој е наполитанскиот крал и дека жали за тагата на неговите поданици што ги остави, неодамна, откако му беше наредено повторно да влезе во служба, а особено по неговата средба со Наполеон во Данциг, кога августовскиот девер му рекол: „Je vous ai fait Roi pour regner a maniere, mais pas a la votre“, [те направив цар за да не царуваш на свој, туку на мој начин.] - почна весело за некоја нему позната задача и, како нахранет, но не и дебел, коњ способен за служба, насетувајќи се во запрега, почна да игра во окните и, откако се испушти што е можно пошарено и поскапо, весела и задоволна, галопирана, не знаејќи каде и зошто, покрај патиштата Полска.