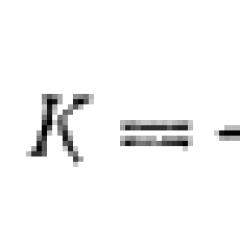Электролитическая диссоциация воды. Константа диссоциации воды. Ионное произведение воды. Что такое диссоциация воды? Электронные облака орбиталей с разными значениями l имеют разную конфигурацию, а с одинаковыми l похожую
Чистая вода, хоть и плохо (по сравнению с растворами электролитов), но может проводить электрический ток. Это вызвано способностью молекулы воды распадаться (диссоциировать) на два иона которые и являются проводниками электрического тока в чистой воде (ниже под диссоциацией подразумевается электролитическая диссоциация - распад на ионы):
Водородный показатель (рН) величина, характеризующая активность или концентрацию ионов водорода в растворах. Водородный показатель обозначается рН. Водородный показатель численно равен отрицательному десятичному логарифму активности или концентрации ионов водорода, выраженной в молях на литр: pH=-lg[ H+ ] Если [ H+ ]>10-7моль/л, [ OH-]<10-7моль/л -среда кислая; рН<7.Если [ H+ ]<10-7 моль/л, [ OH-]>10-7моль/л -среда щелочная; рН>7. Гидролиз солей - это химическое взаимодействие ионов соли с ионами воды, приводящее к образованию слабого электролита. 1). Гидролиз не возможенСоль, образованная сильным основанием и сильной кислотой (KBr , NaCl , NaNO3 ), гидролизу подвергаться не будет, так как в этом случае слабый электролит не образуется.рН таких растворов = 7. Реакция среды остается нейтральной. 2). Гидролиз по катиону (в реакцию с водой вступает только катион). В соли, образованной слабым основанием и сильной кислотой
(FeCl2 , NH4Cl , Al2(SO4)3 ,MgSO4 )
гидролизу подвергается катион:
FeCl2 + HOH <=>Fe(OH)Cl + HCl Fe2+ + 2Cl- + H+ + OH- <=> FeOH+ + 2Cl- + Н+
В результате гидролиза образуется слабый электролит, ион H+ и другие ионы. рН раствора < 7 (раствор приобретает кислую реакцию). 3). Гидролиз по аниону (в реакцию с водой вступает только анион). Соль, образованная сильным основанием и слабой кислотой
(КClO , K2SiO3 , Na2CO3 ,CH3COONa )
подвергается гидролизу по аниону, в результате чего образуется слабый электролит, гидроксид-ион ОН- и другие ионы.
K2SiO3 + НОH <=>KHSiO3 + KОН 2K+ +SiO32- + Н+ + ОH-<=> НSiO3- + 2K+ + ОН-
рН таких растворов > 7 (раствор приобретает щелочную реакцию).4). Совместный гидролиз (в реакцию с водой вступает и катион и анион). Соль, образованная слабым основанием и слабой кислотой
(СН 3СООNН 4 , (NН 4)2СО 3 , Al2S3 ),
гидролизуется и по катиону, и по аниону. В результате образуются малодиссоциирующие основание и кислота. рН растворов таких солей зависит от относительной силы кислоты и основания. Мерой силы кислоты и основания является константа диссоциации соответствующего реактива. Реакция среды этих растворов может быть нейтральной, слабокислой или слабощелочной:
Al2S3 + 6H2O =>2Al(OH)3v+ 3H2S^
Гидролиз - процесс обратимый. Гидролиз протекает необратимо, если в результате реакции образуется нерастворимое основание и (или) летучая кислота
Очень плохо проводит электрический ток, но все же обладает некоторой измеримой электропроводностью, которая объясняется небольшой диссоциацией воды на водородныеи гидроксильные ионы:
H2O ⇄ H + OH’
По величине электропроводности чистой воды можно вычислить концентрацию ионов водорода и ионов гидроксила в воде. Она оказывается равной 10 -7 г -ион /л.
Применяя к диссоциации воды закон действия масс, можно написать:
Перепишем это уравнение следующим образом:
[ОН’] = [Н 2 O] K
Так как воды очень мала, концентрацию недиссоциированных молекул Н 2 О не только в воде, но и во всяком разбавленном водном растворе можно считать величиной постоянной. Поэтому, заменив [Н 2 O] K новой константой КН 2 О, будем иметь:
[Н] [ОН’] = К H2O
Полученное уравнение показывает, что для воды и разбавленных водных растворов при неизменной температуре произведение концентраций водородных и гидроксильных ионов есть величина постоянная. Эта постоянная величина называется ионным произведением воды. Численное значение ее нетрудно получить, подставив в последнее уравнение концентрации водородных и гидроксильных ионов
К H2O = 10 -7 10 -7 = 10 -14
Растворы, в которых концентрация водородных и концентрация гидроксильных ионов одинаковы и равны каждая 10 —7 г-ион/л, называются нейтральными растворами. В кислых растворах больше концентрация водородных ионов, в щелочных - концентрация гидроксильных ионов. Но какова бы ни была реакция раствора, произведение концентраций H и ОН’-ионов должно оставаться постоянным.
Если, например, к чистой воде прибавить столько кислоты, чтобы концентрация водородных ионов повысилась до 10 -3 , концентрация гидроксильных ионов должна будет понизиться так, чтобы произведение [Н ] [ОН’] осталось равным 10 -14 . Следовательно, в этом растворе концентрация гидроксильных ионов будет:
10 -14: 10 -3 = 10 -11
Наоборот, если прибавить к воде щелочи и тем повысить концентрацию гидроксильных ионов, например, до 10 -5 , концентрация водородных ионов станет равна:
10 -14: 10 -5 = 10 -9
Вы читаете, статья на тему Диссоциация воды
Химически чистая вода обладает хотя и ничтожной, но измеримой электропроводностью, так как вода в незначительной степени диссоциирует на ионы. Так при комнатной температуре лишь примерно одна из 10 8 молекул воды находится в диссоциированной форме. Процесс электролитической диссоциации воды возможен благодаря достаточно высокой полярности связей О-Н и наличию между молекулами воды системы водородных связей. Уравнение диссоциации воды записывается так:
2H 2 O ↔ H 3 O + + OH - ,
где H 3 O + - катион гидроксония водорода.
Уравнение диссоциации воды можно записать в более простой форме:
H 2 O ↔ H + + OH - .
Присутствие в воде ионов водорода и гидроксида придают ей специфические свойства амфолита, т.е. способность выполнять функции слабой кислоты и слабого основания. Константа диссоциации воды при температуре 22 0 С:
где и – равновесные концентрации в г-ион/л соответственно катионов водорода и гидроксо-анионов, а – равновесная концентрация воды в моль/л. Учитывая, что степень диссоциации воды чрезвычайно мала, равновесную концентрацию недиссоциированных молекул воды вполне можно приравнять к общему количеству воды, заключающемуся в 1 л ее:
Теперь выражение (1) можно записать в следующем виде:
отсюда = (1,8 10 -16) 55,56 = 10 -14 г-ион 2 /л 2 .
Произведение концентраций ионов водорода и гидроксо-ионов является константой не только для воды, но и для водных растворов солей, кислот и щелочей. Эта величина называется ионным произведением воды или константой воды. Следовательно: К Н2О = = 10 -14 г-ион 2 /л 2 .
Для нейтральных сред = = 10 -7 г-ион/л. В кислых средах > , а в щелочных < . При этом в любых средах произведение концентраций ионов водорода и гидроксо-ионов при данной температуре остается постоянным и равным 10 -14 г-ион 2 /л 2 . Таким образом, пользуясь ионным произведением воды, любую реакцию среды (нейтральную, кислую или щелочную) можно количественно выразить при помощи концентрации водородных ионов.
1.2. Водородный показатель – рН
Для количественной характеристики реакции среды обычно приводят не концентрации водородных ионов, а применяют некоторый условный показатель, обозначаемый через рН и называемый водородным показателем. Он представляет собой отрицательный десятичный логарифм концентрации катионов водорода рН = - lg .
Для нейтральной среды рН = -lg 10 -7 = 7;
для кислотной - рН < 7;
для щелочной - рН >7.
Аналогично вводится понятие гидроксильного показателя рОН = - lg [ОH - ].
рН + рОН = 14.
Определение рН имеет колоссальное значение в технике и, в частности, в строительном деле. Обычно величину рН измеряют при помощи индикаторов - веществ, способных менять свою окраску в зависимости от концентрации ионов водорода. Индикаторами являются слабые кислоты и основания, молекулы и ионы которых окрашены в разный цвет (табл. 1).
Таблица 1
Однако индикаторы дают не точное определение значения рН, поэтому современные измерения рН производятся при использовании электрохимических методов, точность которых составляет ±0,01 единицы рН.
Учебное пособие предназначено для студентов нехимических специальностей высших учебных заведений. Оно может служить пособием для лиц, самостоятельно изучающих основы химии, и для учащихся химических техникумов и старших классов средней школы.
Легендарный учебник, переведенный на многие языки стран Европы, Азии, Африки и выпущенный общим тиражом свыше 5 миллионов экземпляров.
При изготовлении файла, использован сайт http://alnam.ru/book_chem.php
Книга:
| <<< Назад
|
Вперед >>>
|
Чистая вода очень плохо проводит электрический ток, но все же обладает измеримой электрической проводимостью, которая объясняется небольшой диссоциацией воды на ионы водорода и гидроксид-ионы:
По величине электрической проводимости чистой воды можно вычислить концентрацию ионов водорода и гидроксид-ионов в воде. При 25°C она равна 10 -7 моль/л.
Напишем выражение для константы диссоциации воды:
![]()
Перепишем это уравнение следующим образом:
Поскольку степень диссоциации воды очень мала, то концентрация недиссоциированных молекул H 2 O в воде практически равна общей концентрации воды, т. е. 55,55 моль/л (1 л. содержит 1000 г. воды, т. е. 1000:18.02=55.55 моль). В разбавленных водных растворах концентрацию воды можно считать такой же. Поэтому, заменив в последнем уравнении произведение новой константой K H 2 O будем иметь:
![]()
Полученное уравнение показывает, что для воды и разбавленных водных растворов при неизменной температуре произведение концентрата ионов водорода и гидроксид-ионов есть величина постоянная, Эта постоянная величина называется ионным произведением воды. Численное значение ее нетрудно получить, подставив в последнее уравнение концентрации ионов водорода и гидроксид-ионов. В чистой воде при 25°C ==1·10 -7 моль/л. Поэтому для указанной температуры:
Растворы, в которых концентрации ионов водорода и гидроксид-ионов одинаковы, называются нейтральными растворами. При 25°C, как уже сказано, в нейтральных растворах концентрация как ионов водорода, так и гидроксид-ионов равна 10 -7 моль/л. В кислых растворах больше концентрация ионов водорода, в щелочных - концентрация гидроксид-ионов. Но какова бы ни была реакция раствора, произведение концентраций ионов водорода и гидроксид-ионов остается постоянным.
Если, например, к чистой воде добавить столько кислоты, чтобы концентрация ионов водорода повысилась до 10 -3 моль/л, то концентрация гидроксид-ионов понизится так, что произведение останется равным 10 -14 . Следовательно, в этом растворе концентрация гидроксид-ионов будет:
10 -14 /10 -3 =10 -11 моль/л
Наоборот, если добавить к воде щелочи и тем повысить концентрацию гидроксид-ионов, например, до 10 -5 моль/л, то концентрация ионов водорода составит:
10 -14 /10 -5 =10 -9 моль/л
Эти примеры показывают, что если концентрация ионов водорода в водном растворе известна, то тем самым определена и концентрация гидроксид-ионов. Поэтому как степень кислотности, так и степень щелочности раствора можно количественно охарактеризовать концентрацией ионов водорода:

Кислотность или щелочность раствора можно выразить другим, более удобным способом: вместо концентрации ионов водорода указывают ее десятичный логарифм, взятый с обратным знаком. Последняя величина называется водородным показателем и обозначается через pH:
Например, если =10 -5 моль/л, то pH=5 ; если =10 -9 моль/л, то pH=9 и т. д. Отсюда ясно, что в нейтральном растворе (=10 -7 моль/л) pH=7. В кислых растворах pH<7 и тем меньше, чем кислее раствор. Наоборот, в щелочных растворах pH>7 и тем больше, чем больше щелочность раствора.
Для измерения pH существуют различные методы. Приближенно реакцию раствора можно определить с помощью специальных реактивов, называемых индикаторами, окраска которых меняется в зависимости от концентрации ионов водорода. Наиболее распространенные индикаторы - метиловый оранжевый, метиловый красный, фенолфталеин. В табл. 17 дана характеристика некоторых индикаторов.
Для многих процессов значение pH играет важную роль. Так, pH крови человека и животных имеет строго постоянное значение. Растения могут нормально произрастать лишь при значениях pH почвенного раствора, лежащих в определенном интервале, характерном для данного вида растения. Свойства природных вод, в частности их коррозионная активность, сильно зависят от их pH.
Таблица 17. Важнейшие индикаторы

| <<< Назад
|
Вперед >>>
|
Частным случаем диссоциации (процесса распада более крупных частиц вещества — молекул ионов или радикалов — на частицы меньшего размера) является электролитическая диссоциация, при которой нейтральные молекулы вещества, называемого электролитом, в растворе (в результате воздействия молекул полярного растворителя) распадаются на заряженные частицы: катионы и анионы. Этим объясняется способность проводить ток.
Принято делить все электролиты на две группы: слабые и сильные. Вода относится к слабым электролитам, диссоциация воды характеризуется небольшим количеством диссоциированных молекул, так как они достаточно стойкие и практически не распадаются на ионы. Чистая (без примесей) вода слабо проводит электрический ток. Это обусловлено химической природой самой молекулы, когда положительно поляризованные атомы водорода внедрены в электронную оболочку сравнительно небольшого атома кислорода, который поляризован отрицательно.
Сила и слабость электролитов характеризуется (обозначается α, часто эта величина выражается в % от 0 до 100 или в долях единицы от 0 до 1) — способностью распадаться на ионы, то есть отношением количества распавшихся частиц к числу частиц до распада. Такие вещества, как кислоты, соли и основания под действием полярных распадаются на ионы полностью. Диссоциация воды сопровождается распадом молекул Н2О на протон Н+ и гидроксильную группу ОН-. Если представить уравнение диссоциации электролита в виде: М=К++А- , тогда диссоциация воды может быть выражена уравнением: Н2О↔Н++ОН-, а уравнение, с помощью которого рассчитывается степень диссоциации воды, можно представить в двух видах (через концентрацию образовавшихся протонов или концентрацию образовавшихся гидроксильных групп): α=[Н+]/[Н2О] или α=[ОН-]/[Н2О]. Так как на величину α влияет не только химическая природа вещества, но и концентрация раствора или его температура, то принято говорить о кажущейся (мнимой) степени диссоциации.
Склонность молекул слабых электролитов, включая воду, распадаться на ионы в большей степени характеризуется константой диссоциации (частный случай константы равновесия), которую принято обозначать, как Кд. Для расчета этой величины применяется закон действующих масс, который устанавливает соотношение между массами полученных и исходных веществ. Электролитическая диссоциация воды — это распад исходных молекул воды на протоны водорода и гидроксильную группу, поэтому выражается уравнением: Кд = [Н+] . [ОН-]/[Н2О]. Эта величина для воды является постоянной и зависит только от температуры, при температуре, равной 25оС, Кд=1.86.10-16.
Зная молярную массу воды (18 грамм/моль), а также пренебрегая концентрацией диссоциированных молекул и принимая массу 1 дм3 воды за 1000 г, можно рассчитать концентрацию недиссоциированных молекул в 1 дм3 воды: [Н2О]=1000/18,0153=55,51 моль/дм3. Тогда из уравнения константы диссоциации можно найти произведение концентраций протонов и гидроксильных групп: [Н+].[ОН-]=1,86.10-16.55,51=1.10-14. При извлечении квадратного корня из полученной величины получают концентрацию протонов (ионов водорода), определяющую кислотность раствора и равную концентрации гидроксильных групп: [Н+]=[ОН-]=1.10-7.
Но в природе воды такой чистоты не существует из-за присутствия в ней растворенных газов или загрязнения воды другими веществами (фактически вода — это раствор различных электролитов), поэтому при 25оС концентрация протонов водорода или концентрация гидроксильных групп отличается от величины 1.10-7. То есть кислотность воды обусловлена протеканием не только такого процесса, как диссоциация воды. является отрицательным логарифмом концентрации водородных ионов (рН), он введен для оценки кислотности или щелочности воды и водных растворов, так как числами с отрицательными степенями пользоваться затруднительно. Для чистой воды рН=7, но так как в природе чистой воды нет, и диссоциация воды протекает наряду с распадом других растворенных электролитов, то водородный показатель может быть меньше или больше 7, то есть для воды, практически, рН≠7.